
设NA为阿伏加德罗常数的值,下列叙述正确的是
①常温常压下,18g14CH4所含中子数目为8 NA
②1L0.1mol·L-1的氨水中有0.1NA个NH4+
③1mol Na2O2中含有NA个阴离子
④1L1mol·L-1NaClO 溶液中含有ClO-的数目为NA
⑤78g 苯含有C=C双键的数目为3NA
⑥0.1molN2和0.3molH2在某密闭容器中充分反应,转移电子的数目为0.6NA
⑦60gSiO2晶体中含有硅氧键的数目为4NA
A.①③⑦ B.②③⑥ C.②④⑥ D.①④⑤⑦
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:
化学反应中,有时存在“一种物质过量,另一种物质仍不能完全反应”的情况。下列反应中属于这种情况的是
A.过量的浓盐酸与MnO2反应 B.过量的Zn与18 mol/L的硫酸反应
C.过量的Fe与稀硝酸反应 D.过量的H2与N2在催化剂存在下反应
查看答案和解析>>
科目:高中化学 来源: 题型:
二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的消毒剂,是一种黄绿色的气体,易溶于水。
Ⅰ.(1) ClO2可由KClO3在H2SO4存在的条件下与Na2SO3反应制得。则该反应的氧化产物与还原产物的物质的量之比是________。
Ⅱ.实验室也可用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料制备ClO2,其流程如下:

(2) 写出电解时发生反应的化学方程式:____________。
(3) 除去ClO2中的NH3可选用的试剂是________。(填序号)
A.饱和食盐水 B.碱石灰
C.浓硫酸 D.水
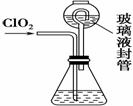
(4) 测定ClO2(如右图)的过程如下:在锥形瓶中加入足量的碘化钾,用100 mL水溶解后,再加3 mL硫酸溶液;在玻璃液封管中加入水;将生成的ClO2气体通过导管在锥形瓶中被吸收;将玻璃封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液,用c mol·L-1硫代硫酸钠标准溶液滴定(I2+2S2O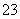 = 2I-+S4O
= 2I-+S4O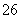 ),共用去V mL硫代硫酸钠溶液。
),共用去V mL硫代硫酸钠溶液。
①装置中玻璃液封管的作用是_______________________________________。
②请写出上述二氧化氯气体与碘化钾溶液反应的离子方程式__________________。
③滴定终点的现象是________________________________________________。
④测得通入ClO2的质量m(ClO2)=________。(用含c、V的代数式表示)
(5) 用ClO2处理过的饮用水(pH为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子ClO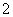 。2001年我国卫生部规定,饮用水的ClO
。2001年我国卫生部规定,饮用水的ClO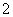 含量应不超过0.2 mg·L-1。若饮用水中ClO
含量应不超过0.2 mg·L-1。若饮用水中ClO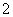 的含量超标,可向其中加入适量的Fe2+,该反应的氧化产物是____________ (填化学式),其发生反应的离子方程式为_________________ __________。
的含量超标,可向其中加入适量的Fe2+,该反应的氧化产物是____________ (填化学式),其发生反应的离子方程式为_________________ __________。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图为某市售盐酸试剂瓶标签上的部分数据.则该盐酸的物质的量浓度是( )
| 盐酸 化学式:HCl 相对分子质量:36.5 密度:1.18g/cm3 HCl的质量分数:36.5% 符合GB622﹣89 |
|
| A. | 3mol/L | B. | 8.4mol/L | C. | 11.8mol/L | D. | 0.5mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
4.8gO2和0.2molCO2,质量之比是 ,在同温同压下的体积之比是 .相同物质的量的SO2和SO3,所含分子的数目之比为 ,所含O原子的物质的量之比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
钠铝合金(常温液态)可作为核反应堆的载热介质。下列说法正确的是
A该合金的熔点高于金属钠的熔点
B.若将钠铝合金投入水中得到无色溶液且无固体剩余,则n(Al)>n(Na)
C.若将钠铝合金投入FeCl3溶液中有Fe(OH)3沉淀生成
D.等质量的钠铝合金中铝的含量越大,与足量盐酸反应时放出的氢气越少
查看答案和解析>>
科目:高中化学 来源: 题型:
近期,世界范围内有成千上万个湖泊变为鱼类绝迹的死湖,数以千万公顷计的森林衰败枯萎,大片土地沙漠化……将这些现象与频繁降落的酸雨相联系,人们认为,酸雨是肇事主因。某研究小组研究某地硫酸型酸雨的形成,有人提出以下猜想:
猜想一:


猜想二:
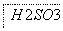

猜想三:以上两过程同时存在
有关上述猜想,收集一定量该地区刚下的雨水进行实验,下列判断中错误的是
A.若猜想一或猜想三正确,该雨水加入盐酸后,再加入BaCl2溶液,有白色沉淀生成
B.若只存在猜想二的过程,则该雨水的pH随时间延长而增大
C.若存在猜想二的过程,则该雨水可能使品红溶液褪色
D.上述任意一个猜想正确,该地区雨水的pH均小于5.6
查看答案和解析>>
科目:高中化学 来源: 题型:
图甲、图乙分别表示反应CO2(g)+H2(g) CO(
CO( g)+H2O(g) ΔH>0在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况,下列说法正确的是
g)+H2O(g) ΔH>0在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况,下列说法正确的是
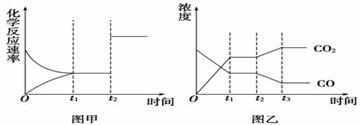
A.图甲中t2时刻发生改变的条件是增大反应物的浓度
B.图甲中t2时刻发生改变的条件可能是增大压强
C.图乙中t2时刻发生改变的条件是升高温度
D.图乙中t2时刻发生改变的条件是从体系中分离出水蒸气
查看答案和解析>>
科目:高中化学 来源: 题型:
【化学—选修5:有机化学基础】(15分)
化合物G的合成路线如下:
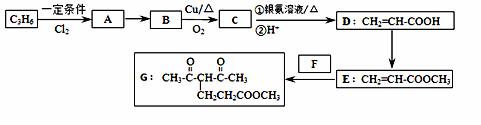
(1)D中含氧官能团的名称为 ,1 mol G发生加成反应最多消耗 mol H2 。
(2)除掉E中含有少量D的试剂和分离方法分别是 , ;
(3)下列说法正确的是 (填字母序号)。
a.A易溶于水
b.只用溴水即可确定C中含有碳碳双键
c.E经加聚、碱性条件下水解,所得高聚物可做具有高吸水性能的树脂
d.E是CH2=CHCOOCH2CH3的同系物
(4)写出A→B的化学反应方程式 ;
写出C和银氨溶液反应的离子方程式 。
(5)反应E + F→ G属于下列麦克尔加成反应类型,则F的结构简式为 。

(6)比G少2个氢原子的物质具有下列性质:①遇FeCl3溶液显紫色;②苯环上的一氯取代物只有一种;③1mol物质最多可消耗2mol Na和1mol NaOH。任写一种该物质的结构简式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com