
【题目】将含有C、H、O的有机物3.24 g装入元素分析装置,通入足量的O2使之完全燃烧,将生成的气体依次通过CaCl2管(A)和碱石灰(B),测得A管质量增加了2.16 g,B管增加了9.24 g,已知该有机物的相对分子质量为108。
(1)求此有机物的分子式。
(2)该有机物1分子中有1个苯环,试写出它的同分异构体的结构简式。
【答案】(1)C7H8O;(2)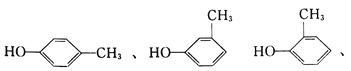
![]()
【解析】考查有机物的分子式的确定,同分异构体的书写,(1)CaCl2的作用是吸收水蒸气,其质量增加是水的质量,m(H2O)=2.16g,水蒸气的物质的量为2.16/18mol=0.12mol,碱石灰的作用是吸收CO2,其质量增加为CO2的质量,m(CO2)=9.24g,其物质的量为n(CO2)=9.24/44mol=0.21mol,C和H来自于有机物,因此有机物中C和H物质的量分别是0.21mol、0.24mol,氧原子的物质的量为(3.24-0.21×12-0.24×1)/16mol=0.03mol,有机物的最简式为C7H8O,因为相对分子质量为108,则有机物的分子式为C7H8O;(2)此有机物可以醇、也可以是醚、酚,因此同分异构体为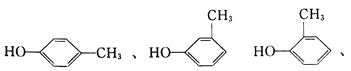
![]() 。
。


 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:
【题目】请把符合要求反应的化学方程式的编号填入括号内:
(1)是分解反应又是氧化还原反应的是(____)
(2)是分解反应不是氧化还原反应的是(____)
(3)是化合反应又是氧化还原反应的是(____)
(4)是化合反应不是氧化还原反应的是(____)
(5)不属于四种基本反应类型的氧化还原反应是 (____)
A.2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
B.2Fe+3Cl2![]() 2FeCl3
2FeCl3
C.NH4HCO3![]() NH3↑+H2O+CO2↑
NH3↑+H2O+CO2↑
D.CaO+CO2![]() CaCO3
CaCO3
E.Cl2+H2O![]() HCl+HClO
HCl+HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中不正确的是( )
A. 盐酸滴在石灰石上:CaCO3+2H+![]() Ca2++H2O+CO2↑
Ca2++H2O+CO2↑
B. 向Ba(OH)2溶液中滴入少量的NaHSO4溶液:H++SO42-+Ba2++OH-![]() BaSO4↓+H2O
BaSO4↓+H2O
C. 向Ba(OH)2溶液中滴入过量的NaHSO4溶液:2H++SO42-+Ba2++2OH-![]() BaSO4↓+2H2O
BaSO4↓+2H2O
D. 稀硫酸滴在铜片上:Cu+2H+![]() Cu2++H2↑
Cu2++H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中,含有离子晶体、分子晶体、原子晶体各一种的是
A.KCl、H2SO4、S B.金刚石、Na3PO4、Mg
C.HF、SiC、Ar D.H2O、SiO2、K2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NO2与以SO2能发生反应:NO2(g)+SO2(g)![]() SO3(g)+NO(g)。
SO3(g)+NO(g)。
(1)上述反应涉及的四种氧化物中,_________(填化学式)属于酸性氧化物。
(2)已知:2NO(g)+O2(g)=2NO2(g)△H1=-113.0kJ·mol-1
2SO2(g)+O2(g) ![]() 2SO3(g)△H2=-196.6kJ·mol-1
2SO3(g)△H2=-196.6kJ·mol-1
则NO2(g)+SO2(g)![]() SO3(g)+NO(g)△H=__________
SO3(g)+NO(g)△H=__________
(3)在一恒容密闭容器中,改变原料气配比[n0(NO2):n0(SO2)]进行多组实验(每次实验的温度可能相同,也可能不同),测定NO2的平衡转化率[a(NO2)]。部分实验结果如图所示。

① 当容器内____(填字母)不再随时间的变化而改变时,可以判断反应达到了化学平衡状态。
a.气体的压强 b.气体的平均摩尔质量 c.气体的密度 d. NO2的体积分数
② 若A点对应的实验中,SO2(g)的起始浓度为c0mol/L,经过t min后反应达到平衡,则反应从起始至t min 内的化学反应速率v(NO2)=_____mol/(L·min)。
③ 若要使图中C点的平衡状态变为B 点的平衡状态,则应采取的措施是_________,若要使图中A点的平衡状态变为B 点的平衡状态,则应采取的措施是___________。
(4)将NO2与SO2的混合气体[n0(NO2):n0(SO2)=1]通入2mL0.1mol/L氯化钡溶液中,只生成一种白色沉淀物M,M的化学式为_______,当溶液中的Ba2+恰好完全沉淀(Ba2+的浓度等于1.0×10-5mol/L),通入的混合气体在标准状况下的体积约为______L。(M的Kap=1.0×10-9)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
选项 | 实验探究内容 | 实验用品 |
A | 铜丝在氯气中燃烧 | 坩埚钳、燃烧匙、氯气、铜丝 |
B | 铝热反应 | 铁架台、大蒸发皿、普通漏斗、铝粉、Fe2O3 |
C | 实验室制备氨气 | 试管、集气瓶、酒精灯、NH4Cl、Ca(OH)2 |
D | 用KMnO4晶体配制500mL0.1mol·L-1KMnO4溶液 | 容量瓶、烧杯、玻璃棒、酸式滴定管、KMnO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质与用途具有对应关系的是
A. Al2O3熔点高,可用作耐高温材料
B. FeCl3溶液呈酸性,可用于腐蚀电路板上的Cu
C. 石墨具有导电性,可用于制铅笔芯
D. 浓硫酸具有强氧化性,可用于干燥CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组同学用下列装置和试剂进行实验,探究O2与KI溶液发生反应的条件。

供选试剂:30% H2O2溶液、0.1mol/L H2SO4溶液、MnO2固体、KMnO4固体
(1)小组同学设计甲、乙、丙三组实验,记录如下:
操作 | 现象 | |
甲 | 向I的锥形瓶中加入______,.向I的______中加入30% H2O2溶液,连接I、Ⅲ,打开活塞 | I中产生无色气体并伴随大量白雾;Ⅲ中有气泡冒出,溶液迅速变蓝 |
乙 | 向Ⅱ中加入KMnO4固体,连接Ⅱ、Ⅲ,点燃酒精灯 | Ⅲ中有气泡冒出,溶液不变蓝 |
丙 | 向Ⅱ中加入KMnO4固体,Ⅲ中加入适量0.1mol/L H2SO4溶液,连接Ⅱ、Ⅲ,点燃酒精灯 | Ⅲ中有气泡冒出,溶液变蓝 |
(2)丙实验中O2与KI溶液反应的离子方程式是__________________________。
(3)对比乙、丙实验可知,O2与KI溶液发生反应的适宜条件是___________。为进一步探究该条件对反应速率的影响,可采取的实验措施是________。
(4)由甲、乙、丙三实验推测,甲实验可能是I中的白雾使溶液变蓝。学生将I中产生的气体直接通入下列________溶液(填序号),证明了白雾中含有H2O2。
A.酸性 KMnO4 B. FeCl2 C. Na2S D.品红
(5)资料显示:KI溶液在空气中久置过程中会被缓慢氧化:4KI +O2 +2H2O=2I2 + 4KOH。该小组同学取20 mL久置的KI溶液,向其中加入几滴淀粉溶液,结果没有观察到溶液颜色变蓝,他们猜想可能是发生了反应(写离子方程式)________________________造成的,请设计实验证明他们的猜想是否正确________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下有①6.72L甲烷②3.01×1023个氯化氢分子③13.6 g硫化氢④0.2 mol NH3。下列对这四种气体的关系从小到大表示不正确的是
A.体积:④<①<②<③ B.密度:①<④<③<②
C.质量:④<①<③<② D.氢原子数:②<④<③<①
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com