
| A. | Fe2O3是还原剂 | B. | Al被还原 | ||
| C. | Fe2O3发生还原反应 | D. | 反应中转移3个电子 |
分析 Fe2O3+2Al $\frac{\underline{\;高温\;}}{\;}$ 2Fe+Al2O3反应中Fe的化合价从+3降低到0价,Al的化合价从0价升高到+3价,结合氧化还原反应的概念分析.
解答 解:A、反应中铁元素化合价从+3价降低到0价,化合价降低,作氧化剂,故A错误;
B、Al的化合价从0价升高到+3价,Al作还原剂,故B错误;
C、Fe2O3做氧化剂被还原,发生还原反应,故C正确;
D、Fe2O3+2Al $\frac{\underline{\;高温\;}}{\;}$ 2Fe+Al2O3反应中Fe的化合价从+3降低到0价,转移6个电子,故D错误;
故选:C.
点评 本题考查了氧化还原反应的概念理解,反应特征判断,电子转移的计算,题目较简单.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;与甲分子具有相同电子数且含元素种类相同的离子有(填化学式)OH-、H3O+.
;与甲分子具有相同电子数且含元素种类相同的离子有(填化学式)OH-、H3O+.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯使溴水褪色、乙酸乙酯在加热的条件下使含酚酞的NaOH溶液颜色变浅 | |
| B. | 由氯乙烯制聚氯乙烯、由纤维素制硝酸纤维 | |
| C. | 由油脂制甘油、由蛋白质制氨基酸 | |
| D. | 由甲苯制甲基环己烷、由乙烷制溴乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
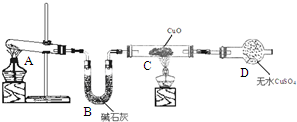 某化学学习小组同学根据实验室现有的制取氨气的药品,设计了如图所示的实验装置(部分夹持仪器未画出),制取并探究氨气的还原性、检验反应产物.请回答下列问题:
某化学学习小组同学根据实验室现有的制取氨气的药品,设计了如图所示的实验装置(部分夹持仪器未画出),制取并探究氨气的还原性、检验反应产物.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2通入Na2S溶液中,能产生淡黄色沉淀 | |
| B. | HCl的热稳定性比H2S强 | |
| C. | HClO4的酸性比H2SO4强 | |
| D. | HCl的酸性比H2S强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
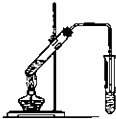 (1)某同学欲用12mol/L的浓盐酸配制1mol/L的盐酸250mL.
(1)某同学欲用12mol/L的浓盐酸配制1mol/L的盐酸250mL.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 限塑的主要意义是减少白色污染 | |
| B. | 塑料袋的材料主要是聚乙烯、聚氯乙烯等 | |
| C. | 聚乙烯、聚氯乙烯等塑料都是天然高分子材料 | |
| D. | 聚乙烯是由乙烯分子通过加成反应聚合而成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4LSO3含有NA个SO3分子 | |
| B. | 1L0.1mol•L-1的氨水含有0.1NA个OH- | |
| C. | 1molFe2+与足量的H2O2溶液反应,转移2NA个电子 | |
| D. | 常温下,23g NO2含有NA个氧原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com