
【题目】以乙烯为原料合成化合物C的流程如图所示: 
(1)乙醇和乙酸中所含官能团的名称分别为:和 .
(2)B物质的结构简式为 .
(3)①、④的反应类型分别为和反应.
(4)反应②和④的化学方程式分别为:
②;
④ .
【答案】
(1)羟基;醛基
(2)CH3CHO
(3)加成;酯化(取代)
(4)CH2=CH2+Cl2→CH2ClCH2Cl;HOCH2CH2OH+2CH3COOH ![]() CH3COOCH2CH2OOCCH+2H2O
CH3COOCH2CH2OOCCH+2H2O
【解析】解:由工艺流程图可知:乙烯与氯气发生加成反应生成物质A:1,2﹣二氯乙烷,1,2﹣二氯乙烷水解生成乙二醇;乙烯与水反应生成乙醇,乙醇发生催化氧化得到物质B:乙醛,乙醛氧化得到乙酸,乙酸与乙二醇在浓硫酸条件下发生酯化反应生成二乙酸乙二酯.(1)乙醇结构简式为C2H5OH,含有官能团为羟基;乙酸结构简式为:CH3COOH,含有官能团为羧基,故答案为:羟基;羧基;(2)乙醇含有醇羟基,在铜做催化剂条件下发生催化氧化生成乙醛,乙醛含有一个甲基和一个醛基,乙醛的结构简式为:CH3CHO,故答案为:CH3CHO;(3)反应①为乙烯在催化剂条件下与水发生加成反应生成乙醇;反应④为乙二醇与乙酸在一定条件下发生酯化反应,有也属于取代反应,故答案为:加成反应;酯化(取代);(4)反应②为乙烯与氯气发生加成反应,化学方程式为:CH2=CH2+Cl2→CH2ClCH2Cl,故答案为:CH2=CH2+Cl2→CH2ClCH2Cl;反应④为乙二醇与乙酸在浓硫酸条件下发生酯化反应,化学方程式为:HOCH2CH2OH+2CH3COOH ![]() CH3COOCH2CH2OOCCH+2H2O,故答案为:HOCH2CH2OH+2CH3COOH
CH3COOCH2CH2OOCCH+2H2O,故答案为:HOCH2CH2OH+2CH3COOH ![]() CH3COOCH2CH2OOCCH+2H2O.
CH3COOCH2CH2OOCCH+2H2O.
由流程图可知:乙烯与氯气发生加成反应生成物质A,则A为:1,2﹣二氯乙烷,1,2﹣二氯乙烷水解生成乙二醇;乙烯与水反应生成乙醇,乙醇发生催化氧化得到物质B,则B为乙醛,乙醛催化氧化得到乙酸;乙酸与乙二醇在浓硫酸条件下发生酯化反应生成二乙酸乙二酯.(1)依据乙醇和乙酸的结构简式判断其含有的官能团名称;(2)乙醇含有醇羟基,在铜做催化剂条件下发生催化氧化生成乙醛;(3)乙烯含有碳碳双键在催化剂条件下能够与水发生加成反应生成乙醇,乙二醇含有羟基,乙酸含有羧基,在一定条件下发生酯化反应;(4)②乙烯与氯气发生加成反应生成1,2﹣二氯乙烷;④乙二醇与乙酸在浓硫酸条件下发生酯化反应生成二乙酸乙二酯和水.


科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:2H2(g)+O2(g)=2H2O(l)△H=﹣571.6kJ/mol,H2(g)+![]() O2(g)=H2O(l)△H=﹣285.8kJ/mol,C(s)+
O2(g)=H2O(l)△H=﹣285.8kJ/mol,C(s)+![]() O2(g)=CO (g)△H=﹣110.5KJ/moL,C(s)+O2(g)=CO2(g)△H=﹣393.5KJ/moL.回答下列各问题:
O2(g)=CO (g)△H=﹣110.5KJ/moL,C(s)+O2(g)=CO2(g)△H=﹣393.5KJ/moL.回答下列各问题:
(1)H2的燃烧热为 ,C的燃烧热为
(2)燃烧10gH2生成液态水,放出的热量为
(3)盖斯定律在生产和科学研究中有很重要的意义,有些反应的反应热虽然无法直接测得,但可通过间接的方法测定,则由已知条件得CO的燃烧热为 ,其燃烧热的热化学方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应2H2O2 = 2H2O+O2↑,下列条件中,反应速率最快的是( )
A. 10 ℃,5 mL 3% H2O2溶液B. 10 ℃,5 mL 5% H2O2溶液
C. 30 ℃,10 mL 5% H2O2溶液D. 30 ℃,5 mL 5% H2O2溶液且加入少量MnO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列反应中,水只作氧化剂的是( )
A.2F2+2H2O═4HF+O2
B.2Na+2H2O═2NaOH+H2↑
C.CaO+H2O═Ca(OH)2
D.2H2O ![]() 2H2↑+O2↑
2H2↑+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据化学反应的实质是旧键断裂和新键形成这一观点,下列变化属于旧键断裂但没有发生化学反应的是( )
A. 氯化钠受热熔化B. 石墨在高温高压下转化为金刚石
C. 单质碘受热升华D. 固态S8加热到444.6℃时变成硫蒸气S2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属晶体、离子晶体、分子晶体采取密堆积方式的原因是( )
A.构成晶体的微粒均可视为圆球
B.三种晶体的构成微粒相同
C.金属键、离子键、范德华力均无饱和性和方向性
D.三种晶体构成微粒的多少及相互作用力相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知苯甲酸微溶于水,易溶于乙醇、乙醚,有弱酸性,酸性比醋酸强.它可用于制备苯甲酸乙酯和苯甲酸铜. (一)制备苯甲酸乙酯![]() +C2H5OH
+C2H5OH ![]()
![]() +H2O
+H2O
相关物质的部分物理性质如上表格:
催化剂组分质量分数(%) | CuO | 0 | 25 | 50 | 75 | 100 |
ZnO | 100 | 75 | 50 | 25 | 0 | |
达到平衡所需要时间(h) | 2.5 | 7.4 | 8.1 | 12 | 无催化剂 | |
实验流程如下:
(1)制备苯甲酸乙酯,下列装置最合适的是 , 反应液中的环己烷在本实验中的作用 . 
(2)步骤②控制温度在65~70℃缓慢加热液体回流,分水器中逐渐出现上、下两层液体,直到反应完成,停止加热.放出分水器中的下层液体后,继续加热,蒸出多余的乙醇和环己烷.反应完成的标志是 .
(3)步骤③碳酸钠的作用是 , 碳酸钠固体需搅拌下分批加入的原因 .
(4)步骤④将中和后的液体转入分液漏斗分出有机层,水层用25mL乙醚萃取,然后合并至有机层,用无水MgSO4干燥.乙醚的作用 .
(5)步骤⑤蒸馏操作中,下列装置最好的是(填标号),蒸馏时先低温蒸出乙醚,蒸馏乙醚时最好采用(水浴加热、直接加热、油浴加热). 
(6)(二)制备苯甲酸铜 将苯甲酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2粉未,然后水浴加热,于70~80℃下保温2~3小时;趁热过滤,滤液蒸发冷却,析出苯甲酸铜晶体,过滤、洗涤、干燥得到成品.
混合溶剂中乙醇的作用是 , 趁热过滤的原因
(7)本实验中下列药品不能代替氢氧化铜使用的是
A.醋酸铜
B.氧化铜
C.碱式碳酸铜
D.硫酸铜
(8)洗涤苯甲酸铜晶体时,下列洗涤剂最合适的是
A.冷水
B.热水
C.乙醇
D.乙醇水混合溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋中有丰富的食品、矿产、能源、药物和水产资源等(如图所示),下列有关说法正确的是( ) 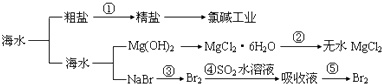
A.第①步中除去粗盐中的SO42﹣、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
B.工业上金属钠是通过氯碱工业制取
C.从第③步到第⑤步的目的是为了浓缩
D.在第③④⑤步中溴元素均被氧化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com