
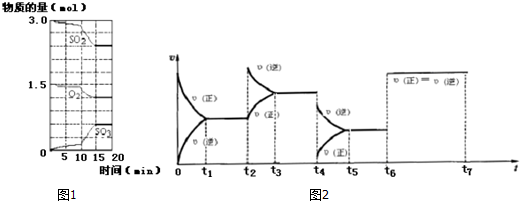
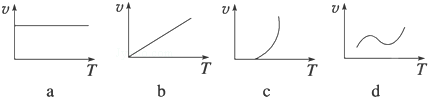
分析 (1)10min到15min时,SO2、O2的物质的量减小,且减少的量为2:1,SO3物质的量增大,则改变条件使平衡正向移动,以此来解答;
(2)当t1=15min时反应达平衡,这段时间内此反应的平均速率v(SO3)=$\frac{△c}{△t}$,SO2的转化率为$\frac{二氧化硫的变化量}{二氧化硫的起始量}×100%$,O2的平衡浓度C(O2 )=$\frac{氧气的物质的量}{容器的体积}$,该反应的化学平衡常数K=$\frac{生成物的浓度幂之积}{反应物浓度幂之积}$;
(3)①t2时正反应速率瞬间不变,逆反应速率增大,然后逆反应速率逐渐减小,正反应速率逐渐增大,直至重新达到平衡,说明t2时加入了加入SO3;
t4时正逆反应速率瞬间同时减小,且逆反应速率减小的幅度小于正反应速率,即v(正)<v(逆),平衡向着逆向移动,然后根据压强、温度对该反应的影响判断此时改变的条件;t6时刻正逆反应速率同时增大,且相等,改变的条件不影响化学平衡,则说明使用了催化剂;
②平衡正向移动SO3的百分含量增加;
(4)根据浓度商和平衡常数的大小比较判断化学反应速率.
解答 解:(1)10min到15min时,SO2、O2的物质的量减小,且减少的量为2:1,SO3物质的量增大,则改变条件使平衡正向移动,
A.催化剂对平衡移动无影响,故A不选;
B.增加SO3的物质的量平衡逆向移动,SO2、O2的物质的量增大,故B不选;
C.△H<0为放热反应,升高温度平衡逆向移动,故C不选;
D.2SO2(g)+O2 (g)?2SO3(g)为气体体积减小的反应,则缩小容器体积,压强增大平衡正向移动,与图一致,故D选;
故选ABC;
(2)v(SO3)=$\frac{△c}{△t}$=$\frac{\frac{0.6}{4}}{15}$=0.01mol/(L.min),SO2的转化率为$\frac{二氧化硫的变化量}{二氧化硫的起始量}×100%$=$\frac{0.6}{3}$=20%,O2的平衡浓度C(O2 )=$\frac{1.2}{4}$=0.3 mol/L,平衡常数K=$\frac{(\frac{0.6}{4})^{2}}{\frac{1.2}{4}×(\frac{2.4}{4})^{2}}$=0.21,故答案为:0.01mol/(L.min);20%;0.3 mol/L;0.21;
(3)①t2时改变反应条件的瞬间,正反应速率不变,逆反应速率增大,v(正)<v(逆),平衡向着逆向移动,之后逆反应速率逐渐减小,正反应速率逐渐增大,直至重新达到平衡,说明t2时加入了加入生成物SO3,增大看生成物浓度;
t4时改变条件的瞬间,正逆反应速率瞬间都减小,且正反应速率减小的幅度大于正反应速率,导致v(正)<v(逆),平衡向着逆向移动,若是减小压强,平衡会向着逆向移动,v(逆)>v(正)满足图象的变化;若减小温度,该反应为 放热反应,平衡向着正向移动,v(正)>v(逆),与图象变化不相符,所以t3时刻是减小了压强;
t6时刻,改变条件下后,正逆反应速率都增大,且v(正)=v(逆),说明改变的反应条件不影响化学平衡,所以改变的条件为:加入催化剂;故答案为:增大生成物(SO3)浓度、减压、加催化剂;
②平衡正向移动SO3的百分含量增加,只有t1~t2 平衡正向移动,所以此时A的百分含量最高,故选:A;
(4)Qc=$\frac{(\frac{1+0.6}{4})^{2}}{\frac{2+1.2}{4}×(\frac{2+2.4}{4})^{2}}$=0.165<K,所以平衡正向移动,所以化学反应速率是V(正) 大于V(逆),故答案为:大于.
点评 本题考查平衡常数、平衡移动、平衡影响因素、反应方向的判断、化学平衡图象等,难度中等.


 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 新制的氯水在光照条件下颜色变浅 | |
| B. | H2、I2、HI平衡混合气体加压后颜色变深 | |
| C. | 钢铁在潮湿的空气中容易生锈 | |
| D. | 加入催化剂有利于氨催化氧化的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
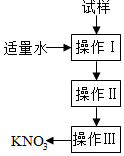 实验室提纯含少量氯化钠杂质的硝酸钾的过程如图所示.下列分析正确的是( )
实验室提纯含少量氯化钠杂质的硝酸钾的过程如图所示.下列分析正确的是( )| A. | 操作Ⅰ是过滤,将固体分离除去 | |
| B. | 操作Ⅱ是加热浓缩,趁热过滤,除去杂质氯化钠 | |
| C. | 操作Ⅲ是过滤、洗涤,将硝酸钾晶体从溶液中分离出来 | |
| D. | 操作Ⅰ~Ⅲ总共只需一次过滤操作 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 实验编号 | NaOH溶液的浓度 (mol/L) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸溶液的体积 (mL) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度 | 25℃~550℃~600℃~700℃ |
| 主要成分 | WO3 W2O5 WO2 W |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 1000 | 1100 |
| 平衡常数 | 0.68 | 0.50 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
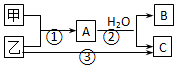
| A. | 若C为酸性气体,则B可能具有两性 | |
| B. | 若C是碱性气体,则B一定是碱 | |
| C. | 若B、C是两种酸,则B、C一定都是一元酸 | |
| D. | 以上3个转变可能都是氧化还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com