
生活和生产中常用到胶体的性质,请看下述四例:
(1)做实验时,手指不慎被玻璃划破,可从急救箱中取氯化铁溶液应急止血,其原理是
_______________________________________________。
(2)在陶瓷工业上常遇到因陶土里混有氧化铁而影响产品质量。解决方法之一是把这些陶土和水一起搅拌,使微粒直径在10-9~10-7m之间,然后插入两根电极,再接通直流电源。这时阳极聚集陶土胶粒,阴极聚集氧化铁胶粒,理由是________。
(3)水泥和冶金工厂常用高压电对气溶胶作用以除去大量烟尘,减少对空气的污染,这种作用运用了________原理。
(4)四氧化三铁在强碱性溶液中与次氯酸盐反应,生成高铁酸盐(FeO42—),FeO42—有强氧化性,可以杀菌消毒。高铁酸盐还有净化水的作用,能净化水的原因是 ______________________________________________________
科目:高中化学 来源: 题型:单选题
有KCl、NaCl、Na2CO3的混合物,其中钠元素的质量分数为31.5%,氯元素的质量分数为27.08%,则Na2CO3的质量分数约为
| A.38% | B.50% | C.75% | D.80% |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
分类方法在化学学科的发展中起了非常重要的作用。图1是某反应在密闭容器中反应前后的分子状况示意图,“ ”和“
”和“ ”分别表示不同的原子。对此反应的分类一定不正确的是
”分别表示不同的原子。对此反应的分类一定不正确的是
| A.置换反应 | B.氧化还原反应 | C.放热反应 | D.化合反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
无机化合物可根据其组成和性质进行分类。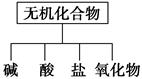
(1)如图所示的物质分类方法是 。
(2)以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在下表②③⑥的后面。
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 |
| 化学式 | ①HCl② | ③ ④Ba(OH)2 | ⑤Na2CO3⑥ | ⑦CO2 ⑧Na2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)NH4Al(SO4)2可作净水剂,其理由是 (用必要的化学用语和相关文字说明)。
(2)相同条件下,0.1 mol·L-1NH4Al(SO4)2中c(NH4+) (填“等于”、“大于”或“小于”)0.1 mol·L-1NH4HSO4中c(NH4+)。
(3)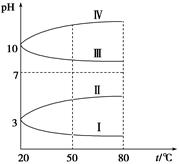
如图是0.1 mol·L-1电解质溶液的pH随温度变化的图像。
①其中符合0.1 mol·L-1NH4Al(SO4)2的pH随温度变化的曲线是 (填写字母),导致pH随温度变化的原因是 ;
②20 ℃时,0.1 mol·L-1NH4Al(SO4)2中2c(SO42-)-c(NH4+)-3c(Al3+)= 。
(4)室温时,向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
试分析图中a、b、c、d四个点,水的电离程度最大的是 ;在b点,溶液中各离子浓度由大到小的排列顺序是 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
根据物质的组成和性质将下列无机化合物进行了分类。
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①H2SO4 ②______ | ③NaOH ④______ | ⑤Na2SO4 ⑥______ | ⑦SO2 ⑧Na2O | ⑨HCl ⑩_____ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)只用一种试剂即可除去少量杂质和鉴别物质。将其填在空格处。
| 编号 | 物质 | 试剂名称或化学式 |
| ① | 除杂质:NaHCO3溶液(Na2CO3) | |
| ② | 除杂质:SiO2(CaCO3) | |
| ③ | 除杂质:FeCl2溶液(FeCl3) | |
| ④ | 鉴别:Na2CO3 Na2SiO3 Na2SO3溶液 | |
| ⑤ | 鉴别:(NH4)2SO4 NH4C1 Na2SO4溶液 | |

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
现有下列4组物质:
| A.CaO、MgO、CO2、CuO | B.H2、Cl2、N2、Cu |
| C.O2、Fe、Cu、Zn | D.HCl、H2O、H2SO4、HNO3 |
| | A组 | B组 | C组 | D组 |
| 分类标准 | 金属氧化物 | | 金属单质 | |
| 不属于该类别的物质 | | Cu | | H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com