
����Ŀ�������������к������ߣ�����������������Ŀռ䡣�������ӵĽṹ��ͼ����V�ͣ�����116��5��������ԭ����һ��Oԭ��Ϊ���ģ�����������Oԭ�ӷֱ�һ���Ǽ��Թ��ۼ����м�Oԭ���ṩ2�����ӣ��Ա�����Oԭ�Ӹ��ṩ1�����ӣ�����һ������Ļ�ѧ����������Oԭ�Ӿ��ȵ�������4�����ӡ���ش�
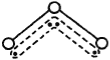
�����ķ��ӽṹ
��1�������������Ĺ�ϵ��___________��
��2��ѡ�����з�����������������ڵȵ�������� ��
���������� �£��ã��� �ã��ӣ��� �ģ��£�ã���
��3��������ijԭ����1��û�и�����ԭ�ӹ��õļ۵��ӽй¶Ե��ӣ���ô����������_______ �Թ¶Ե��ӡ�
��4��������������ת���Ƿ�Ϊ������ԭ��Ӧ___________��
���𰸡� (1)ͬ�������� ��2��C ��3��5 ��4����
��������
�����������1������������������Ԫ���γɵIJ�ͬ���ʣ�����Ϊͬ�������塣
��2��ԭ�����ͼ۵������ֱ���ȵ��ǵȵ����壬��������������ڵȵ����������������ѡC��
��3�����ݳ����Ľṹ�¶Ե��ӵĺ����֪�����������к��еŶԵ�����2��1��2��5�ԡ�
��4����������������ֲ�ͬ�ĵ��ʣ�����֮���ת������ѧ�仯����û�е��ӵĵ�ʧ�����Բ���������ԭ��Ӧ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���Z���Ʊ�ҩ����м��壬�ϳ�Z��·������ͼ��ʾ��

�����й�������ȷ����
A. X����������ԭ�Ӵ���ͬһƽ��
B. X��Y��Z���ܺ�NaOH��Һ��Ӧ
C. ����NaHCO3��Һ����Y��Z
D. 1 mol Y������H2��Ӧ���������3 mol H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ǽ���ʹ�õ�һ�ֽ�����ʹҩ�����ɱ��������ᷴӦ�Ʊ���
![]()
��֪���� �����ױ�������
�� ���������������ʹ���IJ��������������±���
���� | �۵� | �е� | �ܽ��(20 ��) |
�������� | 114.3 �� | 305 �� | 0.46 |
���� | ��6 �� | 184.4�� | 3.4 |
���� | 16.6 �� | 118 �� | ���� |
ʵ�鲽�����£�

����1����50 mLԲ����ƿ�У�����5 mL������7.5 mL�����ἰ����п�ۣ�������ͼװ����װ������
����2�������¶ȼ�ʾ��Լ105 ����С����Ȼ���1 h��
����3�����Ƚ���Ӧ����ﵹ��ʢ��100 mL��ˮ���ձ��У���ȴ����ˣ�ϴ�ӣ��õ��ֲ�Ʒ��
��ش��������⣺
��1������1�м���п�۵�������________________ �����ŷ�ʯ�����á�
��2������2�п����¶ȼ�ʾ��Լ105 ������������������Ҫ������________________�����¶ȹ��ߣ��ᵼ��________________�����η������У����µ��ϣ��¶���________________������������������������������������
��3������3�г���װ������������������ѹϵͳ�⣬��������ƿ��________________����������������
��4������3�õ��Ĵֲ�Ʒ�ɲ�ȡ�ؽᾧ�ķ�����һ���ᴿ������������________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������֧�Թ��зֱ����2 mL 5%H2O2��Һ������������֧�Թ��зֱ�μ�0.1 mol/L FeCl3��Һ��0.1 mol/L CuSO4��Һ���Թ��з�����Ӧ�Ļ�ѧ����ʽ__________������֧�Թ����ܹ۲쵽�Ĺ�ͬ������������__________����ʵ��˵�������ܼӿ컯ѧ��Ӧ���������ܵó��Ľ�����__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭ�������ڻ���ͭ��Ҳ������ʪ����ͭ��ʪ����ͬʱ����ͭ��������������������ҵ��һ�ֹ�������A���������£�
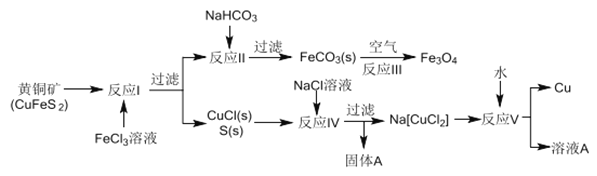
��1����ͭ����Cu �Ļ��ϼ���______����ӦI��65gFeC13 ������________mol CuFeS2��
��2����ҵ�����еĹ��˲��������������������������ʣ������ʺ�������������______��
A�������Ŀ����ϴ� B���������׳��� C�������ʽ�״ D����������״
��3���ڷ�Ӧ���У�����NaHCO3������Һ������CO32-ƽ��Ũ��Ϊ1.2��10-3mol/L���ɲ���FeCO3����ʱ����СFe2+Ũ����_________����֪FeCO3��Ksp��3.0��10-11��
��4����Ӧ�������豸�ײ���������������������շ����Ʊ�������������д����Ӧ�Ļ�ѧ����ʽ_________________��
��5����������A�ijɷ�________��д���ƣ���
��6����ʪ��FeCO3����������ʱ���մ������ڿ�������죬д����صĻ�ѧ����ʽ��_______________��
��7���������п�ʵ��ѭ��ʹ�õ����ʳ���ˮ�⣬����_____________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����3NO2��H2O��2HNO3��NO�У��������뻹ԭ�������ʵ�����Ϊ�� ��
A.1��2B.2��1C.1��3D.3��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Ǽ����������ʵ�һ��ʵ��װ�ã���ش�

��1����XΪ�����������壬YΪ̼������Һʱ���ɹ۲쵽�����ݷų�����ʵ������˵�����������ˮ��Һ����_____�ԡ�
��2����XΪ�����������壬YΪƷ����Һʱ���ɹ۲쵽��������_______����ʵ������˵�����������ˮ��Һ����_______�ԣ���Ӧ���Թ��е���Һ�������һ��ʱ�䣬�ɹ۲쵽��������_______��
��3�����������һ������β����װ�ã����Ż���װ��ͼ��ע����Ҫ��ҩƷ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����12�֣�ij�ֺ�������FeCl2���ʵ�FeCl3��Ʒ����Ҫ�ⶨ������Ԫ�صĺ�����ʵ��������²�����У�
��ȷ����m g��Ʒ��2~3g����
������Ʒ�м���10mL 5mol/L�����ᣬ�ټ�������ˮ�����Ƴ�250mL��Һ��
����ȡ25mL����������õ���Һ������3mL��ˮ������ʹ֮��ȫ��Ӧ��
������Ѹ�ټ���Ũ��Ϊ10%�İ�ˮ����������ֽ��裬ʹ֮��ȫ������
�����ˣ�������ϴ�ӡ����ա���ȴ�������������������ء�
���������������ش�
��1��������ǰ��������ƽ��ָ��ƫ��������������ʱ��ָ��պ��ڱ�ߵ��м䣬��������Ʒ������ ��
A����mg�� B����mg�� C��ǡ��Ϊmg
��2���ܽ���ƷʱҪ�������ᣬԭ���� ��
��3������250mL��Һʱ������250mL������ƿ���ձ��⣬�����õ��IJ��������� ��
��4��������ˮʱ������Ӧ�����ӷ���ʽ�� ��
��5������������ΪW1g�����������պ�������������W2 g������Ʒ����Ԫ�ص����������� ��
��6����������250mL��Һʱ�����õ�����ƿû��ϴ�ɾ�����������������ʱ�����ջ�ʹ��Ԫ�صIJⶨ����������ƫ��������ƫ������������������
��NaCl ��Fe2��SO4��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮΪ��ɢ���ķ�ɢϵ�����ȶ�����ǿ������˳�����е��ǣ� ��
A.��Һ�����塢��Һ
B.��Һ�����塢��Һ
C.���塢��Һ����Һ
D.��Һ����Һ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com