
【题目】在3NO2+H2O=2HNO3+NO中,氧化剂与还原剂的物质的量比为( )
A.1∶2B.2∶1C.1∶3D.3∶1
 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:
【题目】下图是元素周期表的一部分,根据元素在周期表中的位置回答下列问题,
① | ② | ③ | |||||||||||||||
④ | ⑤ | ⑥ | |||||||||||||||
⑦ | ⑧ | ⑨ | |||||||||||||||
⑩ | |||||||||||||||||
(1)元素⑤在周期表中的位置描述为____________,元素⑧的元素符号__________________。
(2)元素①~⑩的最高价氧化物的水化物中,碱性最强的是________________(填化学式)。
(3)元素②的单质的电子式______________,元素②的简单氢化物与其最高价氧化物的水化物反应,生成物中含有的化学键________________(填“离子键”、“极性键”或“非极性键”),元素①、②、③的简单氢化物的沸点由高到低的顺序是___________________(用化学式表示)。
(4)非金属性比较
a.装置1可用于比较元素①、②、⑤的非金属性强弱,则B中发生反应的离子方程式为:_______。
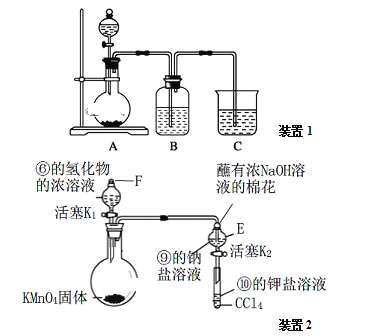
b.打开装置2中玻璃塞F和活塞K1,使液体滴入烧瓶中,待E中溶液颜色不再变化后,打开活塞K2,将E中溶液滴入小试管中,关闭活塞K2,取下小试管振荡,静置,下层液体呈现紫红色。上述实验_______(填“能”或“不能”)证明非金属性⑥>⑨>⑩。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cu(OH)2]=2.2×10-20,在某含有Fe3+和Cu2+的溶液中,c(Fe3+)为4.0×10-8mol·L-1现向该溶液中滴加氨水,当开始出现氢氧化铁沉淀时,溶液的pH及溶液中允许的最大c(Cu2+)为
A. 10 2.2 mol·L-1 B. 4 2.2×10-1 mol·L-1
C. 4 2.2 mol·L-1 D. 10 2.2×10-1 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于自然界中氮循环(如图)的说法不正确的是( )
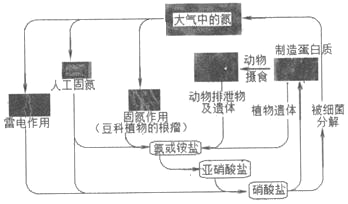
A. 人工固氮可以得到硝酸盐
B. 雷电作用可将氮气直接转化为铵盐
C. 细菌对氮元素的循环有重要作用
D. 亚硝酸盐转化为硝酸盐的过程中,氮元素被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】O3能吸收有害紫外线,保护人类赖以生存的空间。O3分子的结构如图,呈V型,键角116.5℃。三个原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个特殊的化学键——三个O原子均等地享有这4个电子。请回答:
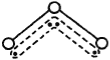
O3的分子结构
(1)臭氧与氧气的关系是___________。
(2)选出下列分子中与O3分子属于等电子体的是 。
A.H2O B.CO2 C.SO2 D.BeCl2
(3)分子中某原子有1对没有跟其他原子共用的价电子叫孤对电子,那么O3分子有_______ 对孤对电子。
(4)O3与O2间的转化是否为氧化还原反应___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Na2CO3溶液中滴加盐酸,反应过程中能量变化如右图所示,下列说法正确的是
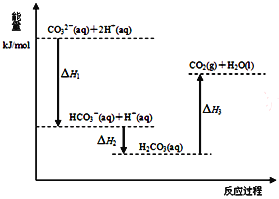
A. 反应HCO3-(aq)+H+(aq)=CO2(g)+H2O(l)为放热反应
B. H1>H2 H2<H3
C. CO32-(aq)+2H+(aq)=CO2(g)+H2O(l) H=(H1+H2+H3)
D. H2CO3(aq)=CO2(g)+H2O(l),若使用催化剂,则H3变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中,表示2A(g)+B(g)![]() 2C(g) △H<0这个可逆反应的正确图像为[注:φ(C)表示体系中物质C的百分含量;体系中压强的增大为压缩体积的结果]
2C(g) △H<0这个可逆反应的正确图像为[注:φ(C)表示体系中物质C的百分含量;体系中压强的增大为压缩体积的结果]


A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H7N9型禽流感是一种新型禽流感,浙江自2015年入秋以来,已累计报告人感染H7N9禽流感4例。研究表明,该病毒对热敏感,煮沸2分钟以上即可失去活性,许多常用消毒药物如:高锰酸钾、漂白粉、氯气等,也都可以将该病毒杀灭。
(1)新制氯水中含有多种微粒,将紫色石蕊试液滴入氯水中,溶液显红色起作用的微粒是___________;过一会儿,溶液颜色逐渐褪去,起作用的微粒是______________。
请写出氯气与水反应的离子方程式_____________________。
(2)工业上制取漂白粉的反应方程式为:__________________。
(3)已知高锰酸钾与浓盐酸混合能产生氯气,化学反应方程式为:2KMnO4 + 16HCl ![]() 2MnCl2 + 2KCl + 8H2O + 5Cl2↑,该反应中氧化剂为____________。
2MnCl2 + 2KCl + 8H2O + 5Cl2↑,该反应中氧化剂为____________。
(4)向漂白粉清液中滴加碳酸钠溶液,有白色沉淀生成,写出发生反应的离子方程式________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com