
【题目】现有下列8种物质:①液氯;②铜;③熔融NaHSO4;④Fe(OH)3固体; ⑤ 盐酸;⑥蔗糖;⑦干冰;⑧红磷固体;⑨ AgCl; ⑩CH3COOH晶体,请按要求回答下列问题(填写物质编号)。
(1) 上述状态下能导电的是_________________________;
(2) 属于电解质是______________;
(3) 属于非电解质的是_______________;
(4) 3.1 g红磷在氯气中充分反应后,生成三氯化磷与五氯化磷的物质的量之比为1:3 , 该反应的化学方程式为___________________;
(5) 写出④与⑤反应的离子方程式________________________;
(6) 写出往NaHSO4溶液中沛加Ba(OH)2溶液至溶液呈中性时的离子方程式________。
【答案】②③⑤ ③④⑨⑩ ⑥⑦ 4P + 9Cl2 = PCl3 + 3PCl5 Fe(OH)3+3H+=Fe3++3H2O Ba2++2OH-+2H++SO42- =BaSO4↓ +2H2O
【解析】
(1)②铜含有自由电子③熔融NaHSO4和⑤盐酸都含有自由移动的离子,三者能导电;故答案为:②③⑤;
(2)③熔融NaHSO4和⑨AgCl熔融状态下能完全电离,属于强电解质;④Fe(OH)3固体;⑩CH3COOH晶体只能部分电离产生自由移动的离子,属于弱电解质,所以属于电解质为:③④⑨⑩;
(3)⑥蔗糖;⑦干冰,本身都不能电离产生自由移动的离子,都是化合物,为非电解质;
故答案为:⑥⑦;
(4)3.1 g红磷的物质的量为:![]() ,在氯气中充分反应,生成三氯化磷与五氯化磷的物质的量之比为1:3,则该反应中氧化剂为氯气,氯元素由0价变为-1价,还原剂为P,化合价由0价变为+3价和+5价,且物质的量之比为1:3,根据电子守恒可知方程式为:4P + 9Cl2 = PCl3 + 3PCl5;
,在氯气中充分反应,生成三氯化磷与五氯化磷的物质的量之比为1:3,则该反应中氧化剂为氯气,氯元素由0价变为-1价,还原剂为P,化合价由0价变为+3价和+5价,且物质的量之比为1:3,根据电子守恒可知方程式为:4P + 9Cl2 = PCl3 + 3PCl5;
(5)氢氧化铁和盐酸反应生成氯化铁和水,离子方程式为:Fe(OH)3+3H+=Fe3++3H2O;
(6)NaHSO4溶液中滴加Ba(OH)2溶液至溶液呈中性,二者反应生成硫酸钡,硫酸钠和水,离子方程式:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O;故答案为:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O;


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
【题目】已知 25℃时,向 0.1mo/L 的碳酸氢钠溶液滴几滴酚酞,呈微红色,则该溶液中
A.若滴加甲基橙溶液呈红色
B.c(HCO3-)>c(CO32-)>c(H2CO3)
C.c(OH-)=c(H+)+ c(H2CO3)- c(CO32-)
D.若加水稀释,![]() 的比值减小
的比值减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以葡萄糖为原料制得的山梨醇(A)和异山梨醇(B)都是重要的生物质转化平台化合物,E 是一种治疗心绞痛的药物。由葡萄糖为原料合成 E 的路线如下:
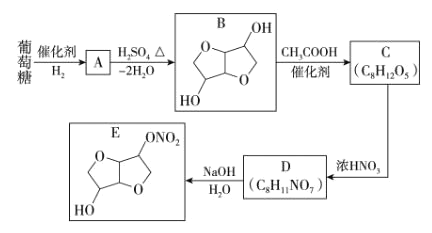
完成下列填空。
(1)A 中含有的官能团的名称为________,由 B 到 C 的反应类型为_________。
(2)写出 C 的结构简式为_____________,写出由 D 到 E 的反应方程式为 _________。
(3)设计 B 到 C 和 D 到 E 的目的是_________。
(4)F 是 B 的同分异构体,且属于二元羧酸,分子中有 3 种化学环境不同的氢原子。写出其结构简式为 _________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油裂解气主要含有丙烯、1,3-丁二烯等不饱和烃,以它们为原料可合成CR橡胶和医药中间体G,合成路线如下:
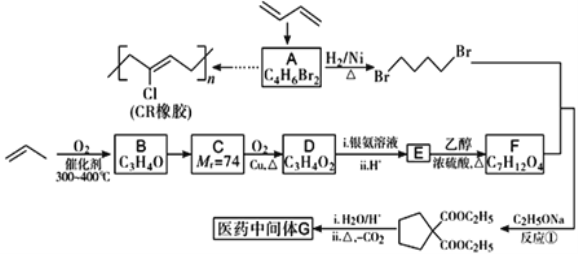
已知:①B、C、D 均能发生银镜反应;
②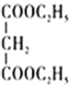
![]()
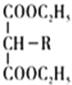
![]() RCH2COOH
RCH2COOH
(1)A的顺式异构体的结构简式为_______。
(2)C中含氧官能团的名称是________,反应①的反应类型为_______。
(3)写出E→F反应的化学方程式:_________。
(4)写出同时满足下列条件的医药中间体G的同分异构体的结构简式: _______。
①与D 互为同系物; ②核磁共振氢谱有三组峰。
(5)用简要语言表述检验B中所含官能团的实验方法:_______。
(6)以A为起始原料合成CR橡胶的线路为______(其它试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型冠状病毒爆发时刻,更能体现化学知识的重要性。下列有关消毒剂的说法中正确的是( )
A.各类消毒剂浓度越大,消毒效果越好
B.为了增强消毒效果,可以将医用酒精、“84”消毒液混用
C.过氧乙酸的结构简式为CH3COOOH,含有-1价氧元素,具有氧化性
D.各类消毒剂均能使病毒蛋白质变性,但是对人体蛋白质无影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.在光照条件下,等物质的量的![]() 与
与![]() 充分反应,只能生成
充分反应,只能生成![]() 和
和![]()
B.对石油分馏产品进行催化裂化,可以提高汽油等轻质油的产量和质量
C.乙炔能使酸性高锰酸钾溶液和溴水褪色,两者褪色的原理不同
D.邻二甲苯只有一种结构,说明苯中的碳碳键是完全相同的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:3Z(s)![]() X(g)+2Y(g) ΔH=akJ·molˉ1(a>0)。下列说法不正确的是
X(g)+2Y(g) ΔH=akJ·molˉ1(a>0)。下列说法不正确的是
A.将0.3molZ置于容器中充分反应生成气体的物质的量一定小于0.3mol
B.达到化学平衡状态时,气体平均摩尔质量不变
C.达到化学平衡状态时,反应放出的总热量可达akJ
D.升高反应温度,逆反应速率增大,正反应速率也增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是一种清洁能源。制氢和储氢作为氢能利用的关键技术,是当前科学家主要关注的热点问题。(1)用甲烷制取氢气的两步反应的能量变化如下图所示:
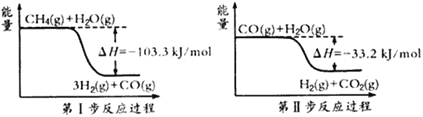
①甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式是________________。
②第Ⅱ步反应为可逆反应。800℃时,若CO的起始浓度为2.0 mol·L-1,水蒸气的起始浓度为3.0 mol·L-1,达到化学平衡状态后,测得CO2的浓度为1.2 mol·L-1,则CO的平衡转化率为__________。
(2)NaBH4是一种重要的储氢载体,能与水反应生成NaBO2,且反应前后B元素的化合价不变,该反应的化学方程式为___________________,反应消耗1mol NaBH4时转移的电子数目为_______。
(3)储氢还可借助有机物,如利用环已烷和苯之间的可逆反应来实现脱氢和加氢。
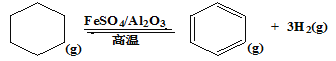
在某温度下,向恒容容器中加入环已烷,其起始浓度为a mol·L-1,平衡时苯的浓度为b mol·L-1,该反应的平衡常数K=____________________(用含a、b的关系式表达)。
(4)一定条件下,如下图所示装置可实现有机物的电化学储氢(除目标产物外,近似认为无其它有机物生成)。
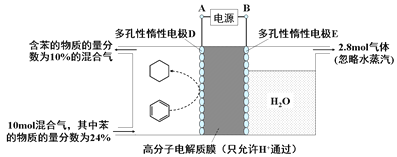
①实现有机物储氢的电极是________;
A.正极 | B.负极 | C.阴极 | D.阳极 |
其电极反应方程为:________________________。
②该储氢装置的电流效率η明显小于100%,其主要原因是相关电极除目标产物外,还有一种单质气体生成,这种气体是_________。由表中数据可知,此装置的电流效率η=______________。[η=(生成目标产物消耗的电子数/转移的电子总数)×100%,计算结果保留小数点后1位]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅的冶炼有很多种方法。
(1)瓦纽科夫法熔炼铅,其相关反应的热化学方程式如下:
① 2PbS(s)+3O2(g)=2PbO(s)+2SO2(g) ΔH1=a kJ·mol-1
② PbS(s)+2PbO(s)=3Pb(s)+SO2(g) ΔH2=b kJ·mol-1
③ PbS(s)+PbSO4(s)=2Pb(s)+2SO2(g) ΔH3=c kJ·mol-1
反应PbS(s)+2O2(g)=PbSO4(s) ΔH=______________ kJ·mol-1(用含a、b、c的代数式表示)。
(2)还原法炼铅,包含反应PbO(s)+CO(g)![]() Pb(s)+CO2(g) ΔH,该反应的平衡常数的对数值与温度的关系如下表:
Pb(s)+CO2(g) ΔH,该反应的平衡常数的对数值与温度的关系如下表:
温度/℃ | 300 | 727 | 1227 |
lgK | 6.17 | 2.87 | 1.24 |
①该反应的ΔH_______0(选填“>”、“<”或“=”)。
②当lgK=1,在恒容密闭容器中放入PbO并通入CO,达平衡时,混合气体中CO的体积分数为______________ (保留两位有效数字);若向容器中充入一定量的CO气体后,平衡向_________ (填“正向”、“逆向”或“不”)移动,再次达到平衡时,CO的转化率_________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com