
【题目】下列电离方程式书写正确的是( )
A.NaHCO3═Na++H++CO32﹣
B.NaHSO4═Na++H++SO42﹣
C.Fe2(SO4)3═Fe3++SO42﹣
D.NH3H2O═NH4++OH﹣
科目:高中化学 来源: 题型:
【题目】某学生设计了三种制备方案:①用KI晶体与浓硫酸反应制HI ②用浓度均为0.1 mol·L-1的氯化铁和氢氧化钠混合制备氢氧化铁胶体 ③用纯碱和石灰水制烧碱,可用的方案是( )
A.①B.③
C.②③D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Y元素最高正价与负价的绝对值之差为4,Y元素与M元素可形成离子化合物,该物质能溶于水并在水中电离出电子层结构相同的离子,该化合物是( )
A.硫化钾
B.硫化钠
C.氯化钠
D.氧化铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无机化合物可根据其组成和性质进行分类
(1)下图所示的物质分类方法名称是。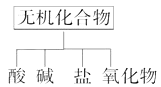
(2)以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在下表②③⑥的后面。
物质类别 | 酸 | 碱 | 盐 | 氧化物 |
化学 | ①HCl | ③ | ⑤Na2CO3 | ⑦CO2 |
(3)写出⑦转化为⑤的化学方程式。
(4)实验室制备⑦常用和反应,检验该气体的方法是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知HClO的酸性比H2CO3弱,下列反应Cl2+H2OHCl+HClO达到平衡后,要使平衡体系中HClO的浓度增大,应采取的方法是( )
A.加入石灰石
B.光照
C.加入固体NaOH
D.加水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,在pH=11的某溶液中,由水电离的c(OH﹣)为( )
①1.0×10﹣7 molL﹣1 ②1.0×10﹣6 molL﹣1
③1.0×10﹣3 molL﹣1 ④1.0×10﹣11 molL﹣1 .
A.③
B.④
C.①或③
D.③或④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同物质的量的Na2O2和Na2O的比较中,不正确的是
A.两种物质所含原子个数之比为4∶3
B.两种物质与足量的水反应后所得溶液的体积相等,溶液的浓度不相等
C.两种物质与足量的CO2反应,消耗气体的质量比为1∶1
D.两种物质中阳离子的物质的量之比为1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、Q、W、R六种短周期元素原子序数依次增大.化合物甲由X、Z、Q三种元素组成,常温下0.1mol/L甲溶液的pH=13.工业上常用电解饱和QR溶液生成甲;化合物乙由X、R两种元素组成;请回答以下问题:
(1)Q的原子结构示意图为 .
(2)Y元素的单质能发生如图所示的转化,则Y元素为(用元素符号表示).在甲溶液中通入足量YZ2气体,所得溶液呈碱性,原因是(用离子方程式和必要的文字说明).
(3)W的单质既能与甲溶液反应,又能与乙溶液反应. ①常温下,将W的单质和甲溶液混合,发生反应的离子方程式为: .
②Q、W两种元素金属性的强弱为QW(填“<”、“>”);
下列表述中证明这一事实的是 .
a.Q的单质的熔点比W单质低
b.Q的最高价氧化物的水化物的碱性比W的最高价氧化物的水化物的碱性强
c.W的原子序数大.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务。
[实验目的]制取乙酸乙酯
[实验原理]甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯。
(1)[装置设计]甲、乙、丙三位同学分别设计了下列三套实验装置:
请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,较合理的是(选填“甲”或“乙”)。丙同学将甲装置中的玻璃管改成了球形干燥管,除起冷凝作用外,另一重要作用是。
(2)[实验步骤]
Ⅰ.按丙同学选择的装置组装仪器,在试管中先加入3 mL乙醇,并在摇动下缓缓加入2 mL浓硫酸充分摇匀,冷却后再加入2 mL冰醋酸;
Ⅱ.将试管固定在铁架台上;
Ⅲ.在试管②中加入适量的饱和Na2CO3溶液;
Ⅳ.用酒精灯对试管①加热;
Ⅴ.当观察到试管②中有明显现象时停止实验。
[问题讨论]
步骤Ⅰ安装好实验装置,加入样品前还应检查
。
(3)写出试管①中发生反应的化学方程式: (注明反应条件)。
(4)试管②中饱和Na2CO3溶液的作用是。
(5)从试管②中分离出乙酸乙酯的实验操作是
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com