
【题目】对于反应:2A(g)+B(g)![]() 2C(g) ΔH<0,下列图像正确的是( )
2C(g) ΔH<0,下列图像正确的是( )
A.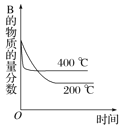 B.
B.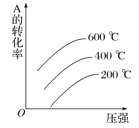
C.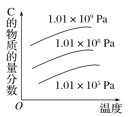 D.
D.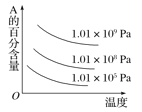
【答案】A
【解析】
由反应2A(g)+B(g)![]() 2C(g)△H<0,可知,该反应为放热反应,升高温度,反应速率增大,平衡向逆反应方向移动,气体反应物的化学计量数之和大于生成物计量数,增大压强,平衡向正反应方向移动,以此解答该题。
2C(g)△H<0,可知,该反应为放热反应,升高温度,反应速率增大,平衡向逆反应方向移动,气体反应物的化学计量数之和大于生成物计量数,增大压强,平衡向正反应方向移动,以此解答该题。
A.该反应为放热反应,升高温度,反应速率增大,到达平衡用的时间少,曲线的斜率增大,平衡向逆反应方向移动,B的物质的量分数增加,A选项正确。
B.反应中气体反应物的化学计量数之和大于生成物计量数,增大压强,平衡向正反应方向移动,A的转化率增大,反应放热,在相同压强下,较高温度时,A的转化率减小,图象不正确,故B选项错误。
C.该反应为放热反应,升高温度,平衡向逆反应方向移动,C的体积分数减小,故C选项错误。
D.该反应为放热反应,升高温度,平衡向逆反应方向移动,A的转化率降低,百分含量升高,D选项错误。
故答案为A。


科目:高中化学 来源: 题型:
【题目】一定温度时,向容积为2L的密闭容器中充入一定量的SO2和O2,发生反应:2SO2(g)+O2(g)![]() 2SO3(g) H=196kJ·moL1,一段时间后达平衡,反应过程中测定的部分数据见下表:
2SO3(g) H=196kJ·moL1,一段时间后达平衡,反应过程中测定的部分数据见下表:
反应时间/min | n(SO2)/mol | n(O2)/mol |
0 | 2 | 1 |
5 | 1.2 | |
10 | 0.4 | |
15 | 0.8 |
下列说法不正确的是
A. 反应在前5min的平均速率为v (SO2)=0.08mol·L1·min1
B. 保持温度不变,向平衡后的容器中再充入0.2molSO2和0.2mol SO3时,v (正)>v (逆)
C. 保持其他条件不变,若起始时向容器中充入2molSO3,达平衡时吸收78.4kJ的热量
D. 相同温度下,起始时向容器中充入1.5mol SO3,达平衡时SO3的转化率为40%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
A.放电时负极反应为:Zn+2OH--2e-=Zn(OH)2
B.充电时阳极反应为:Fe(OH)3+5OH--3e-=FeO42-+4H2O
C.放电时每转移3mol电子,正极有1mol K2FeO4被氧化
D.放电时正极附近溶液的碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是
A. 图甲 中的ΔH1>ΔH2
中的ΔH1>ΔH2
B. 图乙 表示可逆反应A(s)+3B(g)2C(g) ΔH>0
表示可逆反应A(s)+3B(g)2C(g) ΔH>0
C. 图丙 表示充满NO2气体的试管,倒置于水槽中,向其中缓慢通入氧气直至试管中全部充满水,假设溶质不扩散,溶质的物质的量浓度与通入氧气的体积关系
表示充满NO2气体的试管,倒置于水槽中,向其中缓慢通入氧气直至试管中全部充满水,假设溶质不扩散,溶质的物质的量浓度与通入氧气的体积关系
D. 由图丁 可说明烯烃与H2加成反应是放热反应,虚线表示在有催化剂的条件下进行
可说明烯烃与H2加成反应是放热反应,虚线表示在有催化剂的条件下进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】—定温度下,向10mL0.40mol/LH2O2 溶液中加入少量FeCl3溶液(忽略整个过程中溶液体积的变化),不同时刻测得生成O2的体积(已折算为标准状况下)如表所示:
t/min | 0 | 2 | 4 | 6 |
V(O2)/mL | 0 | 9.9 | 17.5 | 22.4 |
资料显示,反应分两步进行:①2Fe3++H2O2=2Fe2++2H++O2;②H2O2+2Fe2++2H+=2H2O+2Fe3+。反应过程中能量变化如图所示。下列说法正确的是

A. Fe2+的作用是增大过氧化氢的分解速率
B. 反应①、②均是放热反应
C. 反应2H2O2(aq)=2H2O(l)+O2(g)是吸热反应
D. 0~6min内的平均反应速率v(H2O2)=3.33×10-2mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某恒温下,在一个容积为2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
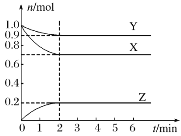
(1)反应开始至2min,以气体Z表示的平均反应速率为___;
(2)达平衡时X与Y的转化率之比为__;
(3)反应达到平衡时:压强是开始时的__倍;
(4)若此时将容器的体积缩小为原来的![]() 倍,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为__(填“放热”或“吸热”)反应。
倍,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为__(填“放热”或“吸热”)反应。
(5)达平衡时该反应放出9.2kJ的热量,则该反应的热化学方程式为:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温、恒容:N2 (g) + 3H2(g)![]() 2NH3(g);△H=-QkJ·mol-1。向甲、乙两个容积相同的密闭容器中分别充入1molN2、3molH2和2molNH3、1molAr,平衡时有关数据如下:
2NH3(g);△H=-QkJ·mol-1。向甲、乙两个容积相同的密闭容器中分别充入1molN2、3molH2和2molNH3、1molAr,平衡时有关数据如下:
容 器 | 甲 | 乙 |
平衡时NH3的体积分数 | ω1 | ω2 |
平衡时N2的浓度(mol·L-1) | c1 | c2 |
反应的能量变化(kJ) | Q1 | Q2 |
反应物的转化率 | α1 | α2 |
下列说法不正确的是
A.ω1=ω2B.c1 =c2C.Q1+Q2 =QD.α1+α2 = 1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应![]() ,某研究小组将4moX和2molY置于一容积不变的密闭容器中,测定1min内X的转化率,得到的数据如表所示,下列判断正确的是( )
,某研究小组将4moX和2molY置于一容积不变的密闭容器中,测定1min内X的转化率,得到的数据如表所示,下列判断正确的是( )
t/min | 2 | 4.5 | 5 | 6 |
X的转化率 | 30% | 40% | 70% | 70% |
A.随着反应的进行,混合气体的密度不断增大
B.反应在5.5min时,![]()
C.6min时,容器中剩余1.4molY
D.其他条件不变,将X的物质的量改为10mol,则可得到4molZ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将0.1molAgCl固体加入1L0.1molL-1Na2CO3溶液中,充分搅拌(不考虑液体体积变化),已知:Ksp(AgCl)=2×10-10;Ksp(Ag2CO3)=1×10-11,下列有关说法正确的是( )
A.沉淀转化反应![]() 的平衡常数为20molL-1
的平衡常数为20molL-1
B.约有10-5molAgCl溶解
C.反应后溶液中的:c(Na+)>c(CO32-)>c(Cl-)>c(Ag+)>c(H+)
D.反应后溶液中的:c(Na+)+c(Ag+)=2c(CO32-)+c(HCO3-)+c(Cl-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com