
【题目】某元素R的最高价氧化物的水化物是HnRO2n-2,则在气态氢化物中R元素的化合价是
A.3n-12B.12-3nC.3n-4D.3n-10
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:
【题目】元素R、T、X、Y、Z在元素周期表中的相对位置如下图所示,其中Z单质与H2混合遇强光会发生爆炸。则下列判断错误的是
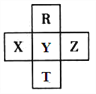
A. 原子半径 Z>Y>R
B. R与Y的电子数相差8
C. 非金属性:Z>Y>X
D. HZO4是目前无机酸中最强的含氧酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,用化学用语回答下列问题:
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
1 | ① | ||||||
2 | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)⑧的原子结构示意图为______________________________________________。
(2)③⑧⑩的最高价含氧酸的酸性最强的是__________(填化学式)。
(3)③的气态氢化物与③的最高价氧化物对应的水化物反应生成盐的化学方程式是_______。
(4)①④⑩三种元素的原子能形成原子数目比为1∶1∶1的共价化合物,它的电子式为_____________,②④两种元素形成原子数目比为1∶2的共价化合物的结构式为___________________________。
(5)⑤的最高价氧化物的水化物与⑦的最高价氧化物反应的离子方程式为_________,⑨的最高价氧化物的水化物的浓溶液与铜反应的化学方程式为:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以Cl2、NaOH、(NH2)2CO(尿素)和SO2为原料可制备N2H4·H2O(水合肼)和无水Na2SO3,其主要实验流程如下:

已知:①Cl2+2OH![]() ClO+Cl+H2O是放热反应。
ClO+Cl+H2O是放热反应。
②N2H4·H2O沸点约118 ℃,具有强还原性,能与NaClO剧烈反应生成N2。
(1)步骤Ⅰ制备NaClO溶液时,若温度超过40 ℃,Cl2与NaOH溶液反应生成NaClO3和NaCl,其离子方程式为____________________________________;实验中控制温度除用冰水浴外,还需采取的措施是____________________________________。
(2)步骤Ⅱ合成N2H4·H2O的装置如题19图1所示。NaClO碱性溶液与尿素水溶液在40 ℃以下反应一段时间后,再迅速升温至110 ℃继续反应。实验中通过滴液漏斗滴加的溶液是_____________;使用冷凝管的目的是_________________________________。

(3)步骤Ⅳ用步骤Ⅲ得到的副产品Na2CO3制备无水Na2SO3(水溶液中H2SO3、![]() 、
、![]() 随pH的分布如题19图2所示,Na2SO3的溶解度曲线如题19图3所示)。
随pH的分布如题19图2所示,Na2SO3的溶解度曲线如题19图3所示)。
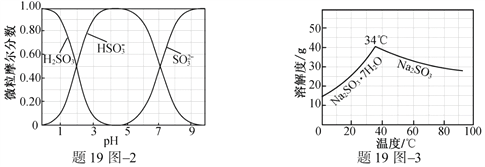
①边搅拌边向Na2CO3溶液中通入SO2制备NaHSO3溶液。实验中确定何时停止通SO2的实验操作为_________________。
②请补充完整由NaHSO3溶液制备无水Na2SO3的实验方案: _______________________,用少量无水乙醇洗涤,干燥,密封包装。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y两元素是同周期的非金属元素,如果X 原子半径比Y的大,下面说法正确的是 ( )
A.最高价氧化物对应的水化物的酸性,X的比Y的强
B.X的非金属性比Y的强
C.X的阴离子比Y的阴离子还原性强
D.X的气态氢化物比Y的稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一块镁铝合金溶于盐酸后,加入过量氢氧化钠溶液,过滤后灼烧沉淀物,所得白色粉末的质量等于原合金的质量,则该合金中镁铝的质量比是( )
A.3:2B.2:3C.1:1D.2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种强氧化性气体(高浓度时呈红黄色,低浓度时呈黄色),在消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过下图所示装置(夹持装置略)对其进行制备、收集、吸收并制取NaClO2。
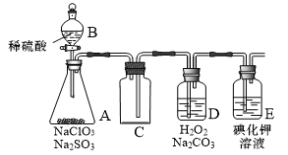
(1)仪器A的名称是______。
(2)图中装置有一明显错误,请指出:______。
(3)打开B的活塞,A中有ClO2生成,D中吸收ClO2后生成NaClO2和NaHCO3,写出D中所发生反应的离子方程式:______。
(4)E中溶液出现黄色能否说明ClO2未被H2O2和Na2CO3的混合溶液充分吸收,判断并说明理由:______。
(5)写出一种提高ClO2吸收率的方法:______。
(6)E装置吸收逸出的少量ClO2气体后所得溶液(pH为5.5~6.5)中存在少量ClO2—,当pH≤2.0时,ClO2—能被I—还原。请补充完整检验E装置溶液中存在少量ClO2—的实验方案:取一定体积E装置中的溶液于分液漏斗中,______,则溶液中存在ClO2—。(实验中须使用的试剂有:CCl4、稀硫酸、淀粉溶液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. NO2、SO2、BF3、NCl3分子中没有一个分子中原子的最外层电子都满足8电子稳定结构
B. PH3和CH4都是正四面体形分子且键角都为109°28′
C. NH3分子中有一对未成键的孤电子对,它对成键电子的排斥作用较强
D. NH4+的电子式为 ,离子呈平面正方形结构
,离子呈平面正方形结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不属于有机物的特点是( )
A.大多数有机物难溶于水,易溶于有机溶剂
B.有机反应比较复杂,一般反应速率较慢
C.绝大多数有机物受热不易分解,且不易燃烧
D.绝大多数有机物是非电解质,不易导电,熔点较低
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com