
【题目】25℃时,NaCN溶液中CN-、HCN浓度所占分数(![]() )随pH变化的关系如图甲所示,其中a点的坐标为(9.5,0.5)。向10mL0.01mol·L-1NaCN溶液中逐滴加入0.01mol·L-1的盐酸,其pH变化曲线如图乙所示。下列溶液中的关系中一定正确的
)随pH变化的关系如图甲所示,其中a点的坐标为(9.5,0.5)。向10mL0.01mol·L-1NaCN溶液中逐滴加入0.01mol·L-1的盐酸,其pH变化曲线如图乙所示。下列溶液中的关系中一定正确的
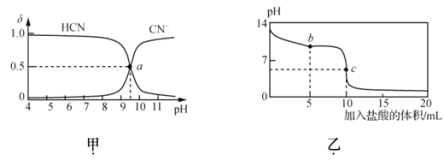
A.图甲中pH=7的溶液:c(Cl-)=c(HCN)
B.常温下,NaCN的水解平衡常数:Kh(NaCN)=10-4.5mol/L
C.图乙中b点的溶液:c(CN-)>c(Cl-)>c(HCN)>c(OH-)>c(H+)
D.图乙中c点的溶液:c(Na+)+ c(H+)= c(HCN)+ c(OH-)+ c(CN-)
【答案】B
【解析】
A. 图甲中可以加入HCN调节溶液的pH=7,溶液中不一定存在Cl-,即不一定存在c(Cl-)=c(HCN),故A错误;
B. a点的坐标为(9.5,0.5),此时c(HCN)=c(CN),HCN的电离平衡常数为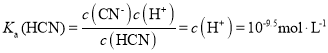 ,则NaCN的水解平衡常数
,则NaCN的水解平衡常数![]() ,故B正确;
,故B正确;
C. b点加入5mL盐酸,反应后溶液组成为等浓度的NaCN、HCN和NaCl,由图乙可知此时溶液呈碱性,则HCN的电离程度小于CN的水解程度,因此c(HCN)>c(CN),故C错误;
D. c点加入10mL盐酸,反应后得到等浓度的HCN和NaCl的混合溶液,任何电解质溶液中都存在电荷守恒和物料守恒,根据物料守恒得c(Cl)=c(HCN)+c(CN),而根据电荷守恒可知,c(Na+)+ c(H+)= c(Cl)+ c(OH)+ c(CN),则c(Na+)+ c(H+)= c(HCN)+ c(OH-)+ 2c(CN-),故D错误;
故选B。


科目:高中化学 来源: 题型:
【题目】实验室用燃烧法测定某种氨基酸(CxHyOzNm)的分子组成。取Wg该种氨基酸放在纯氧中充分燃烧,生成二氧化碳、水和氮气。按下图所示装置进行实验。

回答下列问题:
(1)实验开始时,首先通入一段时间的氧气,其理由是__________________。
(2)以上装置中需要加热的仪器有_______ (填写字母),操作时应先点燃_____处的酒精灯。
(3)A装置中发生反应的化学方程式是____________________________。
(4)D装置的作用是____________________________。
(5)读取氮气的体积时,应注意①_________________;②_________________。
(6)实验中测得氮气的体积为VmL(标准状况),为确定此氨基酸的分子式,还需要的有关数据有____________________。
A.生成二氧化碳气体的质量
B.生成水的质量
C.通人氧气的体积
D.氨基酸的相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次氯酸钾是―种白色粉末,极易溶于冷水,遇热水则分解,在空气中极不稳定,受热后迅速自行分解。工业上生产次氯酸押的流程如下:
![]()
下列说法正确的是
A. 步骤Ⅰ、Ⅱ发生的反应均为非氧化还原反应
B. 步骤Ⅱ采取的方法是加入足量水以制得Ca(OH)2溶液
C. 步骤Ⅲ氧化时,氯气是氧化剂,Ca(OH)2是还原剂
D. 步骤Ⅵ的操作包括蒸发浓缩,冷却结晶、在空气中晾干
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在国家卫健委2020年2月发布的《最新版新型冠状病毒肺炎诊疗方案(试行第六版)》中,新增了几款有疗效的药物,其中一款是老药新用,结构如图所示。已知该药物由短周期元素组成,X、Y为同主族元素,原子半径X小于Y,X、Y原子的质子数之和减去Y原子最外层电子数即为Z元素的原子序数。下列说法错误的是

A.元素非金属性X>Y<Z
B.X的氢化物显酸性
C.Y的最高价氧化物的水化物是中强酸
D.在分子中,存在极性共价键和非极性共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钡在氧气中燃烧时得到一种钡的氧化物晶体,结构如图所示,有关说法不正确的是( )

A. 该晶体属于离子晶体
B. 晶体的化学式为Ba2O2
C. 该晶体晶胞结构与NaCl相似
D. 与每个Ba2+距离相等且最近的Ba2+共有12个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组用如下图所示装置A、B分别探究金属铝与稀氢氧化钠溶液的反应,实验过程中装置A中烧杯内的溶液温度升高,装置B中烧杯的电流计指针发生偏转,请回答以下问题。

(1)装置A烧杯中反应的离子方程式为_________。
(2)装置B中Mg上的现象是_________,Al发生的电极反应式是__________________。
(3)当装置B导线中通过0.3mol电子时,装置B烧杯中溶液的质量变化为__________(填增重或减轻多少克)。
(4)该小组同学反思原电池的原理,其中观点正确的是_________(填字母序号)。
A.原电池反应的过程中一定有电子转移
B.原电池装置需要2个电极
C.电极一定不能参加反应
D.氧化反应和还原反应可以拆开在两极发生
E.原电池的正负极不仅与金属的活动性有关,而且也与电解质溶液有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2是一种重要的氧化物,可用于生产三氧化硫、硫酸、亚硫酸盐、硫代硫酸盐,也可用作熏蒸剂、防腐剂、消毒剂、还原剂等。
(1)SO2性质多变,若将SO2气体通入氢硫酸中,能看到的现象为:__________,该反应中SO2表现出______性;若将SO2气体通入酸性高锰酸钾溶液中,离子反应方程式为_________,该反应中SO2表现出__________性。
(2)SO2有毒,且能形成酸雨,是大气主要污染物之一。石灰-石膏法和碱法是常用的烟气脱硫法。石灰-石膏法的吸收原理:①SO2+Ca(OH)2=CaSO3↓+H2O②2CaSO3+O2+4H2O=2CaSO4·2H2O碱法的吸收原理:将含SO2的尾气通入足量的烧碱溶液中,请写出对应的化学反应方程式__________;
已知:
试剂 | Ca(OH)2 | NaOH |
价格(元/kg) | 0.36 | 2.9 |
余石灰-石膏法相比,碱法的优点是吸收快、效率高,缺点是__________;
(3)在石灰-石膏法和碱法的基础上,设计了双碱法,能实现物料循环利用。

上述方法中,实现循环利用的物质是__________,请用化学方程式表示在Na2SO3溶液中加入CaO后的反应原理__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国研究人员研制出一种新型复合光催化剂,利用太阳光在催化剂表面实现高效分解水,主要过程如下图所示。下列说法不正确的是( )

A.整个过程实现了光能向化学能的转换
B.过程Ⅱ有O-O单键生成并放出能量
C.过程Ⅲ发生的化学反应为:2H2O2 ═ 2H2O + O2↑
D.整个过程的总反应方程式为:2H2O ═ 2H2↑ + O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香豆素衍生物Q是合成抗肿瘤、抗凝血药的中间体,其合成路线如下。

已知:
I、
II、![]()
(1)A的分子式为C6H6O,能与饱和溴水反应生成白色沉淀。
① 按官能团分类,A的类别是_________。
② 生成白色沉淀的反应方程式是_________。
(2)A→B的反应方程式是_________。
(3)D→X的反应类型是_________。
(4)物质a的分子式为C5H10O3,核磁共振氢谱有两种吸收峰,由以下途径合成:

物质a的结构简式是_________。
(5)反应ⅰ为取代反应。Y只含一种官能团,Y的结构简式是_________。
(6)生成香豆素衍生物Q的“三步反应”,依次为“加成反应→消去反应→取代反应”,其中“取代反应”的化学方程式为_________。
(7)研究发现,一定条件下将香豆素衍生物Q水解、酯化生成 ![]() ,其水溶性增强,更有利于合成其他药物。请说明其水溶性增强的原因:______。
,其水溶性增强,更有利于合成其他药物。请说明其水溶性增强的原因:______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com