
����Ŀ����ԭ�������ĵ���,���ֶ�����Ԫ��ԭ�Ӱ뾶����Դ�С��������ۻ�����۵ı仯��������ͼ��ʾ��

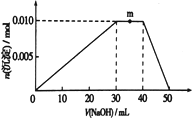
�����жϳ���Ԫ�ػش����⣺
��1��A��B��Ϊ����ij����Ԫ����ɵķ��ӣ�A�����ĸ�ԭ�Ӻ˺�10�����ӣ�B����6��ԭ�Ӻ˺�18�����ӣ���A�ķ���ʽΪ________��B�ķ���ʽΪ_________��
��2���Ƚ�e��f���ӵİ뾶��С(��Ԫ�����ӷ��ű�ʾ)__________________���ǽ�����g_____h(����ǿ��������������)����һ����ѧ����ʽ֤��������� ________��
��3������Ԫ�ؿ������R����ѧʽΪzx4f(gd4)2��,��ʢ��10mL1mol��L1R��Һ���ձ��еμ�NaOH��Һ���������ʵ�����NaOH��Һ����仯ʾ��ͼ��������ͼ��
������NaOH��Һ���ʵ�����Ũ��Ϊ_________________________��
��д��m�㷴Ӧ�����ӷ���ʽ______________________________��
������R��Һ�иļ�20mL1.1mol��L1Ba(OH)2��Һ����ַ�Ӧ����Һ�в������������ʵ���Ϊ______________mol.
���𰸡� NH3 N2H4 r(Na+)>r(Al3+) ���� H2S+Cl2===S��+2HCl 1molL1 NH4++OH-=NH3H2O 0.026.
����������x-h��Ϊ������Ԫ�أ�������״ͼ��֪��x���ڵ�һ���ڣ�y��z��d���ڵڶ����ڣ�e��f��g��h���ڵ������ڣ����ݸ�Ԫ��������ۻ�����ۿ�֪x��e������A�壬y���ڵ���A�壬z���ڵ���A�壬d��g���ڵ���A�壬f���ڵ���A�壬h���ڵ���A�壬�ɴ˿�֪xΪ�⡢yΪ̼��zΪ����dΪ����eΪ�ơ�fΪ����gΪ��hΪ�ȡ�
��1��A�����ĸ�ԭ�Ӻ˺�10�����ӣ�AΪNH3��B����6��ԭ�Ӻ˺�18�����ӣ�BΪN2H4����ȷ����NH3��N2H4��
��2��eΪ�ơ�fΪ������������Ų���ͬ�����ӣ��˵����Խ�����Ӱ뾶ԽСr(Na+)>r(Al3+)��gΪ��hΪ����ͬһ����ԭ�Ӱ뾶ԽС���ǽ�����Խǿ������g����h�����������ⷴӦ�Ʊ����������������������Դ�������Ԫ�صķǽ����Դ�����Ԫ�أ���ӦΪH2S+Cl2==S��+2HCl����ȷ����r(Na+)>r(Al3+)��������H2S+Cl2==S��+2HCl��
��3��������Ԫ�ؿ������R��ѧʽΪNH4Al(SO4)2, ��ʢ��10mL1mol��L1R��Һ���ձ��еμ�NaOH��Һ,���������Ƶμӵ�50 mLʱ��ǡ���γ�ƫ�����ƺ�һˮ�ϰ������ݷ�Ӧ��ϵ��Al3+--4OH- ��NH4+-OH-��֪����NaOH��Һ���ʵ�����Ũ��Ϊcmol/L, c��50��10-3=10mL��1��10-3��4+10mL��1��10-3, c=1mol/L����ȷ����1molL1��
����ͼ��֪0-30mL��������ӦAl3++3OH-=Al(OH)3���������������������࣬m������м����������ƣ��������ʵ������䣬��NH4+��OH-��Ӧ����NH3H2O�����ӷ���ʽΪ��NH4++OH-=NH3H2O ��40-50mL��ʹ�����������ܽ⣻��ȷ�𰸣�NH4++OH-=NH3H2O��
��20mL1.1mol��L1Ba(OH)2��Һ�ṩ�����������ӵ���Ϊ20��1.1��10-3��2=0.044 mol��10mL��1mol��L1 NH4Al(SO4)2��Һ�к���NH4+����Ϊ10mL��1��10-3=0.01 mol������Al3+����Ϊ10mL��1��10-3=0.01 mol����������笠����ӷ�Ӧ���ĵ����������ӵ���Ϊ0.01 mol��ʣ������������ӵ���Ϊ0.044 -0.01=0.034 mol�����ݷ�Ӧ��ϵ��Al3+--3OH��Al(OH)3,��֪��0.01 mol Al3+��ȫ��Ӧ�������������ӵ���Ϊ0.03 mol��������������ϵ��֪��0.004 mol������������ȫ��Ӧ����������������Ϊ0.004 mol�����ղ�����������������Ϊ0.01-0.004 =0.006 mol������������������ӷ�Ӧ���ɳ������ᱵ���ݷ�Ӧ��ϵ��Ba2+---SO42_-BaSO4 ����������ӵ���Ϊ10mL��1��10-3��2=0.02mol�������ӵ���Ϊ20��1.1��10-3=0.022 mol��������������ӽ��м������������ᱵ����0.02mol������Һ�в������������ʵ���Ϊ0.02mol+0.006 mol=0.026 mol����ȷ����0.026��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪԪ�����ڱ���ȡ�Ķ����ڵ�һ���֣�����Ԫ�ؾ�����ϡ������Ԫ�ء����й���������Ԫ�ؼ��仯�����˵������ȷ���� ( )
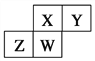
A. ԭ�Ӱ뾶��W>Z>Y>X
B. ��̬�⻯����ȶ��ԣ�Z>W>X>Y
C. W����������ϼ��븺���ϼ۵ľ���ֵһ�������
D. Z������������ˮ�������Ϊ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾװ���У�������ƿ��ʢ��ij�����壬�ձ��͵ι���ʢ��ij����Һ����ѹ�ιܵĽ�ͷ��Ȼ���ֹˮ�У�������ʵ����ʵ�������
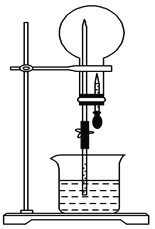
A. NH3(H2O����ɫʯ����Һ)����ɫ��Ȫ
B. SO2(NaOH��Һ)����ɫ��Ȫ
C. HCl(H2O����ɫʯ����Һ)����ɫ��Ȫ
D. NO(NaOH��Һ)����ɫ��Ȫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NaClO2��һ����Ҫ��ɱ����������Ҳ������Ư��֯��ȣ�������������ͼ1�� 
��1�����ϳɡ�������Եõ�ClO2 �� �䷴Ӧ�Ļ�ѧ����ʽΪ ��
��2������⡱��������������һ�����壬�仯ѧʽΪ ��
��3����Ӧ���ɵ�ClO2�����ڸ�Ч�ѳ������е�SO2 �� ��ClO2�ѳ�SO2ʵ��ʱSO2�ѳ�������ҺpH��ϵ��ͼ2��ʾ��pH��3��7.6֮��ʱ����pH����ClO2�����Լ����������ʽ��ͣ�����pH��7.6ʱ����pH����SO2�ѳ��������ߣ���ԭ�����Ϊ ��
��4�����ұ��涨��Ʒ���ż����Լ����ȡ�99.8%���������Լ����ȡ�99.7%����ѧ���Լ����ȡ�99.5%��Ϊ��ȷ��ij����NaClO2��Ʒ�ĵȼ����о�С����Ʋⶨ�������£�ȡ10.00g��Ʒ������������ˮ�ܽ�����Թ�����KI��Һ����ַ�Ӧ����ӦҺ������200mL��ȡ��20.00mL����ƿ������ƿ�еμ����ε�����Һ����2.00molL��1��Na2S2O3��Һ��֮��Ӧ������Na2S2O3��Һ22.00mL������Ʒ�ɴ��Լ����ȣ���д��������̣� ��֪��ClO2��+4I��+4H+�T2H2O+2I2+Cl�� �� I2+2S2O32���T2I��+S4O62�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2016��9��4�գ�G20����ٿ���������ճ��ֳ��ɾ�����ɫ���Ʋ��������ɢ����գ��������������˳����ġ�ˮ���족�� ��Ŀǰ�ҹ��������������ϵ������PM2.5��SO2��NO2��O3��CO��ָ�꣮��������Ϊ����������������Ԫ�ף����������������������Ϊ ��
��NH3����ԭ����������ת��Ϊ����Ⱦ������ĿǰӦ����㷺�����������������ѳ�������д��NH3����ԭNO2��Ӧ�Ļ�ѧ����ʽ ��
�ۼ���CO2���ŷŶ��ڻ�������������Ҫ���壮�ں���̼ѭ���У���ͨ ��ͼ3��ʾ��;����̼��д���ƻ����õ����ӷ���ʽ�� �� 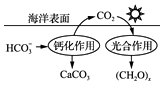
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�����֬����������ȷ���ǣ�������
A.��֬��������
B.��֬û�й̶����۷е�
C.��֬�Ǹ�֬����ĸ�����
D.��֬������ʹ��ˮ��ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ��ֻ����Na����Cl����Fe3����SO42�����������ӣ���֪ǰ�������ӵĸ�����Ϊ3��1��2������Һ��Fe3����SO42���ĸ����ȣ� ��
A. 1��2 B. 1��4 C. 3��4 D. 1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�����ڱ�����Ԫ�ص����ݼ�ͼ������˵����ȷ���ǣ� �� 
A.BiԪ�ص���������209
B.BiԪ�ص����ԭ��������209.0
C.Biԭ��6p�ܼ���һ��δ�ɶԵ���
D.Biԭ���������5��������ͬ�ĵ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com