
【题目】氯气是重要的化工原料。
(1)工业上常用_______法生产氯气,写出发生反应的化学方程式:_________________________。
(2)工业上常用石灰乳和氯气反应制取漂白粉,化学反应方程式是____________________。部分流程如右图所示,其主要设备是氯化塔,,塔从上到下分四层.将含有3%~6%水分的熟石灰从塔顶喷洒而入,氯气从塔的最底层通入,这样加科的目的是___________________________________。
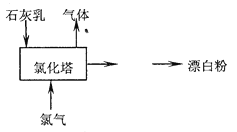
(3)某科研小组在实验室用较浓的KOH溶液直接吸收氯气,研究发现反应进行一段时间后开始出现KClO3并逐渐增多,产生KClO3的离子方程式是___________________,其原因可能是_____________________,由此可知(2)中氯化塔设计为四层是为了减少生产中类似副反应的发生。
【答案】(1)电解饱和食盐水2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
(2)Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O 增大反应物间的接触面积,使反应充分进行(3)6OH-+3Cl2=5Cl-+ClO3-+3H2O;反应放热使温度升高所致
【解析】
试题分析:(1)工业用电解饱和食盐水的方法制备氯气,电解饱和食盐水反应生成NaOH、H2、Cl2,该反应为2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑;(2)氯气通入石灰乳[Ca(OH)2]制取漂白粉,反应生成CaCl2、Ca(ClO)2、H2O,该反应为Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O,含有3%~6%水分的熟石灰从塔顶喷洒而入,氯气从塔的最底层通入时接触面积增大,使反应充分进行;(3)较浓的KOH溶液直接吸收氯气,生成KCl、KClO3、水,离子反应为6OH-+3Cl2=5Cl-+ClO3-+3H2O,发生该反应是因反应放热使温度升高所致。
2NaOH+H2↑+Cl2↑;(2)氯气通入石灰乳[Ca(OH)2]制取漂白粉,反应生成CaCl2、Ca(ClO)2、H2O,该反应为Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O,含有3%~6%水分的熟石灰从塔顶喷洒而入,氯气从塔的最底层通入时接触面积增大,使反应充分进行;(3)较浓的KOH溶液直接吸收氯气,生成KCl、KClO3、水,离子反应为6OH-+3Cl2=5Cl-+ClO3-+3H2O,发生该反应是因反应放热使温度升高所致。


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】工业上制取硝酸铵的流程图如下,请回答下列问题:

(1)在上述工业制硝酸的生产中,B设备的名称是 ______ ,其中发生反应的化学方程式为 ____________________________ 。
(2)此生产过程中,N2与H2合成NH3所用的催化剂是 ____ 。1909年化学家哈伯在实验室首次合成了氨,2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意图如下:

![]() 分别表示N2、H2、NH3 。图⑤表示生成的NH3离开催化剂表面,图②和③的含义分别是 _____ 、 ___ 。
分别表示N2、H2、NH3 。图⑤表示生成的NH3离开催化剂表面,图②和③的含义分别是 _____ 、 ___ 。
(3)在合成氨的设备(合成塔)中,设置热交换器的目的是 ;在合成硝酸的吸收塔中通入空气的目的是 。
(4)生产硝酸的过程中常会产生一些氮的氧化物,可用如下两种方法处理:
碱液吸收法:NO+NO2+2NaOH=2NaNO2+H2O
NH3还原法:8NH3+6NO2=7N2+12H2O(NO也有类似的反应)
以上两种方法中,符合绿色化学的是 ______ 。
(5)某化肥厂用NH3制备NH4NO3。已知:由NH3制NO的产率是96%、NO制HNO3的产率是92%,则制HNO3所用去的NH3的质量占总耗NH3质量(不考虑其它损耗)的 %。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质分类的说法正确的是
A.盐酸和硫酸都属于化合物 B.SO2、SiO2、CO均为酸性氧化物
C.硝酸铵和醋酸都属于弱电解质 D.淀粉和蛋白质都属于高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,浓度都是1mol/L两种气体X2和Y2,在密闭容器中反应生成气体Z ,经过t min后,测得物质的浓度为 (X2)=0.4mol/L,c(Y2)=0.8mol/L,c(Z)=0.4mol/L,则该反应的反应式可表示为( )
A.X2+2Y2=2Z B.2X2 +2Y2=2Z
C.3X2+Y2=2Z D.X2+3Y2=2Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
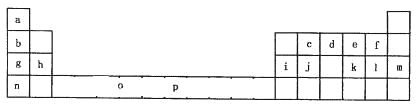
试回答下列问题:
(1)元素p为26号元素,请画出其基态原子外围电子排布图______________;
(2)e与a反应的产物的分子中中心原子的杂化形式为________________;该分子是_________(填“极性”或“非极性”)分子。
(3)上表中元素基态原子的第一电离最大的元素是__________。(用元素符号表示)
(4)o、p两元素的部分电离能数据列于下表:
元 素 | O | P | |
电离能 | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
比较两元素的I2、I3可知,气态o2+再失去一个电子比气态p2+再失去一个电子难,对此,你的解释是______________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在国际环境问题中,一次性使用的聚苯乙烯材料带来的“白色污染”甚为突出。这种材 料难以分解,处理麻烦。最近研究制出一种新型的材料能替代聚苯乙烯。它是由乳酸缩 聚而生成的,该种材料可在乳酸菌作用下发生降解,下列关于聚乳酸的说法正确的是
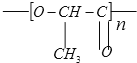
A.聚乳酸是一种纯净物
B.其聚合方式与聚苯乙烯相似
C.其单体为CH3-CH(OH)-COOH
D.聚乳酸是一种线型高分子材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:HCN(aq)与NaOH(aq)反应的△H=-12.1kJ /mol;HCl(aq)与NaOH(aq)反应的△H =-55.6kJ/ mol。则HCN在水溶液中电离的ΔH等于
A. -67.7 kJ /mol B. -43.5kJ /mol C. +43.5 kJ/ mol D. +67.7 kJ/ mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是( )
A.由 D和18O所组成的水11g,所含中子数为4NA
B.1 L 0.4 mol·L-1稀硝酸与Fe完全反应,转移电子数为0.3NA
C.标准状况下,2.24LCHCl3所含分子数为 0.1NA
D.密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com