
【题目】利用氯碱工业中的离子交换膜技术原理,可电解Na2SO4溶液生产NaOH溶液和H2SO4溶液。下列说法中正确的是
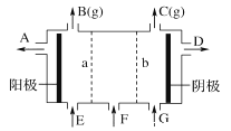
A. 阴极反应式为4OH--4e-=2H2O+O2↑
B. 从A口出来的是NaOH溶液
C. b是阳离子交换膜,允许Na+通过
D. Na2SO4溶液从G口加入
 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:
【题目】将35g锌粉与少量浓硫酸在加热条件下充分反应,共收集到混合气体11.2L(标准状况),其质量为19.6g,则剩余锌粉的质量为
A. 1.0g B. 2.0g C. 2.5g D. 3.5g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种主族元素的离子![]() 、
、![]() 、
、![]() 、
、![]() (a、b、c、d 为元素的原子序数),它们具有相同的电子层结构,若 m>n,对下列叙述的判断正确的是( )
(a、b、c、d 为元素的原子序数),它们具有相同的电子层结构,若 m>n,对下列叙述的判断正确的是( )
①a-b=n-m ②元素的原子序数 a>b>c>d ③元素非金属性 Z>R ④最高价氧化物对应水化物碱性 X>Y
A.③B.①②③④C.①②③D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,我国拥有完全自主产权的氢氧燃料电池车将在北京奥运会期间为运动员提供服务。某种氢氧燃料电池的电解液为KOH溶液,下列有关该电池的叙述不正确的是( )
A. 正极反应式为:O2+2H2O+4e-====4OH-
B. 工作一段时间后,电解液中KOH的物质的量不变
C. 该燃料电池的总反应方程式为:2H2+O2====2H2O
D. 用该电池电解CuCl2溶液,产生2.24 L Cl2(标准状况)时,有0.1 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量混合气体在密闭容器中发生如下反应![]() ;ΔH <0,达到平衡后测得A气体的浓度为0.5mol·L-1;当恒温下将密闭容器的容积扩大两倍并再次达到平衡时,测得A的浓度为0.3 mol·L-1。则下列叙述正确的是( )
;ΔH <0,达到平衡后测得A气体的浓度为0.5mol·L-1;当恒温下将密闭容器的容积扩大两倍并再次达到平衡时,测得A的浓度为0.3 mol·L-1。则下列叙述正确的是( )
A. 平衡向右移动 B. x+y>z C. B的转化率提高 D. C的体积分数增加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见气体在标准状况下的密度为1.25 g·L-1。
(1)该气体的相对分子质量为________。
(2)若该气体的分子式为A2型,其名称为________;
若该气体的分子式为AB型,其名称为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能获得成功的是 ( )
A. 用溴水可鉴别苯、乙醇、苯乙烯![]()
B. 加浓溴水,然后过滤可除去苯中少量乙烯
C. 苯、溴水、铁粉混合制成溴苯
D. 可用分液漏斗分离硝基苯和苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KIO3是一种重要的无机化合物,可作为食盐中的补碘剂。回答下列问题:
(1)KIO3的化学名称是_______。
(2)利用“KClO3氧化法”制备KIO3工艺流程如下图所示:

“酸化反应”所得产物有KH(IO3)2、Cl2和KCl。“逐Cl2”采用的方法是________。“滤液”中的溶质主要是_______。“调pH”中发生反应的化学方程式为__________。
(3)KIO3也可采用“电解法”制备,装置如图所示。
①写出电解时阴极的电极反应式______。
②电解过程中通过阳离子交换膜的离子主要为_________,其迁移方向是_____________。
③与“电解法”相比,“KClO3氧化法”的主要不足之处有______________(写出一点)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关阿伏加德罗常数NA的说法正确的是( )
A. 标准状况下,5.6 L CO2与足量Na2O2反应转移的电子数为0.5NA
B. 常温常压下,11gCO2中含有0.75NA个原子
C. 标准状况下,NA个水分子的体积约为22.4L
D. 50 mL 12 mol·L-1盐酸与足量MnO2共热,转移的电子数为0.3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com