
| A. | 电镀铜时用待镀的金属制品作阳极、铜作阴极 | |
| B. | AlCl3熔点低,电解熔融AlCl3冶炼铝更节能 | |
| C. | 电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属 | |
| D. | 氯碱工业实际是指电解饱和食盐水的工业生产 |
分析 A、电镀铜时用待镀的金属制品作阴极、铜作阳极;
B、氯化铝是共价化合物不能导电;
C、电解精炼铜,阳极上的锌和铁也会失电子生成离子,阳极泥是银、金等;
D、氯碱工业是生成烧碱和氯气的工业.
解答 解:A、电镀过程中,镀件作阴极,镀层金属作阳极,所以电镀铜时用待镀的金属制品作阴极、铜作阳极,故A错误;
B、氯化铝是共价化合物不能导电,工业上是电解熔融的氧化铝制备铝,故B错误;
C、电解精炼铜,阳极上的锌和铁也会失电子生成离子,阳极泥是银、金等,故C错误;
D、氯碱工业是生成烧碱和氯气的工业,故D正确;
故选D.
点评 本题考查了电解池、原电池原理的分析判断,电极反应和电极判断是解题关键,掌握基础是关键,题目难度中等.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源:2016-2017学年陕西省高二上月考一化学卷(解析版)) 题型:选择题
一定量的稀硫酸与足量的铝粉反应时,为了减缓反应速率,且不影响生成氢气的总量,应向稀硫酸中加入适量的
A.KOH(固体) B.CH3COOH C.KCl(固体) D.CH3COOK(固体)
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对于反应CH2=CH2(g)+H2(g)→CH3CH3(g)△H<0,若使用催化剂,反应过程中放出的热量更多 | |
| B. | CO燃烧的热化学方程式为2CO(g)+O2(g)=2CO2(g)△H=+285.8kJ/mol | |
| C. | 反应2Mg+CO2=2MgO+C△H<0从熵变角度看,不可自发进行 | |
| D. | 在密闭容器中,2HI(g)?H2(g)+I2(g)△H=+14.9kJ/mol,若投入NA个HI分子,反应平衡时,吸热7.45kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NA个Fe(OH)3胶体粒子的质量为107 g | |
| B. | 8.0 g Cu2S和CuO的混合物中含有铜原子数为0.1NA | |
| C. | 标准状况下,2.24 L Cl2溶于水中达到饱和,可得到HClO分子的数目是0.1NA | |
| D. | 1 mol Na2O2固体中含离子总数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
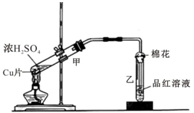 如图为浓硫酸与铜片反应的装置.请回答:
如图为浓硫酸与铜片反应的装置.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com