
【题目】化学研究小组用如图装置测定锌(含有少量铜)的纯度,下列操作能达到实验目的的是( )
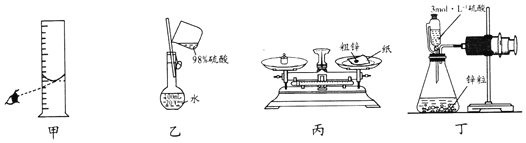
A.用装置甲量取一定体积的浓硫酸
B.用装置乙配制100mL3mo1L-1的稀硫酸
C.用装置丙称量一定质量的粗锌
D.用装置丁测量金属锌与稀硫酸反应产生氢气的体积
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
【题目】已知:N2(g)+3H2(g) ![]() 2NH3(g) △H = -92.2 kJ/mol。下列说法不正确的是
2NH3(g) △H = -92.2 kJ/mol。下列说法不正确的是
A.1 mol N2(g)和3 mol H2(g)的能量之和高于2 mol NH3 (g)的能量
B.形成2 mol NH3(g)的化学键释放的总能量大于断裂1 mol N2 (g) 和3 mol H2 (g) 的化学键所吸收的总能量
C.加入催化剂是为了加大反应速率,缩短生产周期,降低生产成本
D.将1 mol N2(g)和3 mol H2(g)充入一密闭容器中充分反应,放出92.2 kJ 的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,一定条件下,进行如下反应:NO(g)+CO(g) ![]()
![]() N2(g)+CO2(g);ΔH= -373.2kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
N2(g)+CO2(g);ΔH= -373.2kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
A.加催化剂同时升高温度B.加催化剂同时增大压强
C.升高温度同时充入N2D.降低温度同时增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有X、Y、Z和W四种元素.已知:①![]() 、Y、Z属同一短周期,其离子以
、Y、Z属同一短周期,其离子以![]() 、
、![]() 、
、![]() 的形式存在。②
的形式存在。②![]() 和Z组成化合物
和Z组成化合物![]() 溶液遇苯酚呈紫色。请回答:
溶液遇苯酚呈紫色。请回答:
(1)Z的最高价氧化物对应水化物的名称为 ______
(2)X的单质在二氧化碳中燃烧的化学方程式为 ______
(3)Y的单质可用于冶炼金属锰,写出Y与二氧化锰反应的化学方程式 ______,Y的最高价氧化物对应的水化物既可溶于强酸又可溶于强碱,请用电离平衡理论解释其原因______
(4)当有![]() W组成的单质,在加热条件下与足量水完全反应,则生成气体标准状况下的体积为 ______ L
W组成的单质,在加热条件下与足量水完全反应,则生成气体标准状况下的体积为 ______ L
(5)我国陆地上冶炼X的主要流程如图所示:
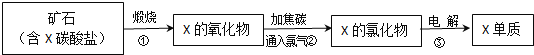 已知当有lmolX的氧化物参加反应时,有2mol电子转移且生成三种产物,则步骤②反应的化学方程式为 ______
已知当有lmolX的氧化物参加反应时,有2mol电子转移且生成三种产物,则步骤②反应的化学方程式为 ______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着我国工业化水平的不断发展,解决水、空气污染问题成为重要课题。
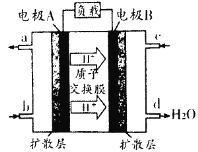
(1)汽车尾气的大量排放是造成空气污染的重要因素之一,发展燃料电池汽车可以有效地解决上述问题。直接甲醇燃料电池(DMFC)不会产生有害产物,能量转换效率比内燃机要高2~3倍,电池结构如图所示,c处通入的物质为为______,外电路中电子从______到______(填“A”或“B”)移动,写出电池负极的电极反应方程式______________
(2)工业废水中常含有一定量的Cr2O72-,会对人类及生态系统产生很大损害,电解法是处理铬污染的常用方法。该法用Fe做电极电解含Cr2O72-的酸性废水,电解时,在阴极上有大量气泡生成,并产生Cr(OH)3、Fe(OH)3沉淀。
①反应中,1molCr2O72-完全生成Cr(OH)3沉淀,外电路通过电子的物质的量为_________ mol。
②常温下,Cr(OH)3的溶度积Ksp=10-12(mol/L)4,当Cr3+浓度小于![]() mol
mol![]() 时可认为完全沉淀,电解完全后,测得溶液的pH=6,则该溶液过滤后为___________(填“能”或“否”)直接排放。
时可认为完全沉淀,电解完全后,测得溶液的pH=6,则该溶液过滤后为___________(填“能”或“否”)直接排放。
(3)含氨废水易引发水体富营养化。向NH4Cl溶液中加入少量NaOH固体,溶液中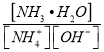 ________(填“增大”“减小”或“不变”);
________(填“增大”“减小”或“不变”);![]() 时,NH3H2O的电离平衡常数Kb=1.8×10-5mol/L,该温度下,1mol
时,NH3H2O的电离平衡常数Kb=1.8×10-5mol/L,该温度下,1mol![]() 的NH4Cl溶液中c(H+)=_______mol/L。(已知
的NH4Cl溶液中c(H+)=_______mol/L。(已知![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C12能与过量的NH3反应得到一种固体M和单质H.下列说法正确的是( )
A.M中含离子键、共价键、配位键B.NH3的电子式为![]()
C.H中σ键与π百键个数比为1:1D.NH3和Cl2都属于极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)在医药、橡胶、印染等方面应用广泛。利用SO2生产Na2S2O5的工艺如图:
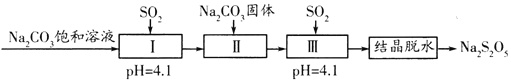
资料:Na2S2O5通常是由NaHSO3过饱和溶液经结晶脱水制得,下列说法正确的是( )
A.Na2S2O5是Na2SO3和SO2的混合物
B.pH=4.1时,I中主要反应的化学方程式为Na2CO3+SO2=Na2SO3+CO2
C.加入Na2CO3固体的目的是调节pH,促进Ⅲ中SO2的再吸收
D.“结晶脱水”过程中反应的化学方程式为2NaHSO3=Na2S2O5+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲酸香叶酯是一种食品香料,可由香叶醇与甲酸发生酯化反应制得。下列说法正确的是( )
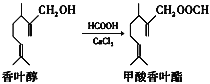
A.香叶醇的分子式为C11H18O
B.香叶醇在浓硫酸、加热条件下可发生消去反应
C.1 mol甲酸香叶酯可以与3 mol H2发生加成反应
D.甲酸香叶酯与新制的Cu(OH)2悬浊液共热可生成红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作能达到实验目的是( )
实验目的 | 实验操作 | |
A | 除去 | 向含有少量 |
B | 检验溶液中是否含有 | 取少量溶液于试管中,先加入 |
C | 比较HCl和 | 用pH试纸测定浓度均为 |
D | 验证 | 将硫酸酸化的 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com