
【题目】焦亚硫酸钠(Na2S2O5)在医药、橡胶、印染等方面应用广泛。利用SO2生产Na2S2O5的工艺如图:
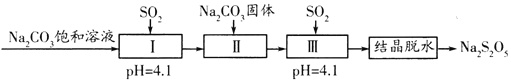
资料:Na2S2O5通常是由NaHSO3过饱和溶液经结晶脱水制得,下列说法正确的是( )
A.Na2S2O5是Na2SO3和SO2的混合物
B.pH=4.1时,I中主要反应的化学方程式为Na2CO3+SO2=Na2SO3+CO2
C.加入Na2CO3固体的目的是调节pH,促进Ⅲ中SO2的再吸收
D.“结晶脱水”过程中反应的化学方程式为2NaHSO3=Na2S2O5+H2O
【答案】CD
【解析】
由流程可知,I中发生Na2CO3+2SO2+H2O=2NaHSO3+CO2,加入Na2CO3固体,并再次充入SO2,可得到NaHSO3过饱和溶液,NaHSO3过饱和溶液经结晶脱水制得Na2S2O5。
A.Na2S2O5为纯净物,由NaHSO3过饱和溶液经结晶脱水制得,故A错误;
B.Na2SO3溶液呈碱性,①Ⅰ中反应的化学方程式为Na2CO3+2SO2+H2O=2NaHSO3+CO2,故B错误;
C.工艺中加入Na2CO3固体,并再次充入SO2的目的是调节pH,促进Ⅲ中SO2的再吸收,得到NaHSO3过饱和溶液,故C正确;
D.由题给信息可知Na2S2O5通常是由NaHSO3过饱和溶液经结晶脱水制得,则反应的化学方程式为2NaHSO3=Na2S2O5+H2O,故D正确。
故选:CD。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】肉桂酸甲酯(H)是常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。它的分子式为C10H10O2,且分子中只含有1个苯环,苯环上只有一个取代基。利用红外光谱仪可初步检测有机化合物中的某些基团,现测得H分子的红外光谱如图所示:
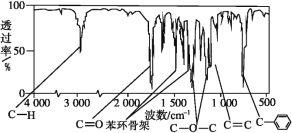
又知J为肉桂酸甲酯的一种同分异构体,其分子结构模型如图所示(图中球与球之间的连线表示单键或双键等化学键)。
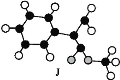
试回答下列问题:
(1)肉桂酸甲酯(H)的结构简式为___。
(2)现测出A的核磁共振氢谱图有6个峰,且面积之比为1∶2∶2∶2∶1∶2。用芳香烃A为原料合成H的路线如下(部分反应物和反应条件已略去) :
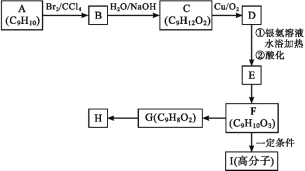
①F→G的反应类型是___。
②写出下列反应的化学方程式:F→I:___。
③F的同分异构体较多,其中有一类可用通式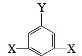 表示(其中X、Y均不为氢原子),试写出符合上述通式且能发生银镜反应的四种物质的结构简式:___。
表示(其中X、Y均不为氢原子),试写出符合上述通式且能发生银镜反应的四种物质的结构简式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列物质在水溶液中的电离方程式:
(1)H2SO4:________________________________________________;
(2)Fe(OH)3:______________________________________________;
(3)NH3·H2O:____________________________________________;
(4)Na2CO3:_______________________________________________;
(5)KHCO3:_______________________________________________。
(6)Al(OH)3的酸式电离:______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学研究小组用如图装置测定锌(含有少量铜)的纯度,下列操作能达到实验目的的是( )
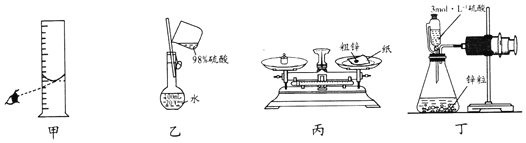
A.用装置甲量取一定体积的浓硫酸
B.用装置乙配制100mL3mo1L-1的稀硫酸
C.用装置丙称量一定质量的粗锌
D.用装置丁测量金属锌与稀硫酸反应产生氢气的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在10 L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g) ![]() M(g)+N(g),所得实验数据如下表:
M(g)+N(g),所得实验数据如下表:
实验 编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
n(X) | n(Y) | n(M) | ||
① | 700 | 0.10 | 0.40 | 0.090 |
② | 800 | 0.10 | 0.40 | 0.080 |
③ | 800 | 0.20 | 0.30 | a |
④ | 900 | 0.10 | 0.15 | b |
下列说法正确的是( )
A.根据实验①、②可以推测该反应正反应△H>0
B.实验②中,该反应的平衡常数K=2.0
C.实验③中,达到平衡时,X的转化率为60%
D.实验④中,达到平衡时,b>0.060
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂离子二次电池正极材料磷酸亚铁锂是应用广泛的正极材料之一。一种制备磷酸亚铁锂的化学方法为:C+4FePO4+2Li2CO3![]() 4LiFePO4+3CO2↑.回答下列问题:
4LiFePO4+3CO2↑.回答下列问题:
(1)Fe失去电子变成为阳离子时首先失去______轨道的电子。
(2)C、O、Li原子的第一电离能由大到小的顺序是______;PO43-的空间构型为______。
(3)C与Si同主族,CO2在高温高压下所形成的晶体结构与SiO2相似,该晶体的熔点比SiO2晶体______(填“高”或“低”)。硅酸盐和SiO2一样,都是以硅氧四面体作为基本结构单元,下图表示一种含n个硅原子的单链式多硅酸根的结构(投影如图1所示),Si原子的杂化类型为______,其化学式可表示为______。

(4)图2表示普鲁士蓝的晶体结构(![]() 个晶胞,K+未标出,每隔一个立方体在立方体体心有一个钾离子)。
个晶胞,K+未标出,每隔一个立方体在立方体体心有一个钾离子)。
①普鲁士蓝晶体中每个Fe3+周围最近且等距离的Fe2+数目为______个。
②晶体中该立方体的边长为a nm,设阿伏加德罗常数为NA,其晶体密度为______gcm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用滴定管量取一定体积的浓氯水置于锥形瓶中,用NaOH溶液以恒定速度来滴定该浓氯水,根据测定结果绘制出ClO-、ClO3-等离子的物质的量浓度c与时间t的关系曲线如下。下列说法正确的是( )
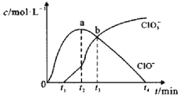
A.NaOH溶液和浓氯水可以使用同种滴定管盛装
B.a点溶液中存在如下关系:c(Na+)+c(H+)=c(ClO-)+c(ClO3-)+c(OH-)
C.b点溶液中各离子浓度:c(Na+)>c(Cl-)>c(ClO3-)=c(ClO-)
D.t2~t4,ClO-的物质的量下降的原因可能是ClO-自身歧化:2ClO-=Cl-+ClO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关仪器使用方法或实验操作正确的是![]()
A.洗净的锥形瓶和容量瓶可以放进烘箱烘干
B.酸式滴定管装标准溶液前,必须先用该溶液润洗
C.酸碱滴定实验中,用待滴定溶液润洗锥形瓶以减小实验误差
D.用容量瓶配溶液时,若加水超过刻度线,立即用滴管吸出多余液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列操作及现象,所得结论不正确的是![]()
![]()
序号 | 操作及现象 | 结论 |
A | 将 |
|
B | “ |
|
C | 向25mL冷水和沸水中分别滴入5滴 | 温度升高, |
D | 将固体 | 同温下溶解度:
|
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com