
| A. | 2个 | B. | 3个 | C. | 4个 | D. | 5个 |
分析 (1)漏掉钡离子与硫酸根离子的反应;
(2)用惰性电极电解Na2S溶液生成氢氧化钠和氢气、硫;
(3)氯气过量二价铁离子、溴离子都被氧化;
(4)三价铁离子与碳酸根离子发生双水解;
(5)二氧化硫少量,生成亚硫酸铵;
(6)电解池中,金属铜作阳极时,铜电极本身失去电子;
(7)用石墨作电极电解AlCl3溶液生成氢氧化铝、氢气和氯气;
(8)Na2O2加入到足量H218O中,过氧化钠既做氧化剂又做还原剂.
解答 解:(1)MgSO4溶液与Ba(OH)2溶液混合:Ba2++SO42-+Mg2++2OH-═Mg(OH)2↓+BaSO4↓,故错误;
(2)用惰性电极电解Na2S溶液,离子方程式:S2-+2H2O$\frac{\underline{\;通电\;}}{\;}$S↓+H2↑+2OH-,故正确;
(3)往FeBr2溶液中通入过量C12,二价铁离子、溴离子都被氧化,离子方程式:3Cl2+2Fe2++4Br-═2Fe3++6Cl-+2Br2,故错误;
(4)FeCl3溶液中撒入CaCO3粉末有气泡产生,离子方程式:2Fe3++3CaCO3+3H2O═2Fe(OH)3↓+3Ca2++3CO2↑,故正确;
(5)氨水吸收少量的二氧化硫,离子方程式:2NH3•H2O+SO2═2NH4++SO32-,故错误;
(6)电解池中,金属铜作阳极时,铜电极本身失去电子,阴极是盐酸中的氢离子放电,故电解原理方程式为Cu+2H+$\frac{\underline{\;通电\;}}{\;}$H2↑+Cu2+,故错误;
(7)用石墨作电极电解AlCl3溶液生成氢氧化铝、氢气和氯气,离子方程式:2Al3++6Cl-+6H2O$\frac{\underline{\;通电\;}}{\;}$2Al(OH)3↓+3H2↑+3Cl2↑,故错误;
(8)Na2O2加入到足量H218O中,过氧化钠既做氧化剂又做还原剂,离子方程式:2Na2O2+2H218O═4Na++418OH-+O2↑,故错误;
故选:A.
点评 本题考查了离子方程式书写,明确反应实质是解题关键,注意离子反应遵循客观事实、遵循电荷守恒规律,题目难度中等.


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
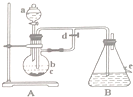 如图所示装置,可用来制取和观察Fe(OH)2在空气中被氧化的颜色变化.实验时必须使用铁屑和6mol/L的硫酸,其他试剂任选.填写下列空白:
如图所示装置,可用来制取和观察Fe(OH)2在空气中被氧化的颜色变化.实验时必须使用铁屑和6mol/L的硫酸,其他试剂任选.填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃,$\frac{{K}_{W}}{c({H}^{+})}$=0.1mol/L的溶液中:ClO-、Cl-、K+、HSO3- | |
| B. | 无色强酸性溶液中:Na+、Cl-、SO42-、[Cu(NH3)4]2+ | |
| C. | 水电离产生的c(H+)=10-13 mol•L-1的溶液中:Na+、Cl-、NO3-、SO42- | |
| D. | 加入Al能放出H2的溶液中:NH4+,SO42-,Br-,NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 足量的CO2通入氨水中:CO2+NH3•H2O═NH4++HCO3- | |
| B. | 除去CO2中的HCl气体:CO32-+2H+═CO2+2H2O | |
| C. | 自然界中溶洞的形成:CaCO3+CO2+2H2O═Ca2++2HCO3- | |
| D. | 用烧碱溶液吸收氯气的反应:Cl2+2OH-═Cl-+ClO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
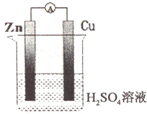
| A. | .锌作负极 | B. | 铜电极上发生氧化反应 | ||
| C. | .铜作负极 | D. | 锌电极上发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硫气体通入过氧化钠:2SO2+2Na2O2═2Na2SO3+O2↑ | |
| B. | 金属铝投入NaOH溶液中:Al+2OH-═AlO${\;}_{2}^{-}$+H2↑ | |
| C. | 硫酸亚铁与酸性高锰酸钾反应:3Fe2++MnO${\;}_{4}^{+}$+4H+=3Fe3++MnO2↓+2H2O | |
| D. | 碳酸氢钠溶液与少量石灰水反应:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ④①②③ | C. | ②①③④ | D. | ④③②① |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com