
【题目】从煤和石油中可以提炼出化工原料A和B,A是一种果实促熟剂,它的产量用来衡量一个国家的石油化工发展水平。B是一种比水轻的油状液体,B仅由碳、氢两种元素组成,碳元素与氢元素的质量比为12∶1,B的相对分子质量为78。回答下列问题:
(1)A的电子式为____________________,A的结构简式为____________________。
(2)A可以使溴的四氯化碳溶液褪色的化学反应方程式为: _________,反应类型为__________。
(3)在碘水中加入B振荡静置后的现象为___________________。
(4)B与浓硫酸和浓硝酸在50~60℃反应的化学反应方程式为: ___________,反应类型为__________。
(5)等质量的A、B完全燃烧时消耗O2的物质的量__________(填"A>B""A<B"或"A=B")。
【答案】![]() CH2=CH2 CH2=CH2+Br2→CH2BrCH2Br 加成反应 分层,下层无色,上层紫红色
CH2=CH2 CH2=CH2+Br2→CH2BrCH2Br 加成反应 分层,下层无色,上层紫红色 ![]() 取代反应(或硝化反应) A>B
取代反应(或硝化反应) A>B
【解析】
A是一种果实促熟剂,它的产量用来衡量一个国家的石油化工发展水平,则A为CH2=CH2,B是一种比水轻的油状液体,B仅由碳氢两种元素组成,碳元素与氢元素的质量比为12∶1,则原子个数之比为1∶1,B的相对分子质量为78,则12n+2n-6=78,解得n=6,所以B为苯,结合乙烯和苯的结构与性质分析解答。
(1)A为CH2=CH2,其电子式为![]() ,结构式为
,结构式为![]() ,结构简式为CH2=CH2,故答案为:
,结构简式为CH2=CH2,故答案为:![]() ;CH2=CH2;
;CH2=CH2;
(2)乙烯含有碳碳双键,能够与溴发生加成反应,使溴水褪色,反应的化学方程式为CH2=CH2+Br2→CH2BrCH2Br,故答案为:CH2=CH2+Br2→CH2BrCH2Br;加成反应;
(3)碘水中加入苯发生萃取,苯的密度比水的小,则苯在上层,上层为紫红色,水在下层,下层为无色,故答案为:分层,下层无色,上层紫红色;
(4)B与浓H2SO4与浓HNO3在50-60℃发生硝化反应,反应的化学反应方程![]() ,属于取代反应(或硝化反应),故答案为:
,属于取代反应(或硝化反应),故答案为:![]() ;取代反应(或硝化反应);
;取代反应(或硝化反应);
(5)设A、B的质量都为mg,由CxHy消耗x+![]() 氧气,可知等质量的A、B完全燃烧时消耗O2的物质的量分别为
氧气,可知等质量的A、B完全燃烧时消耗O2的物质的量分别为![]() ×(2+
×(2+![]() )=
)=![]() mol和
mol和![]() ×(6+
×(6+![]() )=
)=![]() mol,所以等质量的A、B完全燃烧时消耗O2的物质的量A>B,故答案为:A>B。
mol,所以等质量的A、B完全燃烧时消耗O2的物质的量A>B,故答案为:A>B。


科目:高中化学 来源: 题型:
【题目】配制250mL 0.5mol/L NaOH溶液,在下列仪器中:A. 托盘天平 B. 量筒 C.烧杯 D. 玻璃棒 E. 漏斗 F. 500mL容量瓶 G. 药匙 H. 250mL容量瓶 I. 胶头滴管 J. 坩埚。需要用到的仪器有______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如下能量关系示意图,下列说法正确的是
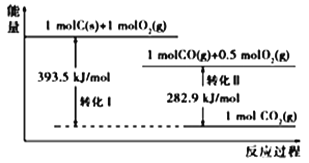
A. 1 molC(g)与1 mol O2(g)的能量之和为393.5 kJ
B. 反应2CO(g)+O2(g) ===2CO2(g)中,生成物的总能量大于反应物的总能量
C. 由C→CO的热化学方程式为:2C(s)+O2(g) ===2CO(g) ΔH= 221.2 kJmol1
D. CO的燃烧热ΔH=+282.9 kJmol1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2NO2(红棕色)![]() N2O4(无色),分别进行如下两个实验:
N2O4(无色),分别进行如下两个实验:
实验ⅰ:将NO2球分别浸泡在热水和冰水中,现象如图1。
实验ⅱ:将一定量的NO2充入注射器中后封口,测定改变注射器体积的过程中气体透光率随时间的变化(气体颜色越深,透光率越小),如图2。下列说法不正确的是
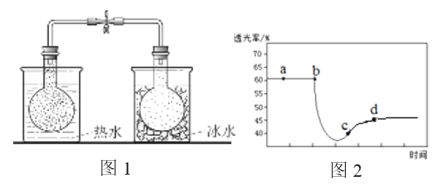
A. 图1现象说明该反应为放热反应
B. 图2中b点的操作是压缩注射器
C. c点:v(正)>v(逆)
D. 若没有能量损失,考查体系温度变化,则T(d)<T(c)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铬是人体必需元素,如含量不足会影响糖类和脂类的代谢,过高则会引起急性中毒。工业上往往采取下列循环工艺防止铬的污染:
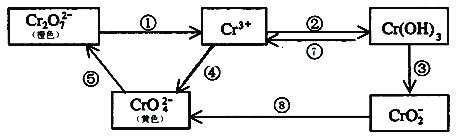
完成下列填空:
(1)①步中含Cr2O![]() 离子的废水在酸性条件下能用Fe3O4处理,反应的离子方程式为_____________;
离子的废水在酸性条件下能用Fe3O4处理,反应的离子方程式为_____________;
(2)反应⑤是可逆反应,在Na2CrO4溶液中加入稀硫酸,溶液由黄色逐渐变成橙色,写出该反应的离子方程式:___________________________________;
(3)向上述反应后的溶液中加入碱溶液,让废水的pH升至8~10,控制适当的温度,使产物中的金属阳离子全部转变为沉淀。回收所得的Cr(OH)3,经处理后又可转变成K2Cr2O7。纯净的K2Cr2O7常用于准确测定Na2S2O3溶液的物质的量浓度,方法如下:
①Cr2O72-+6I-+14H+ =3I2+2Cr3++7H2O
②2S2O32-+ I2 =S4O62-+2I-,准确称取纯净的K2Cr2O7 0.294g配成溶液,加足量KI,用Na2S2O3溶液滴定,消耗Na2S2O3溶液25.00mL。
①回收所得的Cr(OH)3在处理之前需要先进行洗涤,洗涤沉淀的方法为________________________;
②滴定时加入的指示剂通常为_________,滴定至终点的现象是_______________________________;
③Na2S2O3溶液的物质的量浓度为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的氧化物是大气污染物之一,用活性炭或一氧化碳还原氮氧化物,可防止空气污染。回答下列问题:
已知:2C(s)+O2(g)=2CO(g) ΔH=- 221 kJ/mol
C(s)+O2(g)=CO2(g) △H=- 393.5 kJ/mol
N2(g)+O2(g)=2NO(g) ΔH= +181 kJ/mol
(1)若某反应的平衡常数表达式为K=![]() ,请写出此反应的热化学方程式:___________________________;下列措施能够增大此反应中NO的转化率的是(填字母代号)_________。
,请写出此反应的热化学方程式:___________________________;下列措施能够增大此反应中NO的转化率的是(填字母代号)_________。
a.增大容器压强 b.升高温度 c.使用优质催化剂 d.增大CO的浓度
(2)向容积为2L的密闭容器中加入活性炭(足量)和NO,发生反应C(s)+2NO(g)![]() N2(g)+CO2(g),NO和N2的物质的量变化如下表所示。
N2(g)+CO2(g),NO和N2的物质的量变化如下表所示。
物质的量/mol | T1/℃ | T2/℃ | |||||
0 | 5 min | 10 min | 15 min | 20 min | 15 min | 30 min | |
NO | 2.0 | 1.16 | 0.80 | 0.80 | 0.50 | 0.40 | 0.40 |
N2 | 0 | 0.42 | 0.60 | 0.60 | 0.75 | 0.80 | 0.80 |
①0~5min内,以CO2表示的该反应速率v(CO2)=_____,该条件下的平衡常数K=__________。
②第15 min后,温度调整到T2,数据变化如上表所示,则T1_______ T2(填“>”、“<”或“=”)。
③若30min时,保持T2不变,向该容器中再加入该四种反应混合物各2 mol,则此时反应_______移动(填“正向”、“逆向”或“不”);最终达平衡时NO的转化率a=______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如图所示,U形管的左端被水和胶塞封闭有甲烷和氯气(体积比为1∶4)的混合气体,假定氯气在水中的溶解度可以忽略。将封闭有甲烷和氯气混合气体的装置放置在有光亮的地方,让混合气体缓慢地反应一段时间。
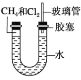
①假设甲烷与氯气反应充分,且只产生一种有机物,请写出化学方程式:_________________;
②若题目中甲烷与氯气的体积之比为1∶1,则得到的产物为____(填字母编号);
A.CH3Cl HCl B.CCl4 HCl C.CH3Cl CH2Cl2 D.CH3Cl CH2Cl2 CHCl3 CCl4 HCl
③经过几个小时的反应后,U形管右端的水柱变化是________ (填字母编号);
A.升高B.降低 C.不变D.无法确定
④若水中含有Na2SiO3,则在U形管左端会观察到__________________________________________;
⑤右端玻璃管的作用是_______________________。
(2)某实验小组用下列装置进行乙醇催化氧化的实验。
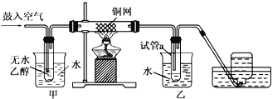
①实验过程中铜网出现红色和黑色交替出现的现象,请写出相应的化学方程式___________________、______________________ ;
②甲和乙两个装置的作用不相同,甲的作用是_____________;乙的作用是 _____________;
③反应进行一段时间后,干燥试管a中能收集到不同的物质,它们是______________________;集气瓶收集到的气体的主要成分是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.如图A、B、C是实验室常见的几种气体发生装置:
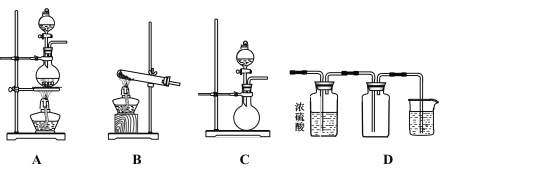
(1)实验室如果用B装置制备氨气,其化学方程式是_________________________________。
(2)气体的性质是选择气体收集方法的主要依据。下列性质与收集方法无关的是_______(填序号,下同)。
①密度 ②颜色 ③溶解性 ④热稳定性 ⑤与氧气反应
(3)若用A装置与D装置相连制备并收集X气体,则X可以是下列气体中的___________。
①CO2 ②NO ③Cl2 ④H2
其中在D装置中连接小烧杯的目的是________________________________。
Ⅱ.海洋是一个巨大的资源宝库,从海水中可制得食盐等多种产品并加以利用。下图所示以食盐为原料进行生产并综合利用的某些过程。

(1)除去粗盐中的Ca2+、Mg2+和SO42-离子,加入下列沉淀剂
① Na2CO3 ② NaOH ③ BaCl2
沉淀剂加入顺序正确的是____________
A.③①② B.③②① C.②③① D.②①③
(2)将滤液的pH调至酸性除去的离子是____________________________________。
(3)若向分离出NaHCO3晶体后的母液中加入过量生石灰,则可获得一种可以循环使用的物质,其化学式是____________。
(4)纯碱在生产、生活中有广泛的应用。
①由碳酸氢钠晶体制纯碱的化学方程式是____________________________________。
②纯碱可用于除灶台油污。其原因是(用离子方程式和简要文字表述)________________。
③工业上,可以用纯碱代替烧碱生产某些化工产品。如用饱和纯碱溶液与Cl2反应制取有效成分为NaClO的消毒液,其反应的离子方程式是____________。(已知碳酸的酸性强于次氯酸)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】采用N2O5为硝化剂是一种新型的绿色硝化技术,在含能材料、医药等工业中得到广泛应用。回答下列问题
(1)1840年 Devil用干燥的氯气通过干燥的硝酸银,得到N2O5。该反应的氧化产物是一种气体,其分子式为___________。
(2)F. Daniels等曾利用测压法在刚性反应器中研究了25℃时N2O5(g)分解反应:
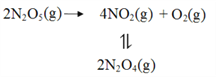
其中NO2二聚为N2O4的反应可以迅速达到平衡。体系的总压强p随时间t的变化如下表所示(t=∞时,N2O5(g)完全分解):
t/min | 0 | 40 | 80 | 160 | 260 | 1300 | 1700 | ∞ |
p/kPa | 35.8 | 40.3 | 42.5. | 45.9 | 49.2 | 61.2 | 62.3 | 63.1 |
①已知:2N2O5(g)=2N2O4(g)+O2(g) ΔH1=4.4 kJ·mol1 ,2NO2(g)=N2O4(g) ΔH 2=55.3 kJ·mol1,则反应N2O5(g)=2NO2(g)+1/2O2(g)的ΔH =_______ kJ·mol1。
②研究表明,N2O5(g)分解的反应速率v=2×10-3×P(N2O5)(KPa/min)。t=62 min时,测得体系中P(O2)=2.9 kPa,则此时的P(N2O5)=________ kPa,v=_______kPa·min1。
③若提高反应温度至35℃,则N2O5(g)完全分解后体系压强p∞(35℃)____63.1 kPa(填“大于”“等于”或“小于”)。
④25℃时N2O4(g)![]() 2NO2(g)反应的平衡常数Kp=_______kPa(Kp为以分压表示的平衡常数,计算结果保留1位小数)。
2NO2(g)反应的平衡常数Kp=_______kPa(Kp为以分压表示的平衡常数,计算结果保留1位小数)。
(3)对于反应2N2O5(g)→4NO2(g)+O2(g),R.A.Ogg提出如下反应历程:
第一步 N2O5![]() NO2+NO3 快速平衡
NO2+NO3 快速平衡
第二步 NO2+NO3→NO+NO2+O2 慢反应
第三步 NO+NO3→2NO2 快反应
其中可近似认为第二步反应不影响第一步的平衡。下列表述正确的是_______(填标号)。
A.v(第一步的逆反应)>v(第二步反应) B.反应的中间产物只有NO3
C.第二步中NO2与NO3的碰撞仅部分有效 D.第三步反应活化能较高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com