
【题目】下列有关化学用语表示正确的是( )
A. 水分子的比例模型![]()
B. 过氧化氢的电子式为:![]()
C. 石油的分馏和煤的气化、液化均为物理变化
D. 甲基环丁烷二氯代物的同分异构体的数目是10种(不考虑立体异构)
科目:高中化学 来源: 题型:
【题目】某100mL溶液可能含有Na+、NH4+、Fe3+、CO32-、SO42-、Cl-中的若干种,取该溶液进行连续实验,实验过程如下:(所加试剂均过量,气体全部逸出)
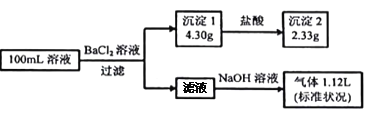
下列说法不正确的是
A. 原溶液一定存在CO32-和SO42-,一定不存在Fe3+
B. 若原溶液中不存在Na+,则c(Cl-)<0.1mol·L-1
C. 原溶液中c(Cl-)≥0.1mol·L-1
D. 原溶液一定存在Cl-,可能存在Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在一恒容密闭容器中,能表示反应 X(g)+2Y(g)![]() 2Z(g) 一定达到化学平衡状态的是
2Z(g) 一定达到化学平衡状态的是
①容器中气体的密度不再发生变化
②X、Y、Z的浓度不再发生变化
③容器中的压强不再发生变化
④单位时间内生成2n mol Z,同时消耗2n mol Y
A. ①② B. ②③ C. ③④ D. ①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图所示,关于该物质的叙述错误的是( )
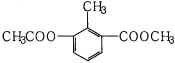
A.一个分子中含有12个H原子
B.苯环上的一氯代物有2种
C.能使酸性KMnO4溶液褪色
D.1mol该物质分别与足量H2、NaOH溶液反应,消耗其物质的量均为3mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:HCN(aq)+ NaOH(aq) ==NaCN(aq)+H2O(l) ΔH=-12.1 kJ·mol-1;
HCl(aq)+NaOH(aq) ==NaCl (aq)+H2O(l) ΔH=-55.6 kJ·mol-1
则HCN在水溶液中电离的ΔH等于
A.+43.5 kJ·mol-1 B .+67.7 kJ·mol-1
C.-43.5 kJ·mol-1 D.-67.7 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将15.2 g 铜和镁组成的混合物加入250 mL4.0molL-1的稀硝酸中,固体完全溶解,生成的气体只有NO。向所得溶液中加入1.0L NaOH溶液,此时金属离子恰好沉淀完全,沉淀质量为25.4 g,下列说法正确的是
A.原固体混合物中,Cu和Mg的物质的量之比为1:2
B.氢氧化钠溶液的浓度为0.8 mol·L-1
C.固体溶解后的溶液中硝酸的物质的量为0.1mol
D.生成的NO气体在标况下的体积为2.24 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,N4分子结构与白磷分子相似,呈正四面体结构。已知断裂1molN—N键吸收193 kJ热量,断裂1molN≡N键吸收941 kJ热量,则1mol N4气体转化为N2时要__________填“吸收”或“放出”)热量________________ kJ。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】富硼渣中含有镁硼酸盐(2MgO·B2O3)、镁硅酸盐(2MgO·SiO2)及少量Al2O3、FeO等杂质。由富硼渣湿法制备硫酸镁晶体和硼酸(H3BO3)晶体的一种工艺流程如下:

已知:生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1mol/L)
Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 | |
开始沉淀时 | 1.9 | 3.4 | 7.0 | 9.1 |
完全沉淀时 | 3.2 | 4.7 | 9.0 | 11.1 |
(1)上述流程中能加快反应速率的措施有_____、_____等。
(2)酸浸时发生反应
2MgO·SiO2 +2H2SO4=2MgSO4+SiO2+2H2O,
2MgO·B2O3+2H2SO4+H2O=2H3BO3+2MgSO4。
①上述反应体现出酸性强弱:H2SO4______H3BO3(填“>”或“<”)。
②酸浸时,富硼渣中所含Al2O3和FeO也同时溶解,写出相关反应的离子方程式:___________、____________。
③已知硼酸与过量NaOH溶液发生的中和反应为:H3BO3+OH- =B(OH)4-。下列关于硼酸的说法正确的是_____。
a.硼酸的电离方程式可表示为:H3BO3 + H2O![]() B(OH)4-+H+
B(OH)4-+H+
b.硼酸是一元弱酸
c.向NaHCO3固体中滴加饱和硼酸溶液,有气泡产生
(3)检验浸出液中的杂质离子
取少量浸出液,______(填操作和现象),证明溶液中含有Fe2+。
(4)除去浸出液中的杂质离子
用MgO调节溶液的pH至____以上,使杂质离子转化为______(填化学式)沉淀,过滤。
(5)获取晶体
ⅰ.浓缩滤液,使MgSO4和H3BO3接近饱和;
ⅱ.控制温度使两种晶体分别从溶液中结晶。结合下图溶解度曲线,简述ⅱ的方法:将浓缩液加入到高压釜(高压环境可保证在高温条件下水为液态)中,__________(将方法补充完整)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a、b、c、d、e五种短周期元素的原子半径和最外层电子数之间的关系如图所示。下列说法正确的是( )

A. 简单离子半径:b>e
B. 常温常压下,a与c形成的化合物可能呈固态
C. 单质沸点:c<d
D. d与e不能存在于同一离子化合物中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com