
【题目】金属镍及其化合物在合金材料以及催化剂等方面应用广泛。请回答下列问题:
(1)Ni原子的核外电子排布式为________
(2)NiO、FeO的晶体结构类型均与氯化钠的相同、Fe2+和Ni2+的离子半径分别78pm和69pm,则熔点FeO________ (填“<”或“>”) NiO;
(3)[Ni(NH3)6]SO4中阴离子的立体构型是_____。氨的沸点____(填“高于”或“低于”)膦(PH3),原因是_________;
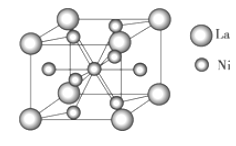
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如图所示。该合金的化学式为________;
(5)某镍白铜合金的立方晶胞结构如图所示。
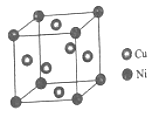
①晶胞中镍原子的堆积模型名称是_____。
②元素铜与镍的第二电离能分别为:ICu=1959kJ/mol,INi=1753kJ/mol,ICu>INi的原因是______
③若合金的密度为dg/cm3,晶胞参数(即边长)a =________nm
【答案】1s22s22p63s23p63d84s2或[Ar]3d84s2 < 正四面体 高于 NH3分子间可形成氢键 LaNi5 简单立方 铜失去的是全充满的3d10电子,镍失去的是4s1电子,所以ICu>INi ![]() ×107
×107
【解析】
(1)Ni原子的质子数是28,所以根据构造原理可知,Ni的基态电子排布式为1s22s22p63s23p63d84s2或[Ar]3d84s2;
(2)NiO、FeO的晶体结构类型均与氯化钠的相同,因此都是离子晶体。由于Ni2+和Fe2+的离子半径分别为69 pm和78 pm,所以NiO中晶格能强于FeO中晶格能,所以熔点FeO< NiO;
(3)[Ni(NH3)6]SO4中阴离子为SO42-,中心原子S的价层电子对数=4+![]() =4且不含孤电子对,根据价层电子对互斥理论,硫酸根离子的立体构型为正四面体;含有分子间氢键的氢化物熔沸点较高,氨气分子间含有氢键、膦(PH3)分子间没有氢键,则氨的熔沸点高于膦(PH3);
=4且不含孤电子对,根据价层电子对互斥理论,硫酸根离子的立体构型为正四面体;含有分子间氢键的氢化物熔沸点较高,氨气分子间含有氢键、膦(PH3)分子间没有氢键,则氨的熔沸点高于膦(PH3);
(4)由“均摊法”知每个晶胞中含有:一个La(8×![]() =1)、五个Ni(1+8×
=1)、五个Ni(1+8×![]() =5),故该合金的化学式为:LaNi5;
=5),故该合金的化学式为:LaNi5;
(5)①该晶胞中Ni原子个数=8×![]() =1、Cu原子个数=6×
=1、Cu原子个数=6×![]() =3,则Cu、Ni原子个数之比为3:1,晶胞中镍原子的堆积模型名称是简单立方;
=3,则Cu、Ni原子个数之比为3:1,晶胞中镍原子的堆积模型名称是简单立方;
②元素铜与镍的第二电离能分别为:ICu=1959kJ/mol,INi=1753kJ/mol,ICu>INi的原因是铜失去的是全充满的3d10电子,镍失去的是4s1电子,所以ICu>INi;
③该晶胞的化学式为Cu3Ni,若合金的密度为dg/cm3,晶胞参数=![]() =
=![]() cm=
cm=![]() ×107nm。
×107nm。


 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:高中化学 来源: 题型:
【题目】酸雨的主要成分是H2SO4,以下是形成途径之一:①NO2+SO2=NO+SO3,②2NO+O2=2NO2,③SO3+H2O=H2SO4,以下叙述错误的是
A. NO2由反应N2+2O2![]() 2NO2生成
2NO2生成
B. 总反应可表示为2SO2+O2+2H2O![]() 2H2SO4
2H2SO4
C. 还可能发生的反应有4NO2+O2+2H2O=4HNO3
D. 还可能发生的反应有4NO+3O2+2H2O=4HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的铜粉加入到100 mL某浓度的稀硝酸中充分反应后,容器中剩有m1 g铜粉,此时共收集到NO气体224 mL(标准状况),然后向上述混合物中加入足量稀硫酸至不再反应为止,容器剩有铜粉m2 g, 则(m1-m2)为
A.5.76B.2.88C.1.92D.0.28
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着大气污染的日趋严重,国家拟于“十二”五期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%。目前,消除大气污染有多种方法。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g) =4NO(g) + CO2(g) +2H2O(g) ⊿H= -574 kJ·mol-1
②CH4(g) +4NO(g) =2N2(g) + CO2(g) + 2H2O(g) ⊿H= -1160 kJ·mol-1
③H2O(g) = H2O(l) △H= -44.0 kJ·mol-1
写出CH4(g)与NO2(g)反应生成N2(g),CO2(g)和H2O(1)的热化学方程式________。
(2)利用Fe2+、Fe3+的催化作用,常温下可将SO2转化为SO42-,从而实现对SO2的治理。已知含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2++ O2+ 4H+= 4Fe3++ 2H2O,则另一反应的离子方程式为________。
(3)用活性炭还原法处理氮氧化物。有关反应为:C(s)+2NO(g)![]() N2(g)+CO2(g) 。某研究小组向密闭的真空容器中(假设容器体积不变,固体试样体积忽略不计)加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
N2(g)+CO2(g) 。某研究小组向密闭的真空容器中(假设容器体积不变,固体试样体积忽略不计)加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
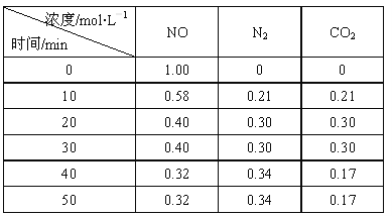
①10min~20min以v(CO2) 表示的平均反应速率为________。
②根据表中数据,计算T1℃时该反应的平衡常数为________ (保留两位小数)。
③一定温度下,随着NO的起始浓度增大,则NO的平衡转化率________ (填“增大”、“不变”或“减小”) 。
④下列各项能作为判断该反应达到平衡的是___(填序号字母)。
A.容器内压强保持不变
B.2v正(NO) =v逆(N2)
C.容器内CO2的体积分数不变
D.混合气体的密度保持不变
⑤30min末改变某一条件,过一段时间反应重新达到平衡,则改变的条件可能是________。请在下图中画出30min至40min的变化曲线________。
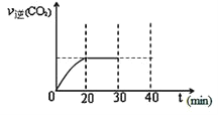
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种激光染料,应用于可调谐染料激光器,它由C、H、O三种元素组成,分子球棍模型如图所示,下列有关叙述正确的是( )
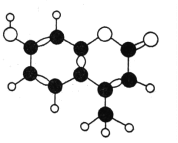
①分子式为C10H9O3 ②不能溶于水 ③1mol该物质最多能与4molH2加成 ④能使酸性KMnO4溶液褪色 ⑤1mol该物质最多能与含2mol NaOH的溶液反应
A. ①②③B. ③④⑤C. ②③④D. ②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】扁桃酸衍生物是重要的医药中间体。以A和B为原料合成扁桃酸衍生物F的路线如下:
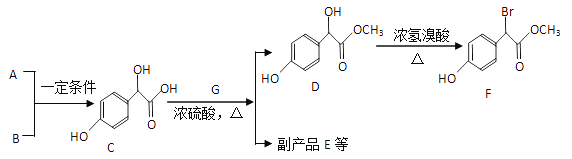
(1) A的分子式为C2H2O3,可发生银镜反应,且具有酸性,写出A+B→C的化学反应方程式:________
(2)C(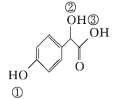 )中①、②、③3个—OH的酸性由强到弱的顺序是______
)中①、②、③3个—OH的酸性由强到弱的顺序是______
(3)E是由2分子C生成的含有3个六元环的化合物,E分子中不同化学环境的氢原子有____种
(4)D→F的反应类型是________,1 mol F在一定条件下与足量NaOH溶液反应,最多消耗NaOH的物质的量为____mol,写出符合下列条件的F的同分异构体2种(不考虑立体异构)的结构简式:_____
①属于一元酸类化合物
②苯环上只有2个取代基且处于对位,其中一个是羟基
(5)已知:
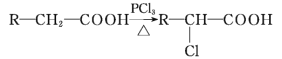
A有多种合成方法,在方框中写出由乙酸合成A的路线流程图(其他原料任选) ______________(合成路线流程图示例如下:
H2C![]() CH2
CH2![]() CH3CH2OH
CH3CH2OH![]() CH3COOC2H5
CH3COOC2H5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人工肾脏可用电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图,下列有关说法不正确的是( )
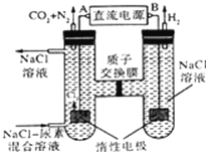
A.B为电源的正极
B.电解结束后,阴极室溶液的pH与电解前相比将升高
C.电子移动的方向是B→右侧惰性电极,左侧惰性电极→A
D.阳极室中发生的反应依次为2Cl﹣﹣2e﹣=Cl2↑、CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今年是门捷列夫发现元素周期律150周年。下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法错误的是

A. 原子半径:W<X
B. 常温常压下,Y单质为固态
C. 气态氢化物热稳定性:Z<W
D. X的最高价氧化物的水化物是强碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g)![]() 2SO3(g)ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
2SO3(g)ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
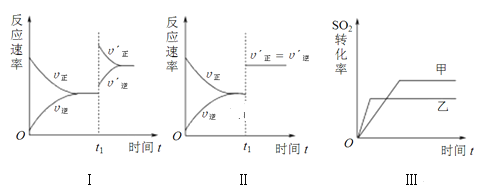
A. 图Ⅰ研究的是t1时刻增大O2的物质的量浓度对反应速率的影响
B. 图Ⅱ研究的是t1时刻通入氦气增大体系压强对反应速率的影响
C. 图Ⅲ研究的是催化剂对化学平衡的影响,且甲的催化效率比乙高
D. 图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com