
【题目】某种激光染料,应用于可调谐染料激光器,它由C、H、O三种元素组成,分子球棍模型如图所示,下列有关叙述正确的是( )
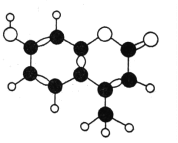
①分子式为C10H9O3 ②不能溶于水 ③1mol该物质最多能与4molH2加成 ④能使酸性KMnO4溶液褪色 ⑤1mol该物质最多能与含2mol NaOH的溶液反应
A. ①②③B. ③④⑤C. ②③④D. ②③④⑤
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
【题目】碳酸镁晶须是一种新型的吸波隐形材料中的增强材料。
(1)合成该物质的步骤如下:
步骤1:配制0.5mol·L-1MgSO4溶液和0.5mol·L-1NH4HCO3溶液。
步骤2:用量筒量取500mL NH4HCO3溶液于1000mL四口烧瓶中,开启搅拌器。温度控制在50℃。
步骤3:将250mL MgSO4溶液逐滴加入NH4HCO3溶液中,1min内滴加完后,用氨水调节溶液pH到9.5。
步骤4:放置1h后,过滤,洗涤。
步骤5:在40℃的真空干燥箱中干燥10h,得碳酸镁晶须产品(MgCO3·nH2O n=1~5)。
①步骤2控制温度在50℃,较好的加热方法是__________。
②步骤3生成MgCO3·nH2O沉淀的离子方程式为________。
③步骤4检验是否洗涤干净的方法是___________。
(2)测定合成的MgCO3·nH2O中的n值。
称量1.000g碳酸镁晶须,放入如图所示的广口瓶中加入水滴入稀硫酸与晶须反应,生成的CO2被NaOH溶液吸收,在室温下反应4~5h,反应后期将温度升到30℃,最后的烧杯中的溶液用已知浓度的盐酸滴定,测得CO2的总量;重复上述操作2次。

①图中气球的作用是___________。
②上述反应后期要升温到30℃,主要目的是_________。
③设3次实验测得每1.000g碳酸镁晶须产生的CO2平均值为a mol,则n值为______(用含a的表达式表示)。
(3)称取100g上述晶须产品进行热重分析,热重曲线如图。

则该条件下合成的晶须中,n=______(选填:1、2、3、4、5)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氨水的叙述中,正确的是
A.氨水能导电,故NH3是电解质
B.氨水中除水外物质的量浓度最大的粒子是NH3
C.氨水显弱碱性,是因为氨水是一种弱碱
D.在1mol/L的氨水中,NH3H2O、NH3、NH![]() 的物质的量浓度之和为1mol/L
的物质的量浓度之和为1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中,下列分析错误的是( )
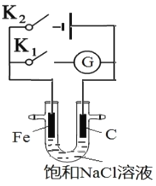
A.闭合K1构成原电池,闭合K2构成电解池
B.K1闭合,铁棒上发生的反应为:Fe﹣2e﹣═Fe2+
C.K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法
D.K1闭合,石墨棒周围溶液pH逐渐升高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】VIA族的氧,硫,硒(Se),碲(Te)等元素在化合物中常表现出多种氧化态,含VIA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)S单质的常见形式为S8,其环状结构如下图所示,S原子采用的轨道杂化方式是______。
![]()
(2)Se原子序数为______,其核外M层电子的排布式为______。
(3)H2Se的酸性比H2S__________(填“强”或“弱”)。气态SeO3分子的立体构型为______,SO32-离子的立体构型为______。
(4)H2SeO3的K1和K2分别为2.7×10-3和2.5×10-8,H2SeO4第一步几乎完全电离,K2为1.2×10-2,请根据结构与性质的关系解释:
①H2SeO3和H2SeO4第一步电离程度大于第二步电离的原因:__________。
②H2SeO4比H2SeO3酸性强的原因:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属镍及其化合物在合金材料以及催化剂等方面应用广泛。请回答下列问题:
(1)Ni原子的核外电子排布式为________
(2)NiO、FeO的晶体结构类型均与氯化钠的相同、Fe2+和Ni2+的离子半径分别78pm和69pm,则熔点FeO________ (填“<”或“>”) NiO;
(3)[Ni(NH3)6]SO4中阴离子的立体构型是_____。氨的沸点____(填“高于”或“低于”)膦(PH3),原因是_________;
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如图所示。该合金的化学式为________;
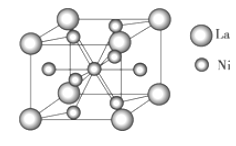
(5)某镍白铜合金的立方晶胞结构如图所示。
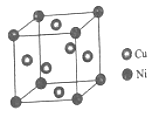
①晶胞中镍原子的堆积模型名称是_____。
②元素铜与镍的第二电离能分别为:ICu=1959kJ/mol,INi=1753kJ/mol,ICu>INi的原因是______
③若合金的密度为dg/cm3,晶胞参数(即边长)a =________nm
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室所用少量氯气是用下列方法制取的:4HCl(浓)+MnO2![]() Cl2↑+MnCl2+2H2O,试回答下列问题:
Cl2↑+MnCl2+2H2O,试回答下列问题:
(1)该反应中氧化剂与还原剂的物质的量比为:__。
(2)写出该反应的离子方程式:___。
(3)当有0.2mol电子转移时,生成标准状况下Cl2的体积是___L。
(4)若用足量二氧化锰与50ml36.5%1.2g/ml浓盐酸反应,制得的Cl2在标准状况下总小于3.36L,原因可能是①__,②__。
(5)检验氯气是否收集满的方法是用___试纸靠近集气瓶口,若试纸变蓝证明氯气已收集满。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100mL FeI2溶液中逐渐通入Cl2(溶液体积变化忽略不计),生成I2、Fe3+的物质的量随通入Cl2的物质的量的变化如图所示,下列说法错误的是( )
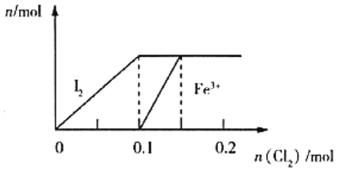
A.还原性强弱:Fe2+<I-
B.n(Cl2)=0.05mol时,溶液中I-的物质的量浓度为0.1mol·L-1
C.若n(Cl2):n(FeI2)=6:5,反应的离子方程式为2Fe2++10I-+6Cl2=5I2+2Fe3++12Cl-
D.n(Cl2)=0.12mol时,溶液中的离子主要有Fe3+、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲用NaOH固体配制1.0 mol·L1的NaOH溶液240 mL:
(1)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④倒转摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却
其正确的操作顺序为________________。本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、胶头滴管、还有________。
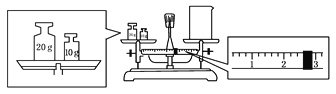
(2)某同学欲称量一定量的NaOH固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图。烧杯的实际质量为____________ g,要完成本实验该同学应称出____________ g NaOH。
(3)使用容量瓶前必须进行的一步操作是________。
(4)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏高的是________。
①没有洗涤烧杯和玻璃棒
②转移溶液时不慎有少量洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤未冷却到室温就将溶液转移到容量瓶并定容
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com