
【题目】实验室所用少量氯气是用下列方法制取的:4HCl(浓)+MnO2![]() Cl2↑+MnCl2+2H2O,试回答下列问题:
Cl2↑+MnCl2+2H2O,试回答下列问题:
(1)该反应中氧化剂与还原剂的物质的量比为:__。
(2)写出该反应的离子方程式:___。
(3)当有0.2mol电子转移时,生成标准状况下Cl2的体积是___L。
(4)若用足量二氧化锰与50ml36.5%1.2g/ml浓盐酸反应,制得的Cl2在标准状况下总小于3.36L,原因可能是①__,②__。
(5)检验氯气是否收集满的方法是用___试纸靠近集气瓶口,若试纸变蓝证明氯气已收集满。
【答案】1:2 4H++2Cl-+MnO2![]() Cl2↑+Mn2++2H2O 2.24 HCl挥发 浓盐酸随反应进行变为稀盐酸,不再与MnO2反应 湿润的淀粉碘化钾
Cl2↑+Mn2++2H2O 2.24 HCl挥发 浓盐酸随反应进行变为稀盐酸,不再与MnO2反应 湿润的淀粉碘化钾
【解析】
该反应中,锰元素化合价降低,MnO2是氧化剂,氯元素化合价升高,HCl是还原剂,当4mol HCl 参加反应时,只有2mol氯元素从-1价升高为0价,被氧化;由于浓盐酸易挥发,且只有浓盐酸与二氧化锰反应,反应过程中浓盐酸会逐渐变稀,稀到一定程度反应不再进行;氯气可从碘化钾中置换出碘,碘遇淀粉变蓝色,据此分析解答。
(1)该反应中,锰元素化合价降低,MnO2是氧化剂,氯元素化合价升高,HCl是还原剂,当4mol HCl 参加反应时,只有2mol氯元素从-1价升高为0价,被氧化,即只有2mol HCl 起到还原剂的作用,因此,该反应中氧化剂与还原剂的物质的量比为1:2;
(2)该反应的离子方程式:4H++2Cl-+MnO2![]() Cl2↑+Mn2++2H2O;
Cl2↑+Mn2++2H2O;
(3)氯元素从-1价升高为0价,每生成1mol Cl2,转移2mol电子。当有0.2mol电子转移时,生成0.1mol Cl2,这些氯气在标准状况下的体积为0.1mol×22.4L/mol=2.24L;
(4)50mL36.5%1.2g/mL浓盐酸中含有氯化氢的物质的量为![]() =0.6mol,根据反应4HCl(浓)+MnO2
=0.6mol,根据反应4HCl(浓)+MnO2![]() Cl2↑+MnCl2+2H2O,若0.6molHCl完全反应转化为Cl2,生成Cl2的物质的量为0.15mol,标况下的体积为3.36L;由于浓盐酸易挥发,且只有浓盐酸与二氧化锰反应,反应过程中浓盐酸会逐渐变稀,稀到一定程度反应不再进行,因此0.6mol的HCl不能完全反应,则生成的Cl2的总物质的量小于0.15mol,标况下的体积也小于3.36L;
Cl2↑+MnCl2+2H2O,若0.6molHCl完全反应转化为Cl2,生成Cl2的物质的量为0.15mol,标况下的体积为3.36L;由于浓盐酸易挥发,且只有浓盐酸与二氧化锰反应,反应过程中浓盐酸会逐渐变稀,稀到一定程度反应不再进行,因此0.6mol的HCl不能完全反应,则生成的Cl2的总物质的量小于0.15mol,标况下的体积也小于3.36L;
(5)氯气可从碘化钾中置换出碘,碘遇淀粉变蓝色,因此,检验氯气是否收集满的方法是用湿润的淀粉碘化钾试纸靠近集气瓶口,若试纸变蓝证明氯气已收集满。


科目:高中化学 来源: 题型:
【题目】用O2将HCl转化为Cl2,可提高效益,减少污染,
(1)传统上该转化通过如图所示的催化剂循环实现,

其中,反应①为:2HCl(g) + CuO(s)![]() H2O(g)+CuCl2(g) △H1
H2O(g)+CuCl2(g) △H1
反应②生成1molCl2(g)的反应热为△H2,则总反应的热化学方程式为___________(反应热用△H1和△H2表示)。
(2)新型RuO2催化剂对上述HCl转化为Cl2的总反应具有更好的催化活性,
①实验测得在一定压强下,总反应的HCl平衡转化率随温度变化的aHCl—T曲线如图,则总反应的△H___0(填“>”、“﹦”或“<”);A、B两点的平衡常数K(A)与K(B)中较大的是_______。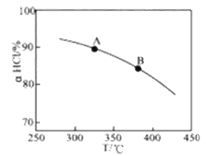
②在上述实验中若压缩体积使压强增大,画出相应aHCl—T曲线的示意图,并简要说明理由______________。
③下列措施中有利于提高aHCl的有___________。
A、增大n(HCl) B、增大n(O2)
C、使用更好的催化剂 D、移去H2O
(3)一定条件下测得反应过程中n(Cl2)的数据如下:
t(min) | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
n(Cl2)/10-3mol | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
计算2.0~6.0min内以HCl的物质的量变化表示的反应速率______(以mol·min-1为单位,写出计算过程)。
(4)Cl2用途广泛,写出用Cl2制备漂白粉的化学方程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关离子方程式,正确的是( )
A. 稀硝酸和过量的铁屑反应:Fe+4H++ NO3-= Fe3++NO↑+2H2O
B. NH4HCO3溶液与少量的NaOH溶液混合:HCO3-+OH- = CO32-+H2O
C. 碳酸氢钠溶液水解的离子方程式:HCO3-+H2O![]() CO32-+H3O+
CO32-+H3O+
D. Fe(OH)3溶于氢碘酸中:Fe(OH)3+3H+= Fe3++3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种激光染料,应用于可调谐染料激光器,它由C、H、O三种元素组成,分子球棍模型如图所示,下列有关叙述正确的是( )
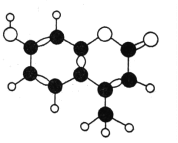
①分子式为C10H9O3 ②不能溶于水 ③1mol该物质最多能与4molH2加成 ④能使酸性KMnO4溶液褪色 ⑤1mol该物质最多能与含2mol NaOH的溶液反应
A. ①②③B. ③④⑤C. ②③④D. ②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生物电池的说法错误的是
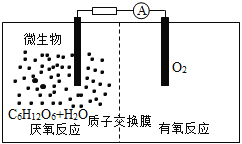
A.正极反应中有CO2生成
B.微生物促进了反应中电子的转移
C.质子通过交换膜从负极区移向正极区
D.电池总反应为C6H12O6+6O2=6CO2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人工肾脏可用电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图,下列有关说法不正确的是( )
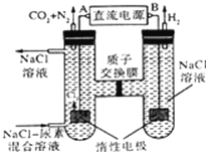
A.B为电源的正极
B.电解结束后,阴极室溶液的pH与电解前相比将升高
C.电子移动的方向是B→右侧惰性电极,左侧惰性电极→A
D.阳极室中发生的反应依次为2Cl﹣﹣2e﹣=Cl2↑、CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为前四周期元素,原子序数依次增大。基态A原子的核外电子占据4个原子轨道;B与C同主族,大气平流层中单质B3浓度减少会致人患皮肤癌增加;D是前四周期元素中第一电离能最小的元素;E的合金是当今用量最大的合金。
(1)E在同期表中的位置是_______,其基态原子的简化电子排布式为____________。
(2)CB![]() 的立体构型是______。
的立体构型是______。
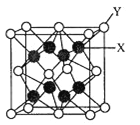
(3)D2C的晶胞结构与CaF2晶胞(如图)相似,则Y应为____(填离子符号);D2C的熔点比CaF2熔点__________________(填“高”、“低”或“无法比较”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数,下列说法不正确的是
A.标准状况下,11.2L的CHCl3所含的分子数为0.5NA
B.28g乙烯所含共用电子对数为6NA
C.2.8g的聚乙烯中含有的碳原子数为0.2NA
D.1mol乙烯中同一平面的原子有6NA个
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com