
【题目】有一反应:2E(g)+F(g)![]() 2G(g),图中曲线是该反应在不同温度下的平衡曲线,y轴表示F的转化率,图中有a、b、c三点,则下列描述中正确的是
2G(g),图中曲线是该反应在不同温度下的平衡曲线,y轴表示F的转化率,图中有a、b、c三点,则下列描述中正确的是

A. 该反应是放热反应
B. b点时混合气体的平均摩尔质量不再变化
C. T1温度下a点表示若想达到平衡,可以采取增大压强的方法
D. c 点可表V正逆
科目:高中化学 来源: 题型:
【题目】以石墨为电极,电解KI溶液(含有少量的酚酞和淀粉).下列说法错误的是
A. 阴极附近溶液显红色 B. 阴极逸出气体
C. 阳极附近溶液呈蓝色 D. 溶液中OH-的物质的量浓度变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表和元素周期律对化学学习具有指导意义,下列有关叙述正确的是( )
A. 铅位于周期表中金属与非金属元素交界处,可做半导体材料
B. 若存在简单阴离子R2-,则R一定属于第ⅥA族元素
C. S和Se属于第ⅥA族元素,H2S还原性比H2Se的强
D. 元素原子最外层电子数较少的金属一定比最外层电子数较多的金属活动性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法正确的是( )
A. 光伏电池板的主要成分是二氧化硅
B. 导致酸雨的主要物质有SO2、NO2和CO2等
C. 食品包装袋中的铁粉包是为了防止食品氧化而变质
D. 包装食品的保鲜膜最好选用PVC(聚氯乙烯)材质的保鲜膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组进行“活泼金属与酸反应”的实验,将5.4g的铝片投入500mL 0.5molL﹣1的硫酸溶液中,下图为反应产生氢气速率与反应时间的关系图. 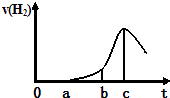
(1)下列关于图像的说法不正确的是(填序号,下同); ①a→b段产生H2加快可能是表面的氧化膜逐渐溶解,加快了反应速率
②b→c段产生H2较快可能是该反应放热,导致温度升高,加快了反应
③c以后,产生H2速率逐渐下降可能是铝片趋于消耗完全
(2)其他条件不变,现换用500mL 1molL﹣1盐酸,产生氢气速率普遍较使用500mL 0.5molL﹣1硫酸的快,可能的原因是; ①盐酸中c(H+)的浓度更大 ②Cl﹣有催化作用 ③SO42﹣有催化作用
④SO42﹣有阻化作用(使反应变慢) ⑤Al3+有催化作用
(3)要加快铝与硫酸溶液制H2的反应速率,小组成员提出一系列方案,比如:①加入某种催化剂;②加入蒸馏水;③将铝片换成铝粉;④增加硫酸的浓度至18mol/L;⑤;⑥ . 以上方案不合理的有;请你再补充两种合理方案,填入空白⑤⑥处.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】21世纪是钛的世纪.在800℃~1000℃时电解TiO2可制得钛,装置如图所示.下列叙述正确的是( ) 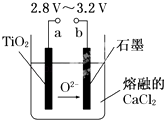
A.a为电源的正极
B.石墨电极上发生还原反应
C.阴极发生的反应为:TiO2+4e﹣═Ti+2O2﹣
D.每生成0.1mol钛,转移电子0.2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质变化的说法不正确的是( )
A. 石油的分馏和裂化都是化学变化 B. 硝化反应和酯化反应都属于取代反应
C. 煤的液化和气化都是化学变化 D. 乙烯与溴水反应和苯与H2反应都属于加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作正确的是( )
A.滴定前用待测液润洗锥形瓶
B.容量瓶和滴定管使用前均需要检漏
C.蒸馏完毕时,先关闭冷凝水,再停止加热
D.分液时,上层溶液先从上口倒出,下层溶液再从下口放出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族.B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物. 请回答下列问题:;
(1)B的原子结构示意图;
(2)C、D、E三种原子对应的离子半径由大到小的顺序是(填具体离子);由A、B、C三种元素按4:2:3组成的化合物所含的化学键类型属于 .
(3)在100mL18mol/L的浓的A、C、E 组成酸溶液中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是;(填序号) a.7.32L b.6.72L c.20.16L d.30.24L
若使上述反应中剩余的铜片继续溶解,可向其中加入硝酸钠,反应的离子方程式为: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com