
【题目】已知:2CO(g)+O2(g)=2CO2(g) △H=-566 kJ·mol-1
2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g) △H=-452 kJ·mol-1
根据以上热化学方程式判断,下列说法正确的是
A. 1molCO 完全燃烧,放出热量为283 J
B. Na2O2(s)+CO2(s)=Na2CO3(s)+ ![]() O2(g) △H=-226 kJ·mol-l
O2(g) △H=-226 kJ·mol-l
C. CO(g) 与Na2O2(s)反应放出509kJ 热量时,电子转移数为1.204×1024
D. CO 的燃烧热为566 kJ·mol-1
【答案】C
【解析】A、燃烧热是指1mol可燃物燃烧释放的热量,1molCO燃烧放热283kJ,故A错误;B、根据2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g) △H=+452kJ·mol-1可知,Na2O2(s)+CO2(s) =Na2CO3(s)+ ![]() O2(g) △H=+226kJ·mol-l,故B错误;C、已知:①2CO(g)+O2(g)═2CO2(g) △H=-566kJ/mol,②Na2O2(s)+CO2(g)═Na2CO3(s)+
O2(g) △H=+226kJ·mol-l,故B错误;C、已知:①2CO(g)+O2(g)═2CO2(g) △H=-566kJ/mol,②Na2O2(s)+CO2(g)═Na2CO3(s)+ ![]() O2(g)△H=-226kJ/mol,据盖斯定律(①+②×2)÷2得:CO(g)+Na2O2(s)=Na2CO3(s) △H=509kJ/mol,反应中C由+2价变成+4价,电子转移数为2mol,故C正确;D、燃烧热是指1mol可燃物燃烧释放的热量,根据2CO(g)+O2(g) =2CO2(g) △H=-566kJ·mol-1,CO的燃烧热为283kJ·mol-1,故D错误;故选C。
O2(g)△H=-226kJ/mol,据盖斯定律(①+②×2)÷2得:CO(g)+Na2O2(s)=Na2CO3(s) △H=509kJ/mol,反应中C由+2价变成+4价,电子转移数为2mol,故C正确;D、燃烧热是指1mol可燃物燃烧释放的热量,根据2CO(g)+O2(g) =2CO2(g) △H=-566kJ·mol-1,CO的燃烧热为283kJ·mol-1,故D错误;故选C。


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
【题目】某学习小组查阅资料,设计以下流程验证 SO2 的还原性。
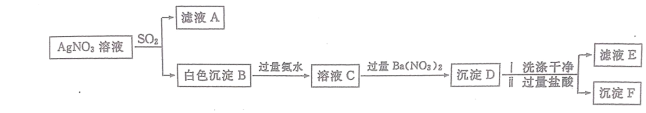
已知:沉淀 D 洗涤干净,加入过量盐酸时,部分沉淀溶解,剩余少量沉淀 F。(1)关于“白色沉淀 B”的成份
①甲同学推断白色沉淀 B 含 Ag2SO4。
实验现象依据:“沉淀 F”说明“沉淀 D”中含________________ (填化学式),进而说明“白色沉淀B"中含 Ag2SO4。
②乙同学认为“白色沉淀 B”中含有 Ag2SO3。
实验现象依据:“沉淀 D 洗涤干净,加入过量盐酸时,部分沉淀溶解”,溶解的物质为 BaSO3, 进而推断沉淀 B 中含 Ag2SO3。为进一步证实 B 中含有 Ag2SO3,可取少量滤液 E于试管中加入少量________________,有白色沉淀生成。
(2)常温下,Ag2SO4 与 Ag2SO3 中 c(Ag+)与 c(SO32-)的关系如下图所示:
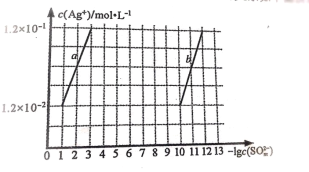
已知:Ksp(Ag2SO4)>Ksp(Ag2SO3),回答问题:
①表示 Ag2SO4 的沉淀溶解平衡关系的曲线是________________ (填“a”、“b”)
②Ksp(Ag2SO3)为________________mol3L-3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知短周期主族元素的离子 aA2+、bB+、cC3-、dD-都具有相同的电子层结构,下列叙述正确的是
A.离子的还原性:C3-<D-B.离子半径:C>D>B>A
C.原子序数: d>c>b>aD.单质的还原性: A>B>D>C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质结构与性质的说法正确的是
A.标况下,22.4 L C2H2中所含的π键数和18 g冰中所含的氢键数均为2NA
B.由于氢键的作用NH3、H2O、HF的沸点反常,且高低顺序为HF>H2O>NH3
C.VSEPR模型就是分子的空间构型
D.HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是

A. 图1表示同温度下,pH = 1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线II为盐酸,且b点溶液的导电性比a点强
B. 图2表示0.1000 mol/L CH3COOH溶液滴定20.00mL0.1000mol/LNaOH溶液所得到的滴定曲线
C. 图3表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大
D. 据图4,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在4左右
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是用于航天飞行器中的一种全天候太阳能电化学电池在光照时的工作原理。下列说法正确的是

A.夜间无光照时,a电极流出电子
B.光照时,H+由a极室通过质子膜进入b极室
C.光照时,b极反应式是VO2++2OH--e-=VO2++H2O
D.该电池与硅太阳能电池供电原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)将Al、Al2O3和Al(OH)3的混合物恰好与NaOH溶液反应,反应后溶液中溶质的化学式为_________。向反应后的溶液中通入少量CO2,反应的离子方程式为_______________。
(2)在100mLFeBr2溶液中通入标准状况下2.24LCl2,溶液中有1/4的Br- 被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为______________(结果保留两位小数)。
(3)三氟化氮(NF3)是一种无色无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
①写出该反应的化学方程式___________________,反应中生成0.2mol HNO3,转移的电子数目为__________。
②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将![]() 缓慢通入100mL水中至饱和,然后向所得饱和氯水中逐滴加人
缓慢通入100mL水中至饱和,然后向所得饱和氯水中逐滴加人![]() 溶液,整个过程中pH的变化如图所示,下列有关叙述正确的是( )
溶液,整个过程中pH的变化如图所示,下列有关叙述正确的是( )

A.曲线③④段有离子反应:![]()
B.可依据②处数据计算所溶解的![]()
C.③处表示氯气与氢氧化钠溶液恰好反应完全
D.①处![]() 约为
约为![]() 处
处![]() 的两倍
的两倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是中学常见的四种短周期元素,其原子序数依次增大,且原子核外最外层电子数都不少于2,X与W的最外层电子数相等。四种元素的单质均能在氧气中燃烧,生成四种相对分子质量都大于26的氧化物,其中有两种氧化物能溶于稀硫酸,三种氧化物能溶于烧碱溶液。四种元素的单质所形成的混合物有如下性质:
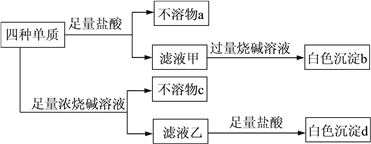
下列说法正确的是
A.原子半径:X>Y>Z>W
B.简单的气态氢化物的热稳定性:W>X
C.最高价氧化物对应水化物的碱性:Z>Y
D.X和W组成的化合物常作砂纸、砂轮的磨料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com