
| A、分子 | B、原子 | C、离子 | D、元素 |
科目:高中化学 来源: 题型:
| A、硝酸银溶液中加入铜粉:Ag++Cu=Cu2++Ag |
| B、过氧化钠投入水中发生反应:2O22-+2H2O=4OH-+O2↑ |
| C、向澄清石灰水中通入足量二氧化碳:OH-+CO2=HCO3- |
| D、金属铝溶于氢氧化钠溶液中:Al+2OH-=AlO2-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、大理石与盐酸反应:CO32-+2H+═H2O+CO2↑ |
| B、铁粉与稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
| C、氯化镁溶液中滴入氢氧化钠溶液:MgCl2+2OH-═Mg(OH)2↓+2Cl- |
| D、氯化钡溶液与稀硫酸混合:Ba2++SO42-=BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、150 mL 1 mol/L的NaCl溶液 |
| B、75 mL 1 mol/L的NH4Cl溶液 |
| C、150 mL 3 mol/L的KCl溶液 |
| D、75 mL 2 mol/L的CaCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
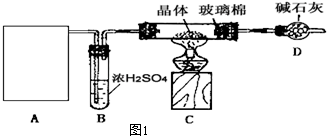

| 硬质玻璃管质量 | 硬质玻璃管与晶体总质量 | 加热后硬质玻璃管与固体 总质量 | 反应前后D的质量 | ||
| 第一次称量 | 第二次称量 | 反应前 | 反应后 | ||
| 82.112g | 85.097g | 84.028g | Wg | 78.368g | 80.474g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④⑤ | B、①②③ |
| C、④⑤ | D、⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 起始n(M):n(H2O) | M转化率 | H2O转化率 |
| 1:1 | 0.5 | 0.5 |
| 1:2 | 0.67 | 0.33 |
| 1:3 | 0.75 | 0.25 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com