
已知:T℃、P kpa时,容积为V 的密闭容器中充有1molA和2molB,保持恒温恒压使反应达平衡:A(g)+B(g)⇌C(g),平衡时C 的体积分数为40%.
(1)欲保持温度、压强在上述条件下不变,在密闭容器中充入2molA和4molB,则平衡时体系容积为 ,C的体积分数为 .
(2)另取一个容积固定不变的密闭容器,仍控制温度为T℃,加入1molB和1molC,要使平衡时C 的体积分数仍为40%,则该密闭容器体积为 .
| 化学平衡的计算.. | |
| 专题: | 化学平衡专题. |
| 分析: | 恒温恒压,使反应:A(g)+B(g) (1)温度和压强在上述条件下恒定不变,在密闭容器中充入2mol A和2mol B,2mol:2mol=1mol:1mol,平衡等效,平衡时体积分数与原状态达平衡的体积分数相同, 令转化的物质的量为a,则: A(g)+B(g) 开始(mol):1 2 0 变化(mol):a a a 平衡(mol):(1﹣a ) (2﹣a) a 则 利用同温同压下体积之比等于物质的量之比,计算容器的体积,由于是恒压过程,起始反应物成比例,所以C的体积分数和原平衡一样,据此答题; (2)容积固定不变的密闭容器,仍然控制温度为T K,使1mol A和1mol B反应达到平衡状态时,C的物质的量分数仍然为40%,则 A(g)+B(g) 开始 1 1 0 转化 x x x 平衡 1﹣x 1﹣x x 则 |
| 解答: | 解:恒温恒压,使反应:A(g)+B(g) (1)温度和压强在上述条件下恒定不变,在密闭容器中充入2mol A和2mol B,2mol:2mol=1mol:1mol,平衡等效,平衡时体积分数与原状态达平衡的体积分数相同, 令转化的物质的量为a,则: A(g)+B(g) 开始(mol):1 2 0 变化(mol):a a a 平衡(mol):(1﹣a ) (2﹣a) a 则 由于是恒压过程,起始反应物成比例,所以在容器中充入2molA和4molB和容器中充有1molA和2molB时C的体积分数一样仍为40%,所以在密闭容器中充入2molA和4molB,则平衡时体系的总物质的量为 故答案为: (2)容积固定不变的密闭容器,仍然控制温度为T K,使1mol A和1mol B反应达到平衡状态时,C的物质的量分数仍然为40%,则 A(g)+B(g) 开始(mol):1 1 0 变化(mol):x x x 平衡(mol):(1﹣x ) (1﹣x) x 则 |
| 点评: | 本题考查化学平衡的有关计算、等效平衡等,题目难度中等,注意对等效平衡的理解,掌握等效平衡规律即可解答. |


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:
在某一化学反应中,反应物A的浓度在15 s内从3.0 mol/L变成1.5 mol/L,
在这15 s内A的化学反应速率为( )
A.1.5 mol/(L·s) B.1.5 mol/L
C.0.1 mol/(L·s) D.0.1 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.电解质与非电解质的本质区别,是在水溶液或熔化状态下能否电离
B.强电解质与弱电解质的本质区别,是其水溶液导电性的减弱
C.酸、碱和盐类都属于电解质,其他化合物都是非电解质
D.常见的强酸、强碱和大部分盐都是强电解质,其他化合物都是非电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
肼(H2N﹣NH2)是一种高能燃料,有关化学反应的能量变化如图所示,已知断裂1mol化学键所需的能量(kJ):N≡N为942、O=O为500、N﹣N为154,则断裂1molN﹣H键所需的能量(kJ)是( )
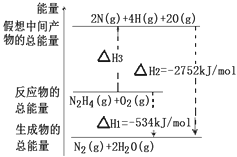
|
| A. | 194 | B. | 391 | C. | 516 | D. | 658 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11.若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液体积比是( )
|
| A. | 1:9 | B. | 1:1 | C. | 1:2 | D. | 1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实与胶体性质无关的是
A.可用半透膜除去淀粉溶液中的少量NaCl
B.黄河入海口容易形成沙洲
C.将植物油倒入水中用力搅拌可形成油水混合物
D.一束平行光线通过蛋白质溶液,从侧面可以看到一条光亮的通路
查看答案和解析>>
科目:高中化学 来源: 题型:
绿原酸的结构简式如图,下列有关绿原酸的说法不正确的是
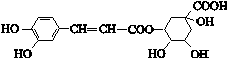
A.分子式为C16H18O9
B.能与Na2CO3反应
C.能发生取代反应和消去反应
D.0.1 mol绿原酸最多与0.8 mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
高分子材料PET聚酯树脂和PMMA的合成路线如下:

已知:
Ⅰ. RCOOR’+ R’’18OH RCO18OR’’+R’OH(R、R’、R’’代表烃基)
RCO18OR’’+R’OH(R、R’、R’’代表烃基)
|
|
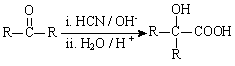 (R、R’代表烃基)
(R、R’代表烃基) (1)①的反应类型是________。
(2)②的化学方程式为________。
(3)PMMA单体的官能团名称是________、________。
(4)F的核磁共振氢谱显示只有一组峰,⑤的化学方程式为________。
(5)G的结构简式为________。
(6)下列说法正确的是________(填字母序号)。
a.⑦为酯化反应
b.B和D互为同系物
c.D的沸点比同碳原子数的烷烃高
d. 1 mol 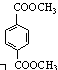 与足量NaOH溶液反应时,最多消耗4 mol NaOH
与足量NaOH溶液反应时,最多消耗4 mol NaOH
(7)J的某种同分异构体与J具有相同官能团,且为顺式结构,其结构简式是________。
(8)写出由PET单体制备PET聚酯并生成B的化学方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温时,下列溶液的pH或微粒的物质的量浓度关系正确的是 ( )
A.某溶液中由水电离出的c(H+)=1×10-a mol/L,若a>7时,该溶液pH一定为14-a
B.0.1mol/L的KHA溶液,其pH=10,c(K+)>c(A2-)>c(HA-) >c(OH-)
C.将0.2 mol/L的某一元酸HA溶液和0.1 mol/L NaOH溶液等体积混合后溶液pH大于7,则反应后的混合液:c(HA)>C(Na+)>c(A-)
D.等体积、等物质的量浓度的Na2CO3溶液与NaHCO3溶液混合:
3c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com