
【题目】氮的氧化物(NOx)是大气主要污染物,有效去除大气中的NOx是环境保护的重要课题。
(1)N2O又称笑气,有轻微的麻醉作用,N2O在一定条件下可分解为N2、O2。回答下列问题:
已知:①N2(g)+O2(g)=2NO(g) △H1=+180.5kJmol-1
②2NO(g)+O2(g)=2NO2(g) △H2=-114.14kJmol-1
③3NO(g)=N2O(g)+NO2(g) △H3=-115.52kJmol-1
则反应2N2O(g)=2N2(g)+O2(g) △H=_______ kJmol-1
(2)汽车尾气中的NO和CO可在催化剂作用下生成无污染的气体而除去。在密闭容器中充入10molCO和8molNO发生反应,测得平衡时NO的体积分数与温度、压强的关系如下图

①已知T2>T1,则反应2NO(g)+2CO(g)![]() 2N2(g)+2CO2(g),△H___0(填“>”“=”或“<”)
2N2(g)+2CO2(g),△H___0(填“>”“=”或“<”)
②该反应达到平衡后,为同时提高反应速率和NO的转化率,可采取的措施有____(填字母序号)
a.改用高效催化剂 b.缩小容器的体积 c.增加CO的浓度 d.升高温度
③压强为10MPa、温度为T1下,若反应进行到20min达到平衡状态,此时容器的体积为4L,则用N2的浓度变化表示的平均反应速率v(N2)=____,该温度下用分压表示的平衡常数Kp= ___MPa-1(分压=总压×物质的量分数)。
④在D点,对反应容器升温的同时扩大体积至体系压强减小,重新达到的平衡状态可能是图中A~G点中____点。
(3)在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2,将一定比例的O2、NH3和NOx的混合气体匀速通入装有催化剂M的反应器中反应,反应相同时间,NOx的去除率随反应温度的变化曲线如图所示。

①在50℃~150℃范围内随温度升高,NOx的去除率迅速上升的原因是____。
②当反应温度高于380℃时,NOx的去除率迅速下降的原因可能是___。
【答案】-244.1 < bc 0.025 mol·L-1·min-1 4/45(或0.089) A 催化剂活性随温度升高而增大,使NOx去除反应速率迅速增大;温度升高,反应速率加快 催化剂活性下降(或NH3与O2反应生成了NO)
【解析】
(1)根据盖斯定律计算△H;
(2)①可逆反应升高温度平衡向吸热反应方向移动;
②为提高反应速率同时提高NO的转化率,需要改变条件平衡正向进行;
③在密闭容器中充入10molCO和8molNO,发生反应,压强为10MPa、温度为T1下,若反应进行到20min达到平衡状态,NO体积分数为25%,结合三行计算列式计算,v(N2)=△c/△t,该温度下平衡常数Kp=生成物平衡分压幂次方乘积/反应物平衡分压幂次方乘积;
④若在D点升温的同时扩大体积至体系压强减小,则平衡会正向移动,NO的体积分数增大;
(3)①在一定温度范围内催化剂活性较大,超过其温度范围,催化剂活性降低;
②在温度、催化剂条件下,氨气能被催化氧化生成NO。
(1)已知:①N2(g)+O2(g)=2NO(g) △H1=+180.5kJmol-1
②2NO(g)+O2(g)=2NO2(g) △H2=-114.14kJmol-1
③3NO(g)=N2O(g)+NO2(g) △H3=-115.52kJmol-1
由盖斯定律可知,②-①2-③2得2N2O(g)=2N2(g)+O2(g),则△H=-114.14 kJmol-1 -(+180.5kJ·mol-1)2-(-115.52kJmol-1)2=-244.1kJ·mol-1,则反应2N2O (g)=2N2(g)+O2(g) △H=-244.1kJmol-1;
(2)①已知T2>T1,由图示可知反应2NO(g)+2CO(g)![]() 2N2(g)+2CO2(g),升高温度后,平衡后NO的体积分数增大,说明升高温度,平衡逆向移动,逆反应方向为吸热反应,则△H<0;
2N2(g)+2CO2(g),升高温度后,平衡后NO的体积分数增大,说明升高温度,平衡逆向移动,逆反应方向为吸热反应,则△H<0;
②2CO(g)+2NO(g)![]() N2(g+2CO2(g)△H<0;
N2(g+2CO2(g)△H<0;
a.改用高效催化剂加快反应速率,平衡不变,转化率不变,故a不能同时提高反应速率和NO的转化率;
b.缩小容器的体积,体系内压强增大,反应速率增大,平衡正向进行,NO的转化率增大,故b能同时提高反应速率和NO的转化率;
c.增加CO的浓度反应速率增大,平衡正向进行,NO的转化率增大,故c能同时提高反应速率和NO的转化率;
d.升高温度反应速率增大,反应为放热反应,升温平衡逆向进行,NO的转化率减小,故d不能同时提高反应速率和NO的转化率;故选bc;
③在密闭容器中充入10molCO和8molNO,发生反应,压强为10MPa、温度为T1下,若反应进行到20min达到平衡状态,NO体积分数为25%,结合三行计算列式计算,设反应生成氮气物质的量为x,
2CO(g)+2NO(g)![]() N2(g)+2CO2(g)△H=-749 kJ·mol-1;
N2(g)+2CO2(g)△H=-749 kJ·mol-1;
起始量(mol) 10 8 0 0
变化量(mol) 2x 2x x 2x
平衡量(mol) 10-2x 8-2x x 2x
(8-2x)/(10-2x+8-2x+x+2x)×100%=25%,x=2mol,v(N2)=△c/△t=2mol/(4L×20min)=0.025 mol·L-1·min-1;
平衡气体总物质的量=16mol,该温度下平衡常数Kp=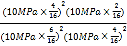 =0.089(MPa)-1;
=0.089(MPa)-1;
④若在D点升温的同时扩大体积至体系压强减小,则平衡会逆向移动,NO的体积分数增大,重新达到的平衡状态可能是图中A点;
(3)在一定温度范围内催化剂活性较大,超过其温度范围,催化剂活性降低,根据图知:
①催化剂活性随温度升高而增大,使NOx去除反应速率迅速增大;温度升高,反应速率加快.
②在一定温度范围内催化剂活性较大,超过其温度范围,催化剂活性下降;(或在温度、催化剂条件下,氨气能被催化氧化生成NO),
即:当反应温度高于380℃时,NOx的去除率迅速下降的原因可能催化剂活性下降(或NH3与O2反应生成了NO)。


科目:高中化学 来源: 题型:
【题目】在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2),当它们混合时,即产生大量![]() N2和水蒸气,并放出大量热.已知0.4mol液态肼和足量液态H2O2反应,生成氮气和水蒸气,放出256kJ的热量。
N2和水蒸气,并放出大量热.已知0.4mol液态肼和足量液态H2O2反应,生成氮气和水蒸气,放出256kJ的热量。
(1)写出该反应的热化学方程式________________。
(2)已知H2O(l)═H2O(g);△H=+44kJ·mol1,则16g液态肼燃烧生成氮气和液态水时,放出的热量是________kJ。
(3)丙烷燃烧可以通过以下两种途径:
途径I:C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=a kJ·mol1
途径II:C3H8(g)═C3H6(g)+H2(g)△H=+b kJ·mol1
2C3H6(g)+9O2(g)═6CO2(g)+6H2O(l)△H=c kJ·mol1
2H2(g)+O2 (g)═2H2O(l)△H=d kJ·mol1 (abcd均为正值)
①判断等量的丙烷通过两种途径放出的热量,途径I放出的热量_______(填“大于”、“等于”或“小于”)途径II放出的热量。
②在C3H8(g)═C3H6(g)+H2(g) 的反应中,反应物具有的总能量________(填“大于”、“等于”或“小于”)生成物具有的总能量。
③b 与a、c、d的数学关系式是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.10 mol·L-1 KOH溶液滴定 10.00 mL 0.10 mol·L-1 H2C2O4(二元弱酸)溶液所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和)。下列说法正确的是
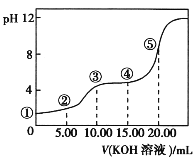
A.点①所示溶液中:![]() =1012
=1012
B.点②所示溶液中:c(K+)+c(H+)=c(HC2O4-)+c(C2O42-)+c(OH-)
C.点③所示溶液中:c(K+)>c(HC2O4-)>c(C2O42-)>c(H+)>c(OH-)
D.点④所示溶液中:c(K+)+c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.10 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若用AG表示溶液的酸度,其表达式为![]() 。室温下,实验室里用0.1mol·L-1的盐酸滴定10mL0.1mol·L-1MOH溶液,滴定曲线如图所示。下列说法正确的是
。室温下,实验室里用0.1mol·L-1的盐酸滴定10mL0.1mol·L-1MOH溶液,滴定曲线如图所示。下列说法正确的是
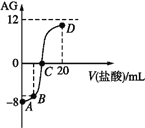
A. MOH为强碱
B. C点时加入盐酸的体积等于10mL
C. 若B点加入的盐酸体积为5mL,所得溶液中:c(M+)+2c(H+)=c(MOH)+2c(OH-)
D. 滴定过程中从A点到D点溶液中水的电离程度:A<B<C<D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫及其化合物有许多用途,相关物质的物理常数如下表所示:
H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
熔点/℃ | 85.5 | 115.2 | >600(分解) | 75.5 | 16.8 | 10.3 |
沸点/℃ | 60.3 | 444.6 | 10.0 | 45.0 | 337.0 |
回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为__________,基态S原子电子占据最高能级的电子云轮廓图为_________形。
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是_________。
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为__________。

(4)气态三氧化硫以单分子形式存在,其分子的立体构型为_____形,其中共价键的类型有______种;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为________。
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为___________g·cm3;晶胞中Fe2+位于![]() 所形成的正八面体的体心,该正八面体的边长为______nm。
所形成的正八面体的体心,该正八面体的边长为______nm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学上常用燃烧法确定有机物的组成。这种方法是在电炉加热时用纯氧氧化管内样品,根据产物质量确定有机物的组成,装置如下图所示,是用燃烧法确定有机物化学式常用的装置。产生的氧气按从左到右流向各导管的连接顺序为g-f,e-h , i-c , d-a。

回答下列问题:
(1)C装置中浓H2SO4的作用______________________________________。
(2)D装置中MnO2的作用为________________________。
(3)E中CuO的作用为_____________________。
(4)若准确称取0.90 g样品(只含C、H、O三种元素中的两种或三种)经充分燃烧后,A管质量增加1.32 g,B管质量增加0.54 g,则该有机物最简式为______________,若此有机物的相对分子质量为90,则其分子式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组探究与铜有关的物质的性质,过程设计如下:
提出猜想:
问题1:在元素周期表中,铜与铝的位置很接近,氢氧化铝具有两性,氢氧化铜有两性吗?
问题2:铁和铜都有变价,一般情况下,Fe2+的稳定性弱于的Fe3+,Cu+的稳定性也弱于Cu2+吗?
问题3:硫酸铜溶液呈蓝色,铜与浓硝酸常温下反应生成的溶液也是蓝色吗?
实验探究:
Ⅰ.解决问题1:
(1)实验需配制100mL0.50molL-1CuSO4溶液,必需的玻璃仪器有胶头滴管、烧杯、___、___。
(2)为达到目的,某同学认为只要进行两次实验即可得出结论。请写出实验②的具体内容。
①向盛有CuSO4溶液的试管中滴加NaOH溶液至过量,观察生成的Cu(OH)2沉淀是否溶解;
②___。
Ⅱ.解决问题2的实验和现象如下:
①取一定量制得的氢氧化铜固体,于坩埚中灼烧,当温度达到80~100℃时得到黑色固体粉末;继续加热至1000℃以上,黑色粉末全部变成红色粉末氧化亚铜;
②取适量红色氧化亚铜粉末于洁净试管中,加入过量的稀硫酸,得到蓝色溶液,同时观察到试管底部还有红色固体存在。根据以上实验及现象回答下列问题:
(3)写出氧化亚铜与稀硫酸反应的离子方程式:___。
(4)从实验中可得出的结论:当温度在1000℃以上时___(填Cu2+或Cu+,下同)稳定,在酸性溶液中___稳定。
Ⅲ.解决问题3,某同学设计的实验如下:
取一铜片装入试管,加入适量的浓硝酸,观察溶液的颜色变化。
(5)另一同学认为此同学设计的实验有缺陷,原因是___。
(6)铜与浓硝酸反应溶液呈绿色,有同学认为这是生成的NO2溶于其中的原因。请设计实验说明此解释是否正确(只需要写出一种方法即可)。___
实验步骤 | 实验结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2SO2(g)+ O2(g)2SO3(g);H=-196.64kJmol-1,下列说法正确的是( )
A.该反应是吸热反应
B.SO2燃烧热为196.64kJmol-1
C.在容器中充入1molSO2和0.5molO2充分反应,热变化为98.32kJ
D.当有NA个电子发生转移时,热变化为49.16kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com