
【题目】PASNa(二水合对氨基水杨酸钠)是抗结核药,其结构简式如图化合物1所示,下列说法正确的是( ) 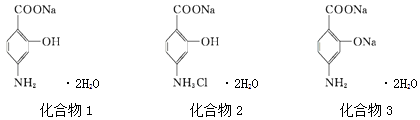
A.化合物1和化合物2均能使酸性KMnO4溶液褪色
B.化合物1的核磁共振氢谱测出5个谱峰
C.PASNa与足量盐酸反应生成如上图化合物2
D.通入足量CO2能将图化合物3转化为PASNa
【答案】AD
【解析】解:A.化合物1和化合物2分子中都含有酚羟基,二者都能够与酸性高锰酸钾溶液氧化,所以二者均能使酸性KMnO4溶液褪色,故A正确;
B.化合物1分子中含有6种等效H,则其核磁共振氢谱测出6个谱峰,故B错误;
C.PASNa与足量盐酸反应,化合物1中﹣COONa会转化成﹣COOH,无法转化成化合物2,故C错误;
D.根据强酸制取弱酸原理,向化合物的溶液中通入足量CO2,可以将图化合物3转化为PASNa,故D正确;
故选AD.
A.化合物1和混合物2分子中都含有酚羟基,都能够与酸性高锰酸钾溶液氧化;
B.核磁共振氢谱中的谱峰取决于有机物分子中等效H原子数;
C.盐酸的酸性大于苯甲酸,盐酸能够将﹣COONa转化成﹣COOH;
D.碳酸的酸性小于苯甲酸、大于苯酚,可以用二氧化碳将化合物3转化成化合物1.


科目:高中化学 来源: 题型:
【题目】某化合物的结构(键线式)及球棍模型如图1:该有机分子的核磁共振氢谱图如图2(单位是ppm):下列关于该有机物的叙述正确的是( ) 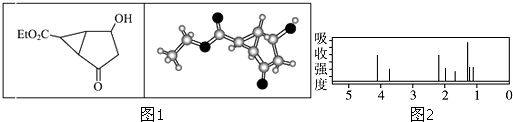
A.该有机物不同化学环境的氢原子有6种
B.该有机物属于芳香化合物
C.键线式中的Et代表的基团为﹣CH3
D.该有机物在一定条件下能够发生消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯、氮、硫的化合物与人类生活和生产有着密切的联系。请回答下列问题:
(1)瑞典化学家舍勒将软锰矿(主要成分是MnO2)与浓盐酸混合加热,在世界上首先制得了氯气。反应的化学方程式为:_________________________。其中,氧化剂是_______。若实验室制得标准状况下4.48L氯气,则转移电子的数目为_____个。
(2)在氮的化合物中,红棕色、有刺激性气味的有毒气体是___________(填写化学式),请写出该气体与水反应的化学方程式________________________。
(3)请配平浓硫酸在加热时与碳发生反应的化学方程式:____C+____H2SO4(浓)=__CO2↑+_____SO2↑+____H2O。
在该反应中,浓H2SO4表现出___________(填“吸水”、“脱水”或“氧化”)性。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是人类从海水资源获取某些重要化工原料的流程示意图:
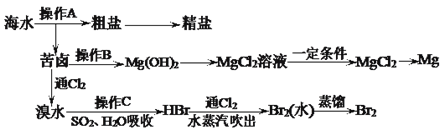
回答下列问题:
(1)操作A是___________和过滤(填实验基本操作名称)。
(2)操作B需加入下列试剂中的一种,最合适的是______(选填编号)。
a.氢氧化钠溶液 b.澄清石灰水 c.石灰乳 d.碳酸钠溶液
(3)工业上由无水MgCl2制取镁的化学方程式为__________________________________。
(4)0.25 mol Cl2缓慢通入含有0.1 mol FeBr2、0.1 mol FeI2的混合溶液中,充分反应,试用一个离子方程式表示总反应:__________________________________________。
(5)某稀硫酸和稀硝酸的混合溶液100 mL,将其平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6 g铜粉;向另一份中逐渐加入铁粉,产生气体的量随铁粉质量的变化关系如图所示(假设硝酸的还原产物为NO气体)。则原混合溶液中NO3-的物质的量为__________,硫酸的物质的量浓度为______________。
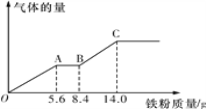
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。

根据判断出的元素回答问题:
(1)X的原子结构示意图为 ______________。
(2)比较d、e常见离子的半径大小(用化学式表示,下同):______> ;比较g、h的最高价氧化物对应水化物的酸性强弱: >_______。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知草酸镍晶体(NiC2O42H2O)难溶于水,工业上从废镍催化剂(主要成分是Ni,含有一定量的Al2O3、Fe、SiO2、CaO等)制备草酸镍晶体的流程如图所示:
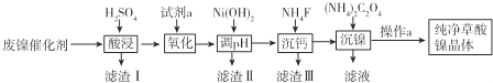
已知:①相关金属离子生成氢氧化物沉淀的pH如表:
金属离子 | Fe3+ | Fe2+ | Al3+ | Ni2+ |
开始沉淀的pH | 1.1 | 5.8 | 3.0 | 6.8 |
完全沉淀的pH | 3.2 | 8.8 | 5.0 | 9.5 |
②Ksp(CaF2)=1.46×10-10
③当某物质浓度小于1.0×10-5mol·L-1时,视为完全沉淀.
请回答下列问题:
(1)请写出一种能提高“酸浸”速率的措施:______________________________________。
(2)试剂a是一种绿色氧化剂,写出氧化时反应的离子方程式:__________________________________。
(3)调节pH的范围为________,试用化学反应原理的相关知识解释滤渣Ⅱ的生成:_____________。
(4)写出沉镍时反应的离子方程式:________________________________________________。证明Ni2+已经沉淀完全的实验步骤及现象是_____________________________________。当Ca2+沉淀完全时,溶液中c(F-)>________mol·L-1。
(5)操作a的内容是_____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质和该性质的应用均正确的是
A. 常温下浓硫酸能使铝发生钝化,可在常温下用铝制容器盛装浓硫酸
B. SiO2不与任何酸反应,可用石英制造耐酸容器
C. ClO2具有还原性,可用于自来水的杀菌消毒
D. Al、Fe、Cu对应的氧化物均为碱性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用酒精灯加热下列溶液,蒸干后灼烧,所得固体质量最大的是( )
A.20 mL 2 mol/L FeCl3溶液
B.40 mL 1 mol/L NaHCO3溶液
C.20 mL 1 mol/L Na2SO3溶液
D.40 mL 2 mol/L NH4HCO3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com