
【题目】下列有机化合物分子中所有的原子不可能都处于同一平面的是(
A.CF2=CF2B.HC≡CHC.C6H5—CH=CH—CHOD.CH3—O—CH3
【答案】D
【解析】
A.![]() 相当于乙烯分子中的氢原子全部替代为F原子,由于乙烯分子中所有原子共平面,所以
相当于乙烯分子中的氢原子全部替代为F原子,由于乙烯分子中所有原子共平面,所以![]() 中所有原子一定共平面,A项不符合题意不选;
中所有原子一定共平面,A项不符合题意不选;
B.![]() 中所有原子在同一条直线上,因此也一定在同一平面内,B项不符合题意不选;
中所有原子在同一条直线上,因此也一定在同一平面内,B项不符合题意不选;
C.![]() 相当于乙烯分子中的一个氢原子被替代为苯基,还有一个氢原子被替代为醛基;由于苯的所有原子共平面,苯基又是通过单键与碳碳双键相连,所以苯基与碳碳双键也可能共平面;醛基中的三个原子共平面,醛基又是通过单键与碳碳双键相连,所以醛基与碳碳双键也可能共平面;综上所述,
相当于乙烯分子中的一个氢原子被替代为苯基,还有一个氢原子被替代为醛基;由于苯的所有原子共平面,苯基又是通过单键与碳碳双键相连,所以苯基与碳碳双键也可能共平面;醛基中的三个原子共平面,醛基又是通过单键与碳碳双键相连,所以醛基与碳碳双键也可能共平面;综上所述,![]() 中的所有原子可能共平面,C项不符合题意不选;
中的所有原子可能共平面,C项不符合题意不选;
D.![]() 中的C形成的都是四条单键,单键键角约为109°28′,与这种C原子相连的所有原子一定不会在同一平面内,因此
中的C形成的都是四条单键,单键键角约为109°28′,与这种C原子相连的所有原子一定不会在同一平面内,因此![]() 中的所有原子一定不会共平面,D项符合题意;
中的所有原子一定不会共平面,D项符合题意;
答案选D。


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
【题目】33.6g 含杂质的Na2CO3、NaHCO3均匀混合物平均分成两份,向一份中加入250ml 1.00mol·L-1过量盐酸反应,生成标准状况下3.36L气体。将另一份充分灼烧,干燥后称得固体质量为13.7g。杂质不与酸反应,受热也不分解。求:
(1)原混合物中含有Na2CO3的物质的量。
(2)Na2CO3、NaHCO3的质量比。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,![]() 比
比![]() 少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为
少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为![]() ,且其核内质子数等子中子数.R是由A、D两元素形成的离子化合物,其中
,且其核内质子数等子中子数.R是由A、D两元素形成的离子化合物,其中![]() 与
与![]() 离子数之比为2:1。请回答下列问题:
离子数之比为2:1。请回答下列问题:
(1)![]() 形成的晶体属于______
形成的晶体属于______![]() 填写离子、分子、原子
填写离子、分子、原子![]() 晶体.
晶体.
(2)![]() 的电子排布式为______,在
的电子排布式为______,在![]() 分子中C元素原子的原子轨道发生的是______杂化,
分子中C元素原子的原子轨道发生的是______杂化,![]() 分子的VSEPR模型为______.
分子的VSEPR模型为______.
(3)![]() 的氢化物在水中的溶解度特别大,原因______
的氢化物在水中的溶解度特别大,原因______
(4)![]() 元素与同周期相邻元素的第一电离能由大到小的关系是:______
元素与同周期相邻元素的第一电离能由大到小的关系是:______![]() 用元素符号表示
用元素符号表示![]() ;用一个化学方程式说明B、D两元素形成的单质的氧化性强弱:______.
;用一个化学方程式说明B、D两元素形成的单质的氧化性强弱:______.
(5)已知下列数据:
![]()
![]()
由![]() 和
和![]() 反应生成CuO的热化学方程式是______.
反应生成CuO的热化学方程式是______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列不能用勒沙特列原理解释的是
A.实验室用排饱和食盐水的方法收集![]()
B.硫酸工业中,使用过量的空气以提高二氧化硫的转化率
C.合成氨工业中,及时液化分离![]() ,并循环利用未反应完的
,并循环利用未反应完的![]() 和
和![]()
D.合成氨工业中,500℃比常温更有利于氨的合成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知0.1 mol·L-1的氢氟酸溶液中存在电离平衡:HF![]() F-+H+,要使溶液中
F-+H+,要使溶液中![]() 的值增大,可以采取的措施是( )
的值增大,可以采取的措施是( )
①加少量烧碱溶液 ②升高温度 ③通入少量HF气体 ④加水
A.①②B.①③C.②④D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酰氯![]() 可用作杀虫剂,通常条件下为无色液体,熔点为
可用作杀虫剂,通常条件下为无色液体,熔点为![]() ,沸点为
,沸点为![]() 。在潮湿空气中“发烟”;
。在潮湿空气中“发烟”;![]() 以上开始分解,生成二氧化硫和氯气,长期放置也可分解,制备时以活性炭为催化剂,反应的热化学方程式为
以上开始分解,生成二氧化硫和氯气,长期放置也可分解,制备时以活性炭为催化剂,反应的热化学方程式为![]()
![]() ,所用装置如图所示。下列叙述错误的是
,所用装置如图所示。下列叙述错误的是![]()
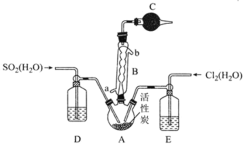
A.球形冷凝管B应从a口进水b口出水
B.可通过观察D和E中气泡产生速率控制通入A中的![]() 和
和![]() 的体积比
的体积比
C.仪器C,D,E中盛放的试剂依次为无水氯化钙、浓硫酸、浓硫酸
D.长期放置的硫酰氯液体会发黄的原因是溶解了氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中的一定量混合气体发生反应xM (g)+yN(g)![]() zP(g)。平衡时测得M的浓度为0.80 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得M的浓度降低为0.50 mol/L。下列有关判断正确的是
zP(g)。平衡时测得M的浓度为0.80 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得M的浓度降低为0.50 mol/L。下列有关判断正确的是
A.x + y < zB.平衡向正反应方向移动
C.N的转化率降低D.混合气体的密度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示。请回答:
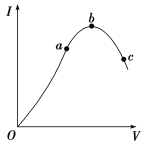
(1)“O”点导电能力为0的理由是_________________________。
(2)写出醋酸的电离方程式___________________________________________。
(3)a、b、c三点溶液中氢离子浓度由小到大的顺序为__________________ 。
(4)a、b、c三点处,电离程度最大的是________。
(5)醋酸与氨水反应的离子方程式:__________________ 。
(6)写出醋酸电离平衡常数表达式:_______________;
(7)向0.1mol/L 醋酸溶液中加入水,电离平衡向_______移动 (填“左”或“右”) ;n(CH3COOH)_______; c(CH3COO-)/c(CH3COOH)_______(填“增大”、“减小”或“不变”);
(8)500mL 0.1mol/L 醋酸溶液a和500mL 0.1mol/L 盐酸溶液b与足量Zn粉反应,初始速率a___b;生成H2的量a____b;完全中和这两种酸,消耗NaOH的量a___b(填“<”、“>”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠![]() 是一种高效的漂白剂和消毒剂,它在酸性条件下生成NaCl并放出
是一种高效的漂白剂和消毒剂,它在酸性条件下生成NaCl并放出![]() ,
,![]() 有类似
有类似![]() 的性质。某兴趣小组探究亚氯酸钠的制备与性质。
的性质。某兴趣小组探究亚氯酸钠的制备与性质。
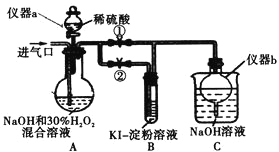
(I)制备亚氯酸钠
关闭止水夹![]() ,打开止水夹
,打开止水夹![]() ,从进气口通入足量
,从进气口通入足量![]() ,充分反应。
,充分反应。
(1)仪器a的名称为_________,仪器b的作用是_________。
(2)装置A中生成![]() 的化学方程式为_________。
的化学方程式为_________。
(3)若从装置A反应后的溶液中获得![]() 晶体,则主要操作有:减压蒸发浓缩、________、过滤、洗涤、干燥等。
晶体,则主要操作有:减压蒸发浓缩、________、过滤、洗涤、干燥等。
(II)探究亚氯酸钠的性质
停止通![]() 气体,再通入空气一段时间后,关闭止水夹
气体,再通入空气一段时间后,关闭止水夹![]() ,打开止水夹
,打开止水夹![]() ,向A中滴入稀硫酸。
,向A中滴入稀硫酸。
(4)请写出这时A中发生反应的离子方程式_________。
(5)开始时A中反应缓慢,稍后产生气体的速率急剧加快,请解释可能的原因_________。
(6)B中现象为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com