
|
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案科目:高中化学 来源:不详 题型:填空题

| A.铁圈和银圈左右摇摆不定 |
| B.保持平衡状态不变 |
| C.铁圈向下倾斜 |
| D.银圈向下倾斜 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
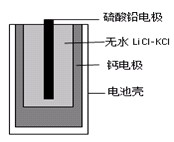
 MgxMo3S4,下列说法错误的是( )
MgxMo3S4,下列说法错误的是( )| A.放电时Mg2+向正极迁移 |
| B.放电时正极反应为Mo3S4+2xe-=Mo3S42x- |
| C.充电时Mo3S4发生氧化反应 |
| D.充电时阴极反应为Mg2++2e-=Mg |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
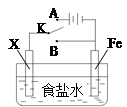
| A.若X为锌棒,开关K置于A处,可减缓铁的腐蚀,这种方法称为牺牲阴极的阳极保护法 |
B.若X为铜棒,开关K置于A处,装置中发生的总反应为2NaCl+2H2O 2NaOH+Cl2↑+H2↑ 2NaOH+Cl2↑+H2↑ |
| C.若X为碳棒,开关K置于B处,在铁棒附近滴入铁氰化钾溶液可看到溶液变血红色 |
| D.若X为碳棒,开关K置于B处,向食盐水中滴入酚酞溶液可看到碳棒附近先变红 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电镀时,通常把待镀的金属制品作阳极 |
| B.氯碱工业是电解熔融的NaCl,在阳极能得到Cl2 |
C.如图中电子由Zn极流向Cu,盐桥中的Cl-移向CuSO4溶液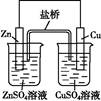 |
| D.氢氧燃料电池(酸性电解质)中O2通入正极,电极反应为:O2+4H++4e-=2H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
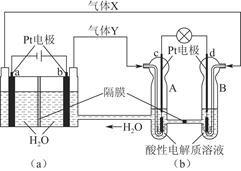
| A.图(a)把化学能转化为电能,图(b)把电能转化为化学能,水得到了循环使用 |
| B.当有0.1 mol电子转移时,a极产生0.56 L O2(标准状况下) |
| C.c极上发生的电极反应是:O2+4H++4e-=2H2O |
| D.图(b)中电子从c极流向d极,提供电能 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
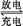 3Zn(OH)2+2Fe(OH)3+4KOH,以下说法错误的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,以下说法错误的是( )| A.电池放电是化学能转化成电能的过程 |
B.放电时正极反应为:Fe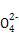 +4H2O+3e- +4H2O+3e-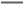 Fe(OH)3+5OH- Fe(OH)3+5OH- |
| C.充电时电池的负极接外电源的正极 |
| D.充电时电解质溶液中的阴离子向阳极定向移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
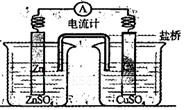
| A.铜是阳极,铜片上有气泡产生 |
| B.铜离子在铜片表面被氧化 |
| C.电子从锌片经外电路流向铜片 |
| D.正极附近的SO42-离子浓度逐渐增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电路中的电子经正极、熔融的K2CO3、负极后再到正极,形成闭合回路 |
| B.电池放电时,电池中CO32-的物质的量将逐渐减少 |
| C.正极反应为2H2O+O2+4e-===4OH- |
| D.放电时CO32-向负极移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com