
【题目】一只量程为25 mL的滴定管,若液面在8.0 mL处,将溶液全部放下来,液体的体积为( )
A.17.00 mLB.大于17.00 mLC.小于17.00 mLD.无法确定
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案科目:高中化学 来源: 题型:
【题目】采用恰当的分离混合物的方法,下列做法中正确的是
A. 分离KNO3和碘的固体混合物:四氯化碳,分液
B. 除去AgI胶体中混有的I-离子:过滤、洗涤、干燥
C. 分离食用油和水:分液
D. 从溴水中分离溴:蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于铁的氧化物①FeO、②Fe2O3、③Fe3O4的下列说法中正确的是( )
A.都是黑色固体
B.都不溶于水
C.铁元素化合价都相同
D.都能与水反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤代烃能够发生下列反应:2CH3CH2Br+2Na→CH3CH2CH2CH3+2NaBr,下列有机物可以合成环丁烷(□)的是
A. BrCH2CH2CH2CH2Br B. ![]()
C. ![]() D. CH3CH2CH2CH2Br
D. CH3CH2CH2CH2Br
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是有关各种形式能量的相互转化途径的叙述,其中错误的是( )
A.家庭液化气灶将化学能转变为热能
B.灯泡将电能全部转变为光能
C.光合作用将光能转变为化学能
D.太阳能电池将光能转变为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中药肉桂中含有某有机物A(分子中只含有C、H、O),其分子的球棍模型如右图所示。回答下列问题:
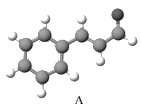
(l)写出有机物A的结构简式:__________。其分子中含有的官能团名称是__________。
(2)有机物A可由有机物M(![]() )为原料制备,转化关系如下图所示:
)为原料制备,转化关系如下图所示:

①由M生成N的反应类型是________________。
②由B生成A的反应条件是_________________。
③写出由N生成B的化学方程式:_________________。
④写出一种满足下列条件的M的同分异构体的结构简式:_________________。
a.与有机物M具有相同的官能团 b.苯环上一氯代物只有两种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D是原子序数依次增大的同一短同期元素,A、B是金属元素,C、D是非金属元素。
(1)A、B各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为_____________________________________。
(2)A与C 可形成化合物A2C,该化合物的电子式为_______________________。
(3)C的低价氧化物通入D单质的水溶液中,发生反应的化学方程式为________________________________________。
(4)A、B、C、D四种元素简单离子的离子半径由大到小的顺序是(用离子符号表示):_____>_____>______>______。
(5)四种元素中金属性最强的(填元素符号)______;非金属性最强的__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是
A. 0.5mol![]() 含中子数为8NA
含中子数为8NA
B. 常温下,1 mol NH4Cl含共价键数目为5NA
C. 足量的Cu与含溶质1mol的浓H2SO4反应,转移的电子数为NA
D. 11.2LH2和O2的混合气体中分子数目为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组探究与铜有关的物质的性质,过程设计如下:
(提出猜想)
问题1:在周期表中,铜与铝的位置很接近,氢氧化铝具有两性,氢氧化铜有两性码?
问题2:铁和铜都有变价,一般情况下,Fe2+的稳定性小于的Fe3+,Cu+的稳定性也小于Cu2+吗?
问题3:硫酸铜溶液呈蓝色,铜与浓硝酸常温下反应生成的溶液也是蓝色吗?
(实验探究)
I. 解决问题1:
(1)实验需配制100mL 0.50mol·L-1 CuSO4溶液,除了天平、烧杯、玻璃棒、胶头滴管以外必需的玻璃仪器是______。
(2)为达到目的,某同学认为只要进行两次实验即可得出结论。请写出实验②的具体内容。
①向盛有CuSO4溶液的试管中滴加NaOH溶液至过量,观察生成的Cu(OH)2沉淀是否溶解;
②_______。
II. 解决问题2的实验步骤和现象如下:
①取一定量制得的氢氧化铜固体,于坩埚中灼烧,当温度达到80C~100C得到黑色固体粉末;继续加热至1000C以上,黑色粉末全部变成红色粉末氧化亚铜(Cu2O);
②取适量红色氧化亚铜粉末于洁净试管中,加入过量的稀硫酸,得到蓝色溶液,同时观察到试管底部还有红色固体存在。根据以上实验及现象:
(3)写出氧化亚铜与稀硫酸反应的离子方程式____________________________。
(4)从实验中可得出的结论是:当温度在1000C以上时________(填:Cu2+或Cu+,下同)稳定,在酸性溶液中________稳定。
III. 解决问题3,某同学设计的实验如下:取一铜片装入试管,加入适量的浓硝酸,观察溶液的颜色变化。
(5)另一同学认为此同学设计的实验有缺陷,原因是__________________________。
(6)铜与浓硝酸反应溶液呈绿色,有同学认为这是生成的NO2溶于其中的原因,并试图设计实验排除这种干扰。提出实验方案:向反应后的溶液中通入足量空气。试用化学反应方程式解释其原理:___________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com