
| 化学键 | C-H | C-F | H-F | F-F |
| 键能/(kJ•mol-1) | 414 | 489 | 565 | 155 |
| A. | -1940 kJ•mol-1 | B. | 1940 kJ•mol-1 | C. | -485 kJ•mol-1 | D. | 485 kJ•mol-1 |
科目:高中化学 来源: 题型:解答题
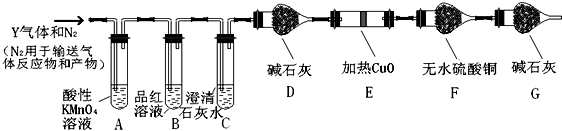 (2)写出产生CO2的化学方程式C+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$ CO2↑+2SO2↑+2H2O.
(2)写出产生CO2的化学方程式C+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$ CO2↑+2SO2↑+2H2O.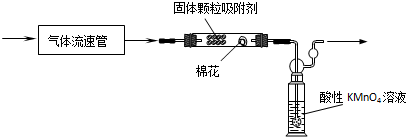
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol NH5中含有5 mol N-H 键 | |
| B. | NH5的熔沸点高于NH3 | |
| C. | NH5固体投入少量水中,可产生两种气体 | |
| D. | NH5中既有离子键又有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4和C4H8 | B. | CH4和C3H6 | C. | C2H6 和C3H6 | D. | C2H6 和C4H8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
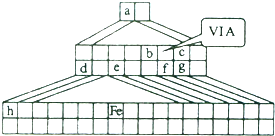
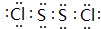 ;该物质遇水不稳定,生成一种黄色沉淀和无色气体,还得到一种酸性溶液.试写出该过程的化学方程式:2S2Cl2+2H2O=3S+SO2↑+4HCl;
;该物质遇水不稳定,生成一种黄色沉淀和无色气体,还得到一种酸性溶液.试写出该过程的化学方程式:2S2Cl2+2H2O=3S+SO2↑+4HCl;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
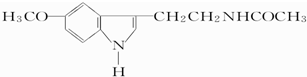 ,下列对该化合物的叙述正确的是( )
,下列对该化合物的叙述正确的是( )| A. | 它属于芳香烃 | B. | 它属于醇类 | ||
| C. | 分子式为C13H17O2N2 | D. | 在一定条件下可以发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

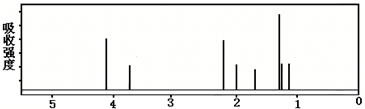
| A. | 键线式中的Et代表的基团为-CH3 | |
| B. | 该有机物属于芳香族化合物 | |
| C. | 该有机物不同化学环境的氢原子有8种 | |
| D. | 该有机物不可能发生消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CHCH(Br)CH2Br | B. | CH2=CH(Br)CHCH2Br | C. | CH2=CH2CH2CHBr2 | D. | CH Br2CH=CHCH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com