
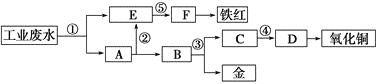
【题目】某酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等离子。利用常用的酸、碱和工业生产中废铁屑,设计如下工艺流程,从废水中回收金,并生产一定量的铁红和氧化铜。下列说法不正确的是
A.标号①②③处发生的反应均为氧化还原反应
B.标号③处加入的相应物质是稀硝酸
C.标号①处发生的离子反应最多有三个
D.铁红的化学式为Fe2O3,工业上常用作红色颜料
【答案】C
【解析】
由工艺流程图示知,E为铁元素的离子,而A为铜、金的混合物,通过过滤将铁元素与活泼性比它弱的铜、金分离出来,因此①处加入的物质为铁屑,发生的反应为Fe+2H+=Fe2++H2↑,2Fe3++Fe=3Fe2+,Cu2++Fe=Cu+Fe2+,2Au3++3Fe=2Au+3Fe2+;②处发生反应:Fe+2H+=Fe2++H2↑。加入稀硫酸以除去铜、金中过量的铁屑,并将过滤后的硫酸亚铁溶液与含Fe2+的E溶液相混合;③处发生反应:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,利用金不溶于硝酸的性质将铜与金分离开;④处发生反应:Cu2++2OH-=Cu(OH)2↓;将得到的铜离子用氢氧化钠转化为氢氧化铜沉淀,从而再受热分解为氧化铜;⑤处发生反应:Fe2++2OH-=Fe(OH)2↓;加入氢氧化钠将亚铁离子转化为氢氧化亚铁沉淀,再利用空气将其转化为氢氧化铁沉淀,最终受热分解为铁红(氧化铁),以此解答。
根据上述分析可知①为铁屑,②为稀硫酸,③为稀硝酸,④为NaOH,⑤为NaOH。A中含有Fe、Cu、Au,B中含有Cu、Au,C为Cu(NO3)2,D为Cu(OH)2,E中含有FeSO4,F中为Fe(OH)3,
A.由以上分析可知,标号①②③处发生的反应有元素化合价的变化,均为氧化还原反应,A正确;
B.标号③处加入的相应物质是稀硝酸,目的是分离铜和金单质,B正确;
C.由以上分析可知,标号①处发生的离子反应有:Fe+2H+=Fe2++H2↑,2Fe3++Fe=3Fe2+,Cu2++Fe=Cu+Fe2+,2Au3++3Fe=2Au+3Fe2+;最多有四个,C错误;
D. Fe2O3的俗名是铁红,工业上常用作红色颜料,D正确;
故合理选项是C。


科目:高中化学 来源: 题型:
【题目】硅是无机非金属材料的主角,硅芯片的使用,促进了信息技术的革命。
![]() 陶瓷、水泥和玻璃都属于传统硅酸盐材料。其中,生产普通玻璃的主要原料除了
陶瓷、水泥和玻璃都属于传统硅酸盐材料。其中,生产普通玻璃的主要原料除了![]() 、
、![]() 外还 ______,玻璃制作过程中发生了
外还 ______,玻璃制作过程中发生了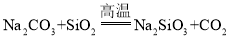 的反应,碳酸酸性强于硅酸,但为什么该反应可在高温下发生? ______。
的反应,碳酸酸性强于硅酸,但为什么该反应可在高温下发生? ______。
![]() 工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如图:
工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如图:
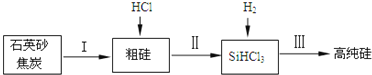
![]() 请写出反应Ⅱ、Ⅲ的化学方程式:Ⅱ ______、Ⅲ ______。
请写出反应Ⅱ、Ⅲ的化学方程式:Ⅱ ______、Ⅲ ______。
![]() 在流化床反应的产物中,
在流化床反应的产物中,![]() 大约占
大约占![]() ,所含有的其它物质的沸点数据如下表:
,所含有的其它物质的沸点数据如下表:
物质 | Si |
|
|
|
| HCl |
|
沸点 | 2355 |
|
|
|
|
|
|
提纯![]() 的主要工艺操作依次是沉降、冷凝和分馏
的主要工艺操作依次是沉降、冷凝和分馏![]() 相当于多次蒸馏
相当于多次蒸馏![]() 。沉降是为了除去 ______ ;在空气中冷凝所得液体主要含有 ______ ;若在实验室进行分馏提纯液体,应该采取以下加热方法中的 ______。
。沉降是为了除去 ______ ;在空气中冷凝所得液体主要含有 ______ ;若在实验室进行分馏提纯液体,应该采取以下加热方法中的 ______。
A.电炉加热![]() 酒精灯加热
酒精灯加热![]() 砂浴加热
砂浴加热![]() 水浴加热
水浴加热
![]() 极易水解,其完全水解时的反应方程式为 ______。
极易水解,其完全水解时的反应方程式为 ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多相催化反应是在催化剂表面通过吸附、解吸过程进行的。我国学者发现T℃时(各物质均为气态),甲醇与水在铜基催化剂上的反应机理和能量图如图:
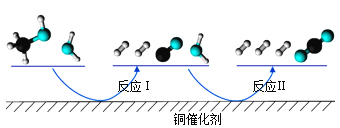

下列说法正确的是( )
A.反应Ⅱ的热化学方程式为:CO(g)+H2O(g)=H2(g)+CO2(g) △H=+akJ/mol(a>0)
B.1molCH3OH(g)和1molH2O(g)的总能量大于1molCO2(g)和3molH2(g)的总能量
C.选择优良的催化剂降低反应Ⅰ和Ⅱ的活化能,有利于减少过程中的能耗
D.CO(g)在反应中生成又消耗,CO(g)可认为是催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为海水利用的部分过程。下列有关说法正确的是
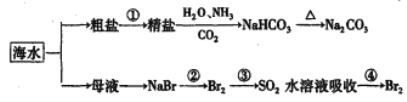
A. 粗盐提取精盐的过程只发生物理变化
B. 用澄清的石灰水可鉴别Na2CO3产品是否含有NaHCO3
C. 在第②、④步骤中,溴元素均被还原
D. 制取NaHCO3的反应是利用其溶解度小于NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学进行下列实验:
装置 | 操作 | 现象 |
| 将盛有浓硝酸的烧杯A放入盛有淀粉KI溶液的烧杯C中,然后将铜片放入烧杯A后,立即用烧杯B罩住。 | 烧杯A液体上方立即出现大量红棕色气体;一段时间后,红棕色气体消失,烧杯A和C中的液体都变成蓝色。 |
下列说法不合理的是
A.烧杯A中发生反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
B.红棕色气体消失可能与NO2和烧杯C中的KI发生反应有关
C.烧杯A中溶液变蓝是因为产生了Cu(NO3)2
D.若将铜片换成铁片,则C中的液体不会变蓝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国传统文化对人类文明贡献巨大,史书记载中也蕴含着丰富的化学知识。下列说法不正确的是 ![]()
![]()
A.《本草经集注》中写到“如握雪不冰。以火烧之,紫青烟起,仍成灰,乃真硝石也”。“硝石”指的是KNO3
B.我国清代《本草纲目拾遗》中记载药物“鼻冲水”,写道:“贮以玻璃瓶,紧塞其口,勿使泄气,则药力不减,气甚辛烈,触人脑,非有病不可嗅.虚弱者忌之。宜外用,勿服。”这里的“鼻冲水”是指氨水
C.《神农本草经》说:“水银,镕化(加热)还复为丹。”![]() 黄帝九鼎神丹经
黄帝九鼎神丹经![]() 中的“柔丹”“伏丹”都是在土釜中加热Hg制得的。这里的“丹”是指汞的硫化物
中的“柔丹”“伏丹”都是在土釜中加热Hg制得的。这里的“丹”是指汞的硫化物
D.《后汉书![]() 郡国志》中记载:“石出泉水……其水有肥,燃之极明,不可食,县人谓之石漆。”《酉阳杂俎》一书:“高奴县石脂水,水腻,浮上如漆,采以膏车及燃灯极明。”这里的“石漆”、“石脂水”是指石油
郡国志》中记载:“石出泉水……其水有肥,燃之极明,不可食,县人谓之石漆。”《酉阳杂俎》一书:“高奴县石脂水,水腻,浮上如漆,采以膏车及燃灯极明。”这里的“石漆”、“石脂水”是指石油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列叙述正确的是
A. 13g锌与一定量浓硫酸恰好完全反应,生成气体的分子数为0.2NA
B. 71g氯气通入足量的水中,反应中转移的电子总数为NA
C. 由D和18O所组成的水11g,所含的中子数为4NA
D. 1molBrCl与H2O完全反应生成氯化氢和次溴酸,转移的电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图A、B、C、D、E、F等几种常见有机物之间的转化关系图,其中A是面粉的主要成分;C和E反应能生成F,F具有香味。
![]()
在有机物中,凡是具有—CHO结构的物质,具有如下性质:
(1)与新制氢氧化铜悬浊液反应,产生砖红色沉淀;
(2)在催化剂作用下, —CHO被氧气氧化为—COOH,即![]() 。
。
根据以上信息及各物质的转化关系完成下列各题。
(1)B的化学式为_________,C的结构简式为__________。
(2)其中能与新制氢氧化铜悬浊液反应产生砖红色沉淀的物质有_________(填名称)。
(3)C→D的化学方程式为______________。
(4)C + E→ F的化学方程式为 ______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com