
【题目】下列分子中的所有碳原子不可能位于同一平面上的是
①![]() ②
②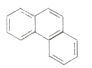 ③
③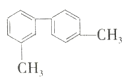 ④
④ ⑤
⑤![]()
A.②③B.①④
C.①②④D.①⑤
【答案】B
【解析】
①丁基中的4个碳原子构成空间四面体结构,所以该分子中所有碳原子不可能位于同一平面上,故①符合题意;
② 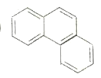 可以看成是相邻的两个苯环共有两个碳原子形成的,所以所有的碳原子位于同一平面上,故②不符合题意;
可以看成是相邻的两个苯环共有两个碳原子形成的,所以所有的碳原子位于同一平面上,故②不符合题意;
③ 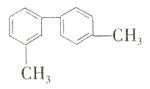 可以看成是一个甲苯中的甲基间位碳原子与另一个甲苯中的甲基对位碳原子相连形成的,每个甲苯中的所有碳原子一定共面,所以该分子中的所有碳原子可能位于同一平面上,故③不符合题意;
可以看成是一个甲苯中的甲基间位碳原子与另一个甲苯中的甲基对位碳原子相连形成的,每个甲苯中的所有碳原子一定共面,所以该分子中的所有碳原子可能位于同一平面上,故③不符合题意;
④ 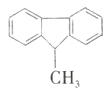 分子中含有两个苯环,每个苯环上的碳原子一定共面,但是甲基碳原子以及甲基相连的碳原子是烷烃的结构,一定不会共面,该分子中的所有碳原子不肯位于同一平面上,故④符合题意;
分子中含有两个苯环,每个苯环上的碳原子一定共面,但是甲基碳原子以及甲基相连的碳原子是烷烃的结构,一定不会共面,该分子中的所有碳原子不肯位于同一平面上,故④符合题意;
⑤CH3CH=CHCH3为烯烃结构,乙烯中的六个原子公平面,该分子可看成两个甲基取代乙烯中的两个氢原子,该分子中四个碳原子位于同一平面上,故⑤不符合题意。
答案选B。


科目:高中化学 来源: 题型:
【题目】NiCl2是化工合成中最重要的镍源,在实验室中模拟工业上以金属镍废料(含Fe、Al等杂质)为原料生产NiCl2的工艺流程如下:

下表列出了相关金属离子生成氢氧化物沉淀的pH
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Ni(OH)2 |
开始沉淀的pH | 2.1 | 6.5 | 3.7 | 7.1 |
沉淀完全的pH | 3.3 | 9.7 | 4.7 | 9.2 |
(1)为了提高镍元素的浸出率,在“酸浸”时可采取的措施有__________(写一条即可)。
(2)加入H2O2时发生主要反应的离子方程式为__________。
(3)“调pH”时,控制溶液pH的范围为__________。
(4)“沉镍”过程中,若滤液A中c(Ni2+)=1.0mol/L,欲使100mL该滤液中的Ni2+沉淀完全[即溶液中c(Ni2+)≤1.0×10-5],则需用托盘天平称取Na2CO3固体的质量至少为_____g。(已知Ksp(NiCO3)=6.5×10-6,忽略溶液体积的变化)
(5)流程中由溶液得到NiCl2·6H2O的实验操作步骤依次为______、过滤、洗涤、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的某磁黄铁矿(主要成分FexS,S为-2价)与100mL盐酸恰好完全反应(矿石中其他成分不与盐酸反应),生成3.2g硫单质、0.4molFeCl2和一定量H2S气体,且溶液中无Fe3+。则下列说法正确的是( )
A.该盐酸的物质的量浓度为4.0mol·L-1
B.该磁黄铁矿FexS中,Fe2+与Fe3+的物质的量之比为2:1
C.生成的H2S气体在标准状况下的体积为8.96L
D.该磁黄铁矿中FexS的x=0.85
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某元素,它们之间具有如下转化关系:甲![]() 乙
乙![]() 丙。下列有关物质的推断不正确的是
丙。下列有关物质的推断不正确的是![]()
A.若甲为![]() ,则丙可能为
,则丙可能为![]()
B.若涉及反应均为氧化还原反应,则甲可能为![]()
C.若涉及反应均为氧化还原反应,则丁可能为![]()
D.若甲为![]() 溶液,则丁可能是NaOH溶液
溶液,则丁可能是NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 表示阿伏加德罗常数,下列说法正确的是
表示阿伏加德罗常数,下列说法正确的是![]()
A.标准状况下,等体积的水和![]() ,含有的氧原子数目为1:2
,含有的氧原子数目为1:2
B.含有![]() 个阴离子的
个阴离子的![]() 与足量水反应,转移电子数为
与足量水反应,转移电子数为![]()
C.向含有![]() 的溶液中通入适量氯气,当有
的溶液中通入适量氯气,当有![]() 个
个![]() 被氧化时,共转移电子数为
被氧化时,共转移电子数为![]()
D.一个NO分子质量为![]() ,一个
,一个![]() 分子质量是
分子质量是![]() ,则
,则![]() 个
个![]() 的质量为
的质量为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄鸣龙是我国著名化学家,利用“黄鸣龙反应”合成一种环己烷衍生物的路线如下:

已知:①R—Cl![]() R—COOH
R—COOH
②![]()
![]() R1CH2R2
R1CH2R2
③RCOOR1+R2CH2COOR3 ![]()
 +R1OH
+R1OH
(1)A 可与NaHCO3 溶液反应,其结构简式是____________。B 中含有的官能团是─COOH 和______________。
(2)D 的结构简式是_______________。
(3)D→E 反应会生成副产物 Y(分子式为 C17H32O6),生成 Y 的化学方程式是_______。
(4)E→F 为两步连续氧化反应,中间产物 X 可发生银镜反应,X 的结构简式是____。
(5)H 的结构简式是________________。
(6)I 的分子式为 C5H8O2,能使Br2 的 CCl4 溶液褪色,H→J 的反应类型是________。
(7)由K 经两步反应可得到化合物 M,转化路线如下:
![]()
环己烷的空间结构可如图1或图2表示,请在图3中将M 的结构简式补充完整:____________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象所得到的结论正确的是![]()
![]()
选项 | 实验操作 | 实验现象 | 结论 |
A | 向足量含KSCN的 | 溶液变黄 | 还原性:Fe2+>Br- |
B | 向2mL浓度为 | 开始出现白色沉淀,后出现黄色沉淀 |
|
C | 取等质量的Al和Fe,分别与足量的稀硫酸反应 | Al产生的氢气多 | 金属性: |
D | 向苯酚浊液中滴加饱和 | 浊液变澄清 | 酸性:苯酚 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作中,能使电离平衡H2O![]() H++OH-,向右移动且溶液呈酸性的是 ( )
H++OH-,向右移动且溶液呈酸性的是 ( )
A.向水中加入NaHSO4溶液
B.向水中加入Al2(SO4)3固体
C.向水中加入Na2CO3溶液
D.将水加热到100℃,使pH=6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等离子。利用常用的酸、碱和工业生产中废铁屑,设计如下工艺流程,从废水中回收金,并生产一定量的铁红和氧化铜。下列说法不正确的是
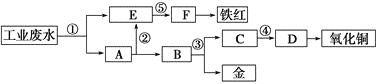
A.标号①②③处发生的反应均为氧化还原反应
B.标号③处加入的相应物质是稀硝酸
C.标号①处发生的离子反应最多有三个
D.铁红的化学式为Fe2O3,工业上常用作红色颜料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com