
| A、18 | B、20 | C、22 | D、24 |
| 0.2mol×(5-2) |
| 1 |


 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源: 题型:
| A、称量时将NaOH固体时用的砝码生锈 |
| B、将称量的NaOH固体置露在空气的时间过长 |
| C、选用的容量瓶内有少量的蒸馏水 |
| D、在烧杯中溶解NaOH后,立即将所得溶液注入容量瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
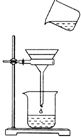 已知粗盐中含有泥沙,硫酸钠、氯化钙杂质,在进行提纯的过程中,某学生设计了如图所示的实验操作.回答下列问题:
已知粗盐中含有泥沙,硫酸钠、氯化钙杂质,在进行提纯的过程中,某学生设计了如图所示的实验操作.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.8g |
| B、1.6ag |
| C、(2a-3.2)g |
| D、(2a-1.6)g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯 乙醛 |
| B、乙炔 乙二醇 |
| C、甲烷 甲醇 |
| D、甲烷 乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、a<b | B、a=b |
| C、a>b | D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、44.8 L氟化氢气体分解成22.4 L的氢气和22.4 L的氟气吸收270 kJ热量 |
| B、1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量大于270 kJ |
| C、相同条件下,1mol氢气与1mol氟气的能量总和高于2mol氟化氢气体的能量 |
| D、2mol H-F键的键能比1mol H-H键和1mol F-F键的键能之和大270 kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com