
【题目】已知:CH4(g)+2H2S(g)![]() CS2(g)+4H2(g)。向恒容密闭容器中充入0.1 mol CH4和0.2 mol H2S,不断升高温度,测得平衡时体系中各物质的物质的量分数与温度的关系如下图所示:
CS2(g)+4H2(g)。向恒容密闭容器中充入0.1 mol CH4和0.2 mol H2S,不断升高温度,测得平衡时体系中各物质的物质的量分数与温度的关系如下图所示:
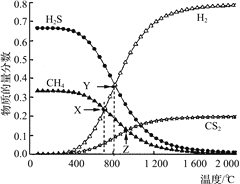
下列说法正确的是( )
A. 该反应的ΔH<0
B. X点CH4的转化率为20%
C. X点与Y点容器内压强比为51∶55
D. 维持Z点温度,向容器中再充入CH4、H2S、CS2、H2各0.1 mol时v(正)<v(逆)
【答案】BD
【解析】A. 由图可知升温平衡右移,所以该反应的ΔH>0,故A错误;B. X点,n(CH4)=n(H2),消耗CH4的物质的量n丿(CH4)=n(H2)/4= n(CH4)/4,所以X点CH4的转化率为20%,故B正确;C. X点容器内气体物质的量为(0.3+2×0.02)mol=0.34mol,Y点,n(H2S)=n(H2),消耗H2S的物质的量n丿(H2S)=n(H2)/2=n(H2S)/2,所以消耗H2S 0.1mol,此时容器内气体物质的量为(0.3+0.1)mol=0.4mol,X点与Y点容器内压强比等于气体物质的量比为17∶20,故C错误; D. 设容器体积为V,Z点,n(CH4)=n(CS2),甲烷转化一半,n(H2)=0.2mol,n(H2S)=0.2mol,平衡常数K=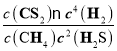 =
=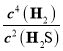 =c2(H2),向容器中再充入CH4、H2S、CS2、H2各0.1 mol时,n(CH4)=n(CS2),n(H2)=0.3mol,n(H2S)=0.3mol,浓度商Q=
=c2(H2),向容器中再充入CH4、H2S、CS2、H2各0.1 mol时,n(CH4)=n(CS2),n(H2)=0.3mol,n(H2S)=0.3mol,浓度商Q= =
=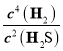 =c2(H2)>K,所以v(正)<v(逆),故D正确。故选BD。
=c2(H2)>K,所以v(正)<v(逆),故D正确。故选BD。


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案科目:高中化学 来源: 题型:
【题目】在500℃时,把0.3mol SO2和0.2mol O2充入一个体积为10L并盛有V2O5(催化剂)的真空密闭容器中,保持温度不变,经2min后,容器内的压强不再变化,此时容器内压强减小20%。下列说法正确的是( )
A.该温度下此反应的平衡常数K=400
B.其他条件不变,再充入0.3mol SO2和0.2mol O2平衡时,SO2的体积分数增大
C.平衡时,SO2的转化率为95%
D.前2min SO2的平均反应速率0.02mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA,下列说法正确的是( )
A. 用惰性电极电解1 L 1mol/L CuSO4溶液,阴极得到的铜原子的数目一定为NA
B. 将2.3g钠投入到100ml 0.8mol/L的稀盐酸中,完全反应后可得到H2的数目为0.01NA
C. 1molCl2溶于水后溶液中Cl2、HClO、ClO-、Cl-四种粒子总数为2NA
D. 标准状况下,2molNa2O2与44.8LSO2完全反应,转移的电子数目为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是( )
A. 无色透明溶液中: Ca2+、Cu2+、Br-、Cl-
B. 能使酚酞变红的溶液中: K+、Na+、CO![]() 、AlO
、AlO![]()
C. c(ClO-)=1mol·L-1的溶液中: Fe2+、Al3+、NO![]() 、I-
、I-
D. ![]() =0.1 mol·L-1的溶液中: NH
=0.1 mol·L-1的溶液中: NH![]() 、Mg2+、SO
、Mg2+、SO![]() 、CH3COO-
、CH3COO-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1L的密闭容器中通入2molNH3,在一定温度下发生下列反应:2NH3![]() N2+3H2,达到平衡时,容器内N2的百分含量为a%。若维持容器的体积和温度都不变,分别通入下列初始物质,达到平衡时,容器内N2的百分含量也为a%的是( )
N2+3H2,达到平衡时,容器内N2的百分含量为a%。若维持容器的体积和温度都不变,分别通入下列初始物质,达到平衡时,容器内N2的百分含量也为a%的是( )
A. 3molH2+2molN2 B. 2molNH3+1molN2
C. 2molH2+3molN2 D. 0.1molNH3+0.95molN2+2.85molH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LED产品的使用为城市增添色彩。右图是氢氧燃料电池驱动LED发光的一种装置示意图。下列有关叙述正确的是( )
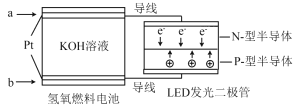
A. 该装置将化学能最终转化为电能
B. b处为电池正极,发生还原反应
C. a处通入O2
D. 通入O2的电极上发生的电极反应为O2 +4H+ +4e–=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸锰铵晶体可用作织物和木材加工的防火剂等。由二氧化锰等作原料制取硫酸锰铵晶体步骤如下:
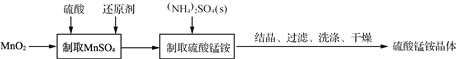
(1)实验前,需称量MnO2的质量,这是因为____________________________。
(2) “制取MnSO4”时,可用C6H12O6(葡萄糖)、H2C2O4(草酸)等物质作还原剂。
①用C6H12O6作还原剂(被氧化为CO2)时,发生反应的n(MnO2)/n(C6H12O6)=________。
②用H2C2O4作还原剂,发生反应的化学方程式为____________________________。
(3)一种测定硫酸锰铵晶体[设为: (NH4)xMny(SO4)z·wH2O]组成的方法如下:
①称取一定量的硫酸锰铵晶体配成250 mL溶液A。
②取25.00 mL溶液A加入足量的BaCl2溶液得BaSO4 0.512 6 g。
③另取25.00 mL溶液A加入10 mL 20%的中性甲醛溶液,摇匀、静置5 min[4NH![]() +6HCHO===3H++6H2O+(CH2)6N4H+,滴定时,1 mol(CH2)6N4H+与1 mol H+相当],加入1~2滴酚酞溶液,用0.100 0 mol·L-1 NaOH标准溶液滴定至终点(在该过程中Mn2+不沉淀),消耗NaOH溶液22.00 mL。
+6HCHO===3H++6H2O+(CH2)6N4H+,滴定时,1 mol(CH2)6N4H+与1 mol H+相当],加入1~2滴酚酞溶液,用0.100 0 mol·L-1 NaOH标准溶液滴定至终点(在该过程中Mn2+不沉淀),消耗NaOH溶液22.00 mL。
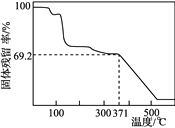
④取一定量样品在空气中加热,样品的固体残留率(固体样品的剩余质量/固体样品的起始质量×100%)随温度的变化如右图所示(样品在371 ℃时已完全失去结晶水)。根据以上实验数据计算确定硫酸锰铵晶体的化学式(写出计算过程)。__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在同一溶液中一定能大量共存的是( )
A. 含大量Ba2+的溶液中:Cl-、K+、SO![]() 、CO
、CO![]()
B. 含大量H+的溶液中:Mg2+、Na+、CO![]() 、SO
、SO![]()
C. 含大量OH-的溶液中:K+、NO、SO![]() 、Cu2+
、Cu2+
D. 含大量Na+的溶液中:H+、K+、SO![]() 、NO
、NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里需用480mL0.1mol/L的硫酸铜溶液,现选用合适的容量瓶进行配制,以下操作正确的是
A.称取7.68g硫酸铜,配成500mL溶液
B.称取8.0g硫酸铜,加入500mL水
C.称取12.5g胆矾(CuSO4·5H2O)配成500mL溶液
D.称取12.0g胆矾(CuSO4·5H2O)配成500mL溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com