
【题目】将2molI2(g)和1molH2置于某2L密闭容器中,在一定温度下发生反应:I2(g)+H2(g)![]() 2HI(g) ΔH<0,并达平衡,HI的体积分数φ(HI)随时间变化如下图中曲线(Ⅱ)所示.
2HI(g) ΔH<0,并达平衡,HI的体积分数φ(HI)随时间变化如下图中曲线(Ⅱ)所示.

(1)达平衡时,I2(g)的物质的量浓度为 .
(2)若改变反应条件下,在甲条件下ω(HI)的变化如图曲线(I)所示,在乙条件下ω(HI)的变化如图曲线(III)所示。则甲条件可能是 (填入下列条件的序号。下同),乙条件可能是 。
①恒温条件下,扩大反应容器体积
②恒容条件下,降低温度
③恒温条件下,缩小反应容器体积
④恒容条件下,升高温度
⑤恒温恒容条件下,加入适当催化剂
(3)若保持温度不变,在另一相同的2L密闭容器中加入a mol I2(g)、b mol H2和c mol HI(a、b、c 均大于0),发生反应,达平衡时,HI的体积分数仍为0.60,则a、b、c的关系是 。
【答案】(1)0.55mol/L;(2)③⑤;①;(3)2a-c=4b
【解析】
试题分析:(1)碘的初始浓度=![]() =1.0mol/L,该反应前后气体体积不变,平衡时,HI的体积分数为0.6,则n(HI)=3mol×0.6=1.8mol,c(HI)=
=1.0mol/L,该反应前后气体体积不变,平衡时,HI的体积分数为0.6,则n(HI)=3mol×0.6=1.8mol,c(HI)=![]() =0.9mol/L,根据I原子守恒得c(HI)+2c(I2)=1mol/L×2,c(I2)=
=0.9mol/L,根据I原子守恒得c(HI)+2c(I2)=1mol/L×2,c(I2)=![]() mol/L=0.55molL-1,故答案为:0.55molL-1;
mol/L=0.55molL-1,故答案为:0.55molL-1;
(2)该反应是一个反应前后气体体积不变的可逆反应,改变条件时,该反应中HI的体积分数不变,说明改变体积平衡不移动,改变条件时到达平衡的时间缩短,说明加快反应速率,改变的条件可能是增大压强、加入催化剂,故选③⑤;
若保持温度不变,在另一个相同的2L密闭容器中加入a mol I2(g)、b mol H2(g)和c mol HI(a、b、c均大于0),发生反应,达平衡时,HI的体积分数仍为0.6,与原来的平衡是等效平衡,恒温恒容,前后气体体积不变化,按化学计量数转化到左边,满足与原来加入的反应物物质的量比例相等即可;
对于反应 I2(g)+H2(g) ![]() 2HI(g);
2HI(g);
开始(mol): a b c
变化(mol): ![]() c
c ![]() c c
c c
平衡(mol):a+![]() c b+
c b+![]() c 0
c 0
则(a+![]() c ):( b+
c ):( b+![]() c)=2:1,所以2a-c=4b,故答案为:2a-c=4b。
c)=2:1,所以2a-c=4b,故答案为:2a-c=4b。


科目:高中化学 来源: 题型:
【题目】对于固定体积的密闭容器中进行的气体反应可以说明A(g) + B(g)![]() C(g)+D(g)在恒温下已达到平衡的是
C(g)+D(g)在恒温下已达到平衡的是
A.反应容器的压强不随时间而变化
B.A气体和B气体的生成速率相等
C.A、B、C三种气体的生成速率相等
D.反应混合气体的密度不随时间而变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1451.6kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH=-566.0kJ/mol
(1)写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式_______________
(2)某小组根据甲醇燃烧的反应原理,设计如图所示的电池装置:
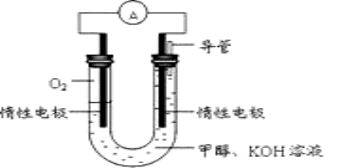
该电池正极的电极反应式____________________
工作一段时间后,测得溶液的pH______________(填增大、减小或不变),则该电池总反应的离子方程式__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将由NaOH、BaCl2、Al2(SO4)3三种固体组成的混合物溶于足量的水中,充分溶解后,向混合溶液中滴加1mol·L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的质量关系如图所示。下列有关判断正确的是( )

A.AB段发生反应的离子方程式为Ba2++SO42-=BaSO4↓
B.BC段发生反应的离子方程式为H++OH-=H2O
C.D点表示的沉淀的化学式为Al(OH)3
D.E点时溶液中含有大量的AlO2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.请回答:
(1)Na2O2的电子式 。
(2)除去FeCl3中少量FeCl2,除杂过程涉及的化学反应方程式 。
(3)往饱和Na2CO3溶液中通入CO2气体,溶液中出现白色浑浊,写出该反应的离子方程式 。
(4)双氧水能使酸性高锰酸钾溶液褪色,请完成以下相关反应的离子方程式:
( )MnO4-+( )H2O2+ =( )Mn2++( )H2O+ 。
Ⅱ.无机化合物A 和NaH都是重要的还原剂,遇水都强烈反应。一定条件下,2.40g NaH与气体B反应生成3.90g化合物A和 2.24L(已折算成标准状况)的H2。已知气体B可使湿润红色石蕊试纸变蓝。已知:NH3+ NH3=NH4++NH2-
请回答下列问题:
(1)A的化学式是 。
(2)A与足量盐酸发生非氧化还原反应的化学方程式 。
(3)在高温下氢化钠(NaH)可将四氯化钛(TiC14)还原成金属钛,该反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[实验化学]对氨基苯磺酸是制取染料和一些药物的重要中间体,可由苯胺磺化得到。
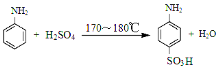
已知:100 mL水在20℃时可溶解对氨基苯磺酸1.08 g,在100℃时可溶解6.67 g。
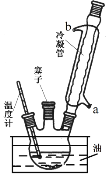
实验室可用苯胺、浓硫酸为原料,利用右图所示实验装置合成对氨基苯磺酸。实验步骤如下:步骤1:在一个250 mL三颈烧瓶中加入10 mL苯胺及几粒沸石,将三颈烧瓶放在冰水中冷却,小心地加入18 mL浓硫酸。在三颈烧瓶的两个瓶口上分别装冷凝管、温度计,另一个没有使用的瓶口用塞子塞紧。将三颈烧瓶置于油浴中缓慢加热至170~180℃,维持此温度2~2.5小时。
步骤2:将反应产物冷却至约50℃后,倒入盛有100 mL冷水的烧杯中,用玻璃棒不断搅拌,促使对氨基苯磺酸晶体析出。用该烧杯中的少量冷水将烧瓶内残留的产物冲洗到烧杯中,抽滤,用少量冷水洗涤,得到对氨基苯磺酸粗产品。
步骤3:将粗产品用沸水溶解,冷却结晶,抽滤,收集产品,晾干可得纯净的对氨基苯磺酸。
(1)实验装置中冷凝管由 处(填“a”或“b”)通入冷凝水。
(2)步骤1油浴加热的优点有 。
(3)步骤2中用玻璃棒不断搅拌可促使对氨基苯磺酸晶体析出的理由是 ,用少量冷水洗涤的目的是 。
(4)步骤2和3均进行抽滤操作,在抽滤完毕停止抽滤时,应注意先拆下连接泵和吸滤瓶的橡皮管,然后关闭水龙头,其目的是 。
(5)步骤3中若溶液颜色过深,可用 进行脱色处理。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A.用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3-=Ag++NO↑+H2O
B.碳酸钙粉末加入醋酸溶液中:CaCO3+2H+=Ca2++CO2↑+H2O
C.Ca(OH)2溶液与过量NaHCO3溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
D.电解饱和NaCl溶液:2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将甲酸和氢氧化钠溶液混合,所得溶液pH=7,则此溶液中( )
A. c(HCOO-)>c(Na+) B. c(HCOO-)<c(Na+)
C. c(HCOO-)=c(Na+) D. 无法确定c(HCOO-)与c(Na+)的关系
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com