
����Ŀ��1942 �꣬�ҹ�����ר�Һ�°��� NaCl��NH3��CO2 ��Ϊԭ�����Ƶ� NaHCO3��������������� �����������Ƽ��Ϊ�����Ƽҵ������ͻ�����ס��йط�Ӧ�Ļ�ѧ����ʽ���£�
NH3��CO2��H2O=NH4HCO3 ��
NH4HCO3��NaCl=NaHCO3����NH4Cl ��
2NaHCO3![]() Na2CO3��CO2����H2O
Na2CO3��CO2����H2O
(1)�������Ƽ���Ѻϳɰ��ʹ������ֲ�Ʒ������������д����ҵ�ϳɰ��Ļ�ѧ��Ӧ����ʽ_______
(2)̼������뱥��ʳ��ˮ��Ӧ��������̼�����ƾ����ԭ����_______��
a��̼������������ˮ
b��̼�����������ֽ�
c��̼�����Ƶ��ܽ����Խ�С����������Һ�����Ƚᾧ����
(3)ij̽���С����������Ƽ�ԭ�������Ʊ�̼�����ƣ�ͬѧ�ǰ�������Ƶķ�������ʵ�顣
��һλͬѧ����������̼����ͨ�뺬���ı���ʳ��ˮ���Ʊ�̼�����ƣ�ʵ��װ����ͼ��ʾ(ͼ�мг֡��̶��õ�����δ����)��
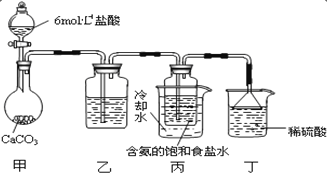
��ش�
��д�����з�����Ӧ�����ӷ���ʽ_______��
����װ���е��Լ���_______��
��ʵ���������� NaHCO3 ����IJ�����_______ (��������������)��
�ڶ�λͬѧ������ͼװ�ý���ʵ��(����װ��δ����)��
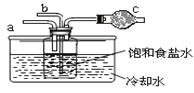
��Ϊ��߶�����̼�ڴ˷�Ӧ��Һ�б����յij̶ȣ�ʵ��ʱ�����ȴ� a ��ͨ��_______���壬�ٴ�b ����ͨ��_______���塣
��װ�� c �е��Լ�Ϊ_______(ѡ����ĸ)��
e����ʯ�� f.��Ũ���� g����ˮ�Ȼ���
���𰸡�N2 + 3H2![]() 2NH3 c CaCO3 + 2H+= Ca2++ H2O + CO2�� ����̼��������Һ ���� NH3(��) CO2 (������̼) g
2NH3 c CaCO3 + 2H+= Ca2++ H2O + CO2�� ����̼��������Һ ���� NH3(��) CO2 (������̼) g
��������
(1)��ҵ�ϳɰ���Ӧ������N2��H2�ڸ��¡���ѹ��������������NH3��
(2)a��̼������������ˮ��
b��̼�����ƹ�̬ʱ�����ֽ⣬��ˮ��Һ�����Ȳ��ֽ⣻
c��̼�����Ƶ��ܽ����Խ�С���ᾧ��������ʹƽ���������﷽���ƶ���
(3)��һλͬѧ����������̼����ͨ�뺬���ı���ʳ��ˮ���Ʊ�̼�����ƣ�
��װ���У�CaCO3�����ᷴӦ��CO2���壬��CO2�л���HCl�����м��뱥��NaHCO3��Һ���Գ�ȥCO2�е�HCl���ڱ�װ���У�CO2ͨ�뺬���ı���ʳ��ˮ�У�����NaHCO3��NH4Cl����װ������������δ��ӦCO2�ݳ���NH3��
�ڶ�λͬѧ������ͼװ�ý���ʵ��(����װ��δ����)��
����CO2��ˮ�е��ܽ�Ȳ�������Ӧ��ͨNH3����ͨCO2�����������δ��Ӧ��NH3��
(1) ��ҵ�ϳɰ���Ӧ������N2��H2�ڸ��¡���ѹ��������������NH3����Ӧ����ʽN2 + 3H2![]() 2NH3����Ϊ��N2 + 3H2
2NH3������N2 + 3H2![]() 2NH3��
2NH3��
(2) a��̼������������ˮ��a�������⣻
b��̼�����ƹ�̬ʱ�����ֽ⣬�Ժ�°��ƼӦ������Ӱ�죬b�������⣻
c��̼�����Ƶ��ܽ����Խ�С���ᾧ��������ʹƽ���������﷽���ƶ����Ӷ�ʹNaHCO3�ᾧ������c�������⣻
��ѡc��
(3) ��һλͬѧ����������̼����ͨ�뺬���ı���ʳ��ˮ���Ʊ�̼�����ƣ�
�ټ���CaCO3�����ᷴӦ��CO2���壬���ӷ���ʽΪCaCO3 + 2H+= Ca2++ H2O + CO2������Ϊ��CaCO3 + 2H+= Ca2++ H2O + CO2����
����װ�õ������dz�ȥCO2�е�HCl�����Լ��뱥��NaHCO3��Һ����Ϊ������̼��������Һ��
��ʵ���������� NaHCO3�ᾧ�����������˹�����Һ��IJ����ǹ��ˣ���Ϊ�����ˣ�
�ڶ�λͬѧ������ͼװ�ý���ʵ��(����װ��δ����)��
������CO2��ˮ�е��ܽ�Ȳ�������Ӧ��ͨNH3����ͨCO2������ a ��ͨ��NH3(��)���壬�ٴ�b ����ͨ��CO2 (������̼)���壻��Ϊ��NH3(��)��CO2 (������̼)��
��e����ʯ�ң����������������ƵĻ�����������NH3��e�������⣻
f.��Ũ�����Һ̬�����ܷ��ڸ�����ڣ�f�������⣻
g����ˮ�Ȼ��Ƴʹ�̬���ܹ����ڸ�����ڣ���������NH3��g�������⣻
��ѡg��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ѡ�������������ͭ�Ƚ������仯�����ڹ�ҵ������Ҫ��;��
(1)�����Ͻ�����ϵ����Ͻ�Ĵ������úϽ���з����¶ȵ͡��۸����е��ŵ㡣
��Ti�Ļ�̬ԭ�Ӽ۵����Ų�ʽΪ________��
��Fe�Ļ�̬ԭ�ӹ���______�ֲ�ͬ�ܼ��ĵ��ӣ�
(2)�Ʊ�CrO2Cl2�ķ�ӦΪK2Cr2O7��3CCl4=2KCl��2CrO2Cl2��3COCl2����
��������ѧ����ʽ�зǽ���Ԫ�ص縺���ɴ�С��˳����_______��
��COCl2�����������������ĸ�����Ϊ______������ԭ�ӵ��ӻ���ʽΪ_______��
(3)NiO��FeO�ľ���ṹ�����Ȼ��Ƶľ���ṹ��ͬ������Ni2����Fe2�������Ӱ뾶�ֱ�Ϊ6.9��10��2 nm��7.8��10��2 nm�����۵㣺NiO____(������������������������)FeO��
(4)����ij�ֵ��ʵľ���Ϊ���������ṹ��ԭ�ӵ���λ��Ϊ_______������ԭ�Ӱ뾶Ϊa nm����õ��ʵ��ܶ�Ϊ_______g/cm3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���� NA Ϊ�����ӵ�����������������ȷ����( )
A.��1mol�������Һ��H+������0.1NA
B.��״���£�22.4L�Ҵ��ķ�����ΪNA
C.28g��ϩ�ͱ�ϩ����̼�������ĿΪ4NA
D.1 mol�������ĵ�����Ϊ10NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������1807�껯ѧ�Ҵ�ά�õ���������������Ƶ��ƣ�4NaOH�������� ![]() 4Na��O2����2H2O��������������������������������������Ҳ�Ƶ��ƣ���Ӧԭ��Ϊ3Fe��4NaOH��������
4Na��O2����2H2O��������������������������������������Ҳ�Ƶ��ƣ���Ӧԭ��Ϊ3Fe��4NaOH�������� ![]() Fe3O4��2H2����4Na���������й�˵����ȷ����
Fe3O4��2H2����4Na���������й�˵����ȷ����
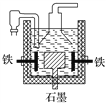
A. ������������������ƣ����������ĵ缫��ӦΪ2OH����2e��===H2����O2��
B. ���������˷�����ԭ�����������Ļ�ԭ�Ա���ǿ
C. ����ά������������˷��Ƶõ������ƣ�������Ӧ��ת�Ƶĵ�������Ҳ��ͬ
D. Ŀǰ��ҵ�ϳ��õ�������Ȼ��Ʒ�����������ͼ����������ʯīΪ��������Ϊ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ߴ���������Ϊ�ϳ���������Ԫ�������ϵ�ԭ�ϣ���ҵ�Ͽ�����Ȼ�������̷������̿���Fe��Al��Mg��Zn��Ni��Si��Ԫ�أ��Ʊ�����������ͼ��ʾ���ش��������⣺

��ؽ�������[c0(Mn+)=0.1 mol��L1]�γ��������������pH��Χ���£�
�������� | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
��ʼ������pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
������ȫ��pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
��1��������1������S��__________________________��д�����ܽ����ж������������̷�Ӧ�Ļ�ѧ����ʽ____________________________________________________��
��2����������������������MnO2�������ǽ�________________________��
��3������pH��������������Һ��pH��ΧӦ����Ϊ_______~6֮�䡣
��4��������1����Ŀ���dz�ȥZn2+��Ni2+��������3������Ҫ�ɷ���______________��
��5��������2����Ŀ��������MgF2������ȥMg2+������Һ��ȹ��ߣ�Mg2+��������ȫ��ԭ����_____________________________________________________________________��
��6��д���������������ӷ���ʽ___________________________________________________��
��7����״��������Ԫ���Ͽ���Ϊ����ӵ���������ϣ��仯ѧʽΪLiNixCoyMn![]() ʱ��z=___________��
ʱ��z=___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Dz��ֶ�����Ԫ��ԭ�Ӱ뾶��ԭ�������Ĺ�ϵͼ��������˵������ȷ����( )
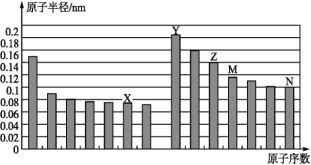
A.Z��N����Ԫ�ص����Ӱ뾶��ȣ����߽ϴ�
B.X��N����Ԫ�ص���̬�⻯����ȶ�����ȣ�ǰ�߽�ǿ
C.��X��M����Ԫ����ɵĻ����ﲻ�����κ��ᷴӦ��������ǿ�Ӧ
D.Z�����������ֱܷ��ܽ���Y�����������ˮ��Һ��N���⻯���ˮ��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴Ӧ 2NO2(g)![]() N2O4 (g)�����������ܱ������з�Ӧ���ﵽƽ��״̬�ı�־��
N2O4 (g)�����������ܱ������з�Ӧ���ﵽƽ��״̬�ı�־��
����λʱ�������� n mol N2O4 ��ͬʱ���� 2n mol NO2
����λʱ�������� n mol N2O4��ͬʱ���� 2n mol NO2
����������ƽ����Է����������ٸı��״̬
������������ɫ���ٸı��״̬
����NO2��N2O4�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ���ʵı�Ϊ2��1 ��״̬
A.�٢ܢ�B.�ڢ�C.�٢ۢ�D.�٢ڢۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)д�������л����ϵͳ������ṹ��ʽ
�� _____________________
_____________________
�� (CH3)2CH(CH2)3CH3 _____________________
��3,4-����-4-�һ�����_____________________
��2��3��4-��������_____________________
(2)д��C5H12 ��ͬ���칹�Ľṹ��ʽ����ϵͳ����������_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��8.34 g FeSO4��7H2O(��Է���������278)��Ʒ������ˮ���̵���������(��Ʒ�������¶ȱ仯������)����ͼ��ʾ������˵������ȷ����( )

A.�¶�Ϊ78 ��ʱ��������M�Ļ�ѧʽΪFeSO4��4H2O
B.ȡ����380 ��ʱ���õ���ƷP����������������650�棬�õ�һ�ֹ�������Q��ͬʱ��������ɫ�������ɣ�Q�Ļ�ѧʽΪFe2O3
C.�ڸ������������£�N�õ�P�Ļ�ѧ����ʽΪFeSO4��H2O![]() FeSO4��H2O
FeSO4��H2O
D.�¶�Ϊ159 ��ʱ����N�Ļ�ѧʽΪFeSO4��2H2O
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com