
ЁОЬтФПЁПВПЗжШѕЫсЕФЕчРыЦНКтГЃЪ§ШчБэЃК
ШѕЫс | HCOOH | HClO | H2CO3 | H2SO3 |
ЕчРыЦНКт ГЃЪ§ЃЈ25ЁцЃЉ | KaЃН1.77ЁС10Ѓ4 | KaЃН4.0ЁС10Ѓ8 | Ka1ЃН4.3ЁС10Ѓ7 Ka2ЃН4.7ЁС10Ѓ11 | Ka1ЃН1.54ЁС10Ѓ2 Ka2ЃН1.02ЁС10Ѓ7 |
ЃЈ1ЃЉЪвЮТЯТЂй0.1molЁЄL-1HCOONaЃЌЂк0.1molЁЄL-1NaClOЃЌЂл0.1molЁЄL-1Na2CO3ЃЌЂм0.1molЁЄL-1NaHCO3ШмвКЕФpHгЩДѓЕНаЁЕФЙиЯЕЮЊ_______________________ЁЃ
ЃЈ2ЃЉХЈЖШОљЮЊ0.1 molЁЄLЃ1ЕФNa2SO3КЭNa2CO3ЕФЛьКЯШмвКжаЃЌSO32-ЁЂCO32-ЁЂHSO3-ЁЂHCO3-ХЈЖШДгДѓЕНаЁЕФЫГађЮЊ_______________________ЁЃ
ЃЈ3ЃЉЯТСаРызгЗНГЬЪНе§ШЗЕФЪЧ___________ЃЈЬюзжФИЃЉЁЃ
A.2ClO-+H2O+CO2=2HClO+CO32-
B.2HCOOH+CO32-=2HCOO-+H2O+CO2Ёќ
C.H2SO3+=2HCOO-=2HCOOH+SO32-
D.Cl2+H2O+2CO32-=2HCO3-+Cl-+ClO-
ЃЈ4ЃЉФГЮТЖШЃЈTЁцЃЉЯТЕФШмвКжаЃЌcЃЈH+ЃЉ=10-xmolЁЄL-1ЃЌcЃЈHO-ЃЉ=10-ymolЁЄL-1ЃЌxгыyЕФЙиЯЕШчЭМЫљЪОЁЃ
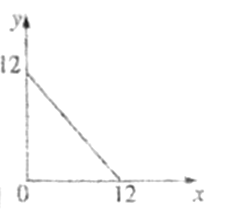
ЂйДЫЮТЖШЯТЃЌ0.01mol/LЕФNaOHШмвКжаЫЎЕчРыГіЕФOH-ХЈЖШЮЊ____________ЁЃ
ЂкдкДЫЮТЖШЯТЃЌ0.1molЁЄL-1ЕФNaHSO4ШмвКгы0.1molЁЄL-1ЕФBaЃЈOHЃЉ2ШмвКАДЯТБэжаМзЁЂввЁЂБћЁЂЖЁВЛЭЌЗНЪНЛьКЯЃК
Мз | вв | Бћ | ЖЁ | |
0.1molЁЄL-1ЕФBaЃЈOHЃЉ2 | 10 | 10 | 10 | 10 |
0.1molЁЄL-1ЕФNaHSO4 | 5 | 10 | 15 | 20 |
АДЖЁЗНЪНЛьКЯКѓЃЌЫљЕУШмвКЯд____________ЃЈЬюЁАЫсЁБЁАМюЁБЛђЁАжаЁБЃЉадЃЌаДГіАДввЗНЪНЛьКЯКѓЃЌЗДгІЕФРызгЗНГЬЪНЃК______________ЁЃАДМзЗНЪНЛьКЯКѓЃЌЫљЕУШмвКЕФpHЮЊ____________ЁЃ
ЁОД№АИЁПЂлЃОЂкЃОЂмЃОЂй cЃЈSO32-ЃЉЃОcЃЈCO32-ЃЉЃОcЃЈHCO3-ЃЉЃОcЃЈHSO3-ЃЉ BD 1ЁС10-10molЁЄL-1 жа Ba2ЃЋЃЋOHЃЃЋHЃЋЃЋSO42Ѓ=BaSO4Ё§ЃЋH2O 11
ЁОНтЮіЁП
ЃЈ1ЃЉМИжжЮяжЪЖМЪЧЧПМюШѕЫсбЮЃЌШмвКЯдМюадЃЌИљОнБэИёЪ§ОнЃЌЭЦГіЕчРыГіHЃЋФмСІЕФДѓаЁЪЧH2SO3>HCOOH>H2CO3>HSO3Ѓ>HClO>HCO3ЃЃЌРћгУбЮРрЫЎНтЕФЙцТЩЃЌЕУГіpHДгДѓЕНаЁЕФЙиЯЕЮЊNa2CO3>NaClO>Na2SO3>NaHCO3>HCOONa>NaHSO3ЃЌМДгаЂл>Ђк>Ђм>ЂйЃЛ
ЃЈ2ЃЉвРОнЫЎНтГЬЖШдНДѓЃЌШмвКжаЫсИљРызгХЈЖШдНаЁЃЌИљОн(1)ЕФЗжЮіЃЌЕУГіШмвКжаРызгХЈЖШЃКc(SO32Ѓ)>c(CO32Ѓ)>c(HCO3Ѓ)>c(HSO3Ѓ)ЃЛ
ЃЈ3ЃЉИљОнБэИёЪ§ОнЃЌЭЦГіЕчРыГіHЃЋФмСІЕФДѓаЁЪЧH2SO3>HCOOH>H2CO3>HSO3Ѓ>HClO>HCO3ЃЃЌ
AЁЂHClOЕчРыГіHЃЋФмСІЧПгкHCO3ЃЃЌвђДЫЗДгІЕФРызгЗНГЬЪНЮЊClOЃЃЋH2OЃЋCO2=HClOЃЋHCO3ЃЃЌЙЪAДэЮѓЃЛ
BЁЂHCOOHЕФЫсадЧПгкЬМЫсЃЌЗЂЩњ2HCOOHЃЋCO32Ѓ=2HCOOЃЃЋH2OЃЋCO2ЁќЃЌЙЪBе§ШЗЃЛ
CЁЂИљОнЕчРыГіHЃЋЧПШѕЃЌЭЦГіH2SO3ЃЋHCOOЃ=HCOOHЃЋHSO3ЃЃЌЙЪCДэЮѓЃЛ
DЁЂCl2ФмгыH2OЗДгІCl2ЃЋH2O![]() HClЃЋHClOЃЌгаПЩФмЗЂЩњCl2ЃЋH2OЃЋ2CO32Ѓ=2HCO3ЃЃЋClЃЃЋClOЃЃЌЙЪDе§ШЗЃЛ
HClЃЋHClOЃЌгаПЩФмЗЂЩњCl2ЃЋH2OЃЋ2CO32Ѓ=2HCO3ЃЃЋClЃЃЋClOЃЃЌЙЪDе§ШЗЃЛ
Д№АИбЁBDЃЛ
ЃЈ4ЃЉЂйИУЮТЖШЯТЕФЫЎЕФРызгЛ§ЮЊc(HЃЋ)ЁСc(OHЃ)=100ЁС10Ѓ12=10Ѓ12ЃЌДЫЮТЖШЯТЃЌ0.01molЁЄLЃ1ЕФNaOHШмвКжаЫЎЕчРыГіЕФc(OHЃ)=c(HЃЋ)=![]() =
=![]() =10Ѓ10molЁЄLЃ1ЃЛ
=10Ѓ10molЁЄLЃ1ЃЛ
Ђк10mL0.1molЁЄLЃ1Ba(OH)2гы20mL0.1molЁЄLЃ1NaHSO4ЛьКЯЃЌЗЂЩњЕФЗДгІЗНГЬЪНЮЊBa(OH)2ЃЋH2SO4=2H2OЃЋBaSO4Ё§ЃЋNa2SO4ЃЌШмвКЯджаадЃЛАДввЗНЪНЛьКЯЃЌЦфРызгЗНГЬЪНЮЊЃКBa2ЃЋЃЋOHЃЃЋHЃЋЃЋSO42Ѓ=BaSO4Ё§ЃЋH2OЃЛАДМзЗНЪНЛьКЯЃЌЗЂЩњРызгЗДгІЗНГЬЪНЮЊBa2ЃЋЃЋOHЃЃЋHЃЋЃЋSO42Ѓ=BaSO4Ё§ЃЋH2OЃЌЗДгІКѓШмвКжаn(OHЃ)=10ЁС10Ѓ3LЁС0.1molЁЄLЃ1ЁС2Ѓ5ЁС10Ѓ3LЁС0.1molЁЄLЃ1=1.5ЁС10Ѓ3molЃЌМДc(OHЃ)=![]() =0.1molЁЄLЃ1ЃЌpHЮЊ11ЁЃ
=0.1molЁЄLЃ1ЃЌpHЮЊ11ЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГЪЕбщаЁзщЭЌбЇАбаЁПщФОЬПдкОЦОЋЕЦЩЯЩежСКьШШЃЌбИЫйЭЖШыШШЕФХЈЯѕЫсжаЃЌЗЂЩњОчСвЗДгІЃЌЭЌЪБгаДѓСПКьзиЩЋЦјЬхВњЩњЃЌвКУцЩЯФОЬПбИЫйШМЩеЗЂГіССЙтЁЃОВщдФзЪСЯПЩжЊХЈЯѕЫсЗжНтВњЩњNO2КЭO2ЁЃЮЊСЫЬНОПЁАвКУцЩЯФОЬПбИЫйШМЩеЗЂГіССЙтЁБЕФдвђЃЌИУаЁзщЭЌбЇгУШчЭМзАжУЭъГЩвдЯТЪЕбщЃК
ађКХ | ЪЕбщI | ЪЕбщII |
МЏЦјЦПжаЫљЪЂЦјЬх | O2 | МгШШХЈЯѕЫс ВњЩњЕФЦјЬх |
ЯжЯѓ | ФОЬПбИЫйШМЩеЗЂГіССЙт | ФОЬПбИЫйШМЩеЗЂГіССЙт |
ЯТСаЫЕЗЈе§ШЗЕФЪЧ
A. ХЈЯѕЫсЗжНтВњЩњЕФV(NO2):V(O2)=1:1
B. КьзиЩЋЦјЬхЕФВњЩњБэУїФОЬПгыХЈЯѕЫсЗЂЩњСЫЗДгІ
C. ФмЪЙвКУцЩЯФОЬПбИЫйШМЩеЗЂГіССЙтЕФжївЊЦјЬхЪЧбѕЦј
D. вдЩЯЪЕбщВЛФмШЗЖЈЪЙвКУцЩЯФОЬПбИЫйШМЩеЗЂГіССЙтЕФжївЊЦјЬхвЛЖЈЪЧNO2
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПШчЭМЪЧl molН№ЪєУОКЭТБЫиЗДгІЕФЁїH(ЕЅЮЛЃКkJЁЄ molЃ1)ЪОвтЭМЃЌЗДгІЮяКЭЩњГЩЮяОљЮЊГЃЮТЪБЕФЮШЖЈзДЬЌЃЌЯТСабЁЯюжаВЛе§ШЗЕФЪЧ
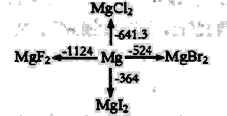
A.гЩЭМПЩжЊЃЌMgF2(s)ЃЋBr2(l)ЃНMgBr2(s)ЃЋF2(g)ЁїHЃНЃЋ600kJЁЄ molЃ1
B.MgI2гыBr2ЗДгІЕФЁїH<0
C.ЕчНтMgBr2жЦMgЪЧЮќШШЗДгІ
D.ЛЏКЯЮяЕФШШЮШЖЈадЫГађЃКMgI2>MgBr2>MgCl2>MgF2
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПТСШШЗДгІЪЧТСЕФвЛИіживЊаджЪЃЌИУаджЪгУЭОЪЎЗжЙуЗКЃЌВЛНіБЛгУгкКИНгИжЙьЃЌЖјЧвЛЙГЃБЛгУгквБСЖИпШлЕуЕФН№ЪєШчЗАЁЂИѕЁЂУЬЕШЁЃ
(l)ФГаЃЛЏбЇаЫШЄаЁзщЭЌбЇЃЌШЁДХадбѕЛЏЬњАДНЬВФжаЕФЪЕбщзАжУ(ШчЭМ)НјааТСШШЗДгІЃЌЯжЯѓКмзГЙлЁЃЪЙгУУОЬѕКЭТШЫсМиЕФФПЕФЪЧ___________ЁЃ
(2)ФГЭЌбЇШЁЗДгІКѓЕФЁАЬњПщЁБКЭЯЁЯѕЫсЗДгІжЦБИFe(NO3)3ШмвКЃЌЦфРызгЗНГЬЪНЮЊ__________ЃЌШмвКжаПЩФмКЌгаFe2ЃЋЃЌЦфдвђЪЧ___________ЃЛ
(3)ПЩЭЈЙ§KClOШмвКгыFe(NO3)3ШмвКЕФЗДгІжЦБИИпЬњЫсМи(K2FeO4)ЃЌШчЭМЫљЪОЪЧЪЕбщЪвФЃФтЙЄвЕжЦБИKClOШмвКзАжУЁЃвбжЊТШЦјКЭШШМюШмвКЗДгІЩњГЩТШЛЏМиКЭТШЫсМиКЭЫЎ

ЂйЪЂзАБЅКЭЪГбЮЫЎЕФBзАжУзїгУЮЊ______________ЃЛ
ЂкЗДгІЪБашНЋCзАжУжУгкРфЫЎдЁжаЃЌЦфдвђЮЊ___________ЃЛ
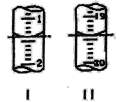
(4)ЙЄвЕЩЯгУЁАМфНгЕтСПЗЈЁБВтЖЈИпЬњЫсМиЕФДПЖШЃКгУМюадKIШмвКШмНт1.00g K2FeO4бљЦЗЃЌЕїНкpHЪЙИпЬњЫсИљШЋВПБЛЛЙдГЩбЧЬњРызгЃЌдйЕїНкpHЮЊ3ЁЋ4ЃЌгУ1.0 mol/LЕФNa2S2O3БъзМШмвКзїЮЊЕЮЖЈМСНјааЕЮЖЈ(2Na2S2O3ЃЋI2ЃНNa2S4O6ЃЋ2NaI)ЃЌЕэЗлзїжИЪОМСЃЌзАгаNa2S2O3БъзМШмвКЕФЕЮЖЈЙмЦ№ЪМКЭжеЕуЖСЪ§ШчЭМЫљЪОЃК
ЂйжеЕуIIЕФЖСЪ§ЮЊ_______mLЁЃ
ЂкдбљЦЗжаИпЬњЫсМиЕФжЪСПЗжЪ§ЮЊ_________ЁЃ[M(K2FeO4)ЃН198g/mol]
ЂлШєдкХфжЦNa2S2O3БъзМШмвКЕФЙ§ГЬжаЖЈШнЪБИЉЪгПЬЖШЯпЃЌдђЕМжТЫљВтИпЬњЫсМиЕФжЪСПЗжЪ§_______(ЬюЁАЦЋИпЁБЁЂЁАЦЋЕЭЁБЛђЁАЮогАЯьЁБ)ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПОнБЈЕРЃЌПЦбЇМввбОбажЦГіЪРНчЩЯзюБЁЕФВФСЯЁЊЁЊЬМФЄЦЌЃЌЦфКёЖШжЛгавЛИљЭЗЗЂЕФЖўЪЎЭђЗжжЎвЛЁЃШчЭМЫљЪОЃЌетжжЬМФЄЦЌаЮзДШчЗфГВЃЌЪЧгЩЬМдзгЙЙГЩЕФСљБпаЮЕЅдЊЯђЭтбгеЙЖјГЩЃЌЯТСагаЙиЬМФЄЦЌЕФЫЕЗЈжаЃЌе§ШЗЕФЪЧЃЈ ЃЉ
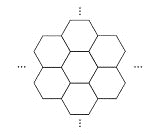
A. ЬМФЄЦЌЪєгквЛжжаТаЭЕФЛЏКЯЮя
B. ЬМФЄЦЌгыЪЏФЋЕФНсЙЙЯрЭЌ
C. ЬМФЄЦЌгыC60ЛЅЮЊЭЌЫивьаЮЬх
D. ЬМФЄЦЌдкбѕЦјжаЭъШЋШМЩеЕФВњЮяКЭЬМдкбѕЦјжаЭъШЋШМЩеЕФВњЮяВЛЭЌ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПШчЭМЪЧвЛжжзлКЯДІРэSO2ЗЯЦјЕФЙЄвеСїГЬ.ЯТСаЫЕЗЈе§ШЗЕФЪЧ( )
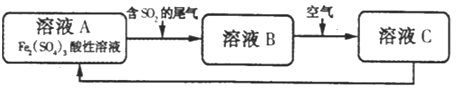
AЃЎЯђBШмвКжаЕЮМгKSCNШмвКЃЌШмвКПЩФмБфЮЊбЊКьЩЋ
BЃЎШмвКBзЊЛЏЮЊШмвКCЗЂЩњЕФБфЛЏЕФРызгЗНГЬЪНЮЊ4H+ + 2Fe2++O2=2Fe3++2H2OЃЌ
CЃЎШмвКЫсад:A>B>C
DЃЎМгбѕЛЏбЧЬњПЩвдЪЙШмвКCзЊЛЏЮЊШмвКA
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвЛжжгУВнЫсФрдќ(КЌ73.75ЃЅPbC2O4ЁЂ24.24ЃЅPbSO4)жЦБИPbCrO4ЕФЙЄвеСїГЬШчЯТЃК
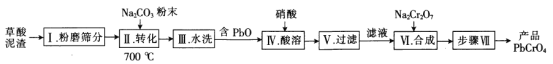
ЛиД№ЯТСаЮЪЬтЃК
вбжЊЃКЂйPbC2O4ЭъШЋЗжНтЕФЛЏбЇЗНГЬЪНЮЊ![]() ЁЃ
ЁЃ
ЂкPbCrO4ФбШмгкЫЎЁЃ
(1)ФрдќЁАЗлФЅЩИЗжЁБЕФФПЕФЪЧ___________________________________ЁЃ
(2)гУNa2CO3НЋPbSO4зЊЛЏЮЊPbCO3ЕФФПЕФЪЧ_______________________ЃЛШєдкЫЎШмвКжаНјаа![]() ЃЌИУЗДгІЕФЦНКтГЃЪ§K=______________________________________[вбжЊKSP(PbCO3)ЃН6.4ЁС10Ѓ14ЃЌKSP(PbSO4)ЃН1.6ЁС10Ѓ8]ЁЃ
ЃЌИУЗДгІЕФЦНКтГЃЪ§K=______________________________________[вбжЊKSP(PbCO3)ЃН6.4ЁС10Ѓ14ЃЌKSP(PbSO4)ЃН1.6ЁС10Ѓ8]ЁЃ
(3)ВНжшЂіЁАКЯГЩЁБЪБЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЮЊ____________________ЁЃ
(4)ЁАВНжшЂїЁБАќКЌЕФЪЕбщВйзїга___________________________________МАИЩдяЁЃ
(5)ФГЙЄГЇгУ10tИУВнЫсФрдќжЦБИPbCrO4ЃЌзюжеЕУЕН9.69tВњЦЗЃЌPbдЊЫиЕФзЊЛЏТЪЮЊ_______(ОЋШЗЕНаЁЪ§ЕуКѓ2ЮЛ)ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЗњЕФЕЅжЪМАКЌЗњЛЏКЯЮягУЭОЗЧГЃЙуЗКЁЃЛиД№ЯТСаЮЪЬтЃК
(1)BF3ГЃгУзїгаЛњЗДгІЕФДпЛЏМСЃЌЯТСаBдзгЕчзгХХВМЭМБэЪОЕФзДЬЌжаЃЌФмСПзюЕЭКЭзюИпЕФЗжБ№ЮЊ____________ЁЂ_______________ЁЃ(ЬюБъКХ)
(2)NH4HF2(ЗњЧтЛЏяЇ)ЙЬЬЌЪБАќКЌЕФзїгУСІга_______________(ЬюБъКХ)ЁЃ
a.РызгМќ b.![]() Мќ c.
Мќ c.![]() Мќ d.ЧтМќ
Мќ d.ЧтМќ
(3)гЩЗДгІ2F2+2NaOHЃНOF2+2NaF+H2OПЩжЦБИOF2ЁЃOF2ЕФПеМфЙЙаЭЮЊ___________ЃЌбѕдзгЕФдгЛЏЗНЪНЪЧ_____________________________
(4)CsFЪЧРызгОЇЬхЃЌЦфОЇИёФмПЩЭЈЙ§ЭМ(a)ЕФbornЃHaberбЛЗМЦЫуЕУЕНЁЃ
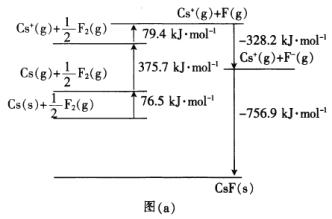
гЩЭМЃЈaЃЉПЩжЊЃЌCsдзгЕФЕквЛЕчРыФмЮЊ_______________________kJЁЄmolЃ1ЃЌFЃFМќЕФМќФмЮЊ________kJЁЄmolЃ1ЃЌCsFЕФОЇИёФмЮЊ________kJЁЄmolЃ1ЁЃ
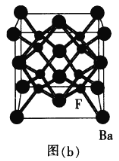
(5)BaF2ОЇАћЪЧвЛжжСМКУЕФЩСЫИОЇЬх[ШчЭМ(b)ЫљЪО]ЁЃBa2ЃЋЕФХфЮЛЪ§ЮЊ_________ИіЃЛвбжЊЦфУмЖШЮЊ![]() ЃЌдђBaF2ЕФОЇАћВЮЪ§ЮЊa=____________(ЩшNAЮЊАЂЗќМгЕТТоГЃЪ§ЕФЪ§жЕЃЌСаГіМЦЫуЪН) nmЁЃ
ЃЌдђBaF2ЕФОЇАћВЮЪ§ЮЊa=____________(ЩшNAЮЊАЂЗќМгЕТТоГЃЪ§ЕФЪ§жЕЃЌСаГіМЦЫуЪН) nmЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁППижЦЁЂжЮРэЕЊбѕЛЏЮяЖдДѓЦјЕФЮлШОЪЧИФЩЦДѓЦјжЪСПЕФживЊЗНЗЈЁЃЛиД№ЯТСагыЮэіВжЮРэгаЙиЕФЮЪЬтЃК
Ђё.(1)дкДпЛЏМСзїгУЯТЃЌМзЭщПЩЛЙдЕЊбѕЛЏЮяЃЌДгЖјДяЕНжЮРэЕЊбѕЛЏЮяЮлШОЕФФПЕФЁЃвбжЊЃКЂйCH4(g)ЃЋ4NO2(g)= 4NO(g)ЃЋCO2(g)ЃЋ2H2O(g)ЁЁІЄHЃНЃ574 kJЁЄmolЃ1ЃЛЂк4NO2(g)ЃЋ2N2(g)= 8NO(g)ЁЁІЄHЃНЃЋ586 kJЁЄmolЃ1ЁЃдђCH4(g)ЃЋ4NO(g)= 2N2(g)ЃЋCO2(g)ЃЋ2H2O(g)ЁЁІЄHЃН________ kJЁЄmolЃ1ЁЃ
(2)ЙЄвЕбЬЦјжаЕФЕЊбѕЛЏЮяПЩгУNH3ДпЛЏЛЙдЃЌЗДгІдРэШчЭМЫљЪОЁЃ

ЦфжаXЮЊвЛжжЮоЖОЕФЦјЬхЃЌдђNH3ДпЛЏЛЙдЕЊбѕЛЏЮяЕФЛЏбЇЗНГЬЪНЮЊ______ЁЃ
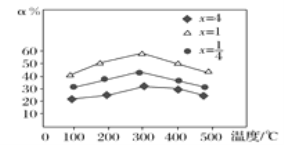
(3)гУNH3ДпЛЏЛЙдбЬЦјжаЕФЕЊбѕЛЏЮяЪБЃЌЕБ![]() ЃНxЃЌгУFeзїДпЛЏМСЪБЃЌдкNH3ГфзуЕФЬѕМўЯТЃЌВЛЭЌxжЕЖдгІЕФЭбЕЊТЪІС(БЛЛЙдЕФЕЊбѕЛЏЮяЕФАйЗжТЪ)ВЛЭЌЃЌдкВЛЭЌЮТЖШЯТЦфЙиЯЕШчЭМЫљЪОЃЌЕБxЃН_____ЪБЃЌЭбЕЊаЇЙћзюМбЃЌзюМбЕФЭбЕЊЮТЖШЪЧ____ ЁцЁЃ
ЃНxЃЌгУFeзїДпЛЏМСЪБЃЌдкNH3ГфзуЕФЬѕМўЯТЃЌВЛЭЌxжЕЖдгІЕФЭбЕЊТЪІС(БЛЛЙдЕФЕЊбѕЛЏЮяЕФАйЗжТЪ)ВЛЭЌЃЌдкВЛЭЌЮТЖШЯТЦфЙиЯЕШчЭМЫљЪОЃЌЕБxЃН_____ЪБЃЌЭбЕЊаЇЙћзюМбЃЌзюМбЕФЭбЕЊЮТЖШЪЧ____ ЁцЁЃ
Ђђ.(4)МзДМЪЧвЛжжТЬЩЋШМСЯЃЌМзДМЕФЙЄвЕКЯГЩЗНЗЈНЯЖрЃЌШчCO(g)ЃЋ2H2(g)![]() CH3OH(g)ЁЃдк2 LКуШнУмБеШнЦїжаГфШы1 mol COКЭ2 mol H2ЛьКЯдСЯЦјЃЌГфЗжЗДгІДяЕНЦНКтЃЌВтЕУЦНКтЪБЛьКЯЮяжаCH3OHЕФЬхЛ§ЗжЪ§гыбЙЧПЁЂЮТЖШЕФЙиЯЕШчЭМЫљЪОЁЃ
CH3OH(g)ЁЃдк2 LКуШнУмБеШнЦїжаГфШы1 mol COКЭ2 mol H2ЛьКЯдСЯЦјЃЌГфЗжЗДгІДяЕНЦНКтЃЌВтЕУЦНКтЪБЛьКЯЮяжаCH3OHЕФЬхЛ§ЗжЪ§гыбЙЧПЁЂЮТЖШЕФЙиЯЕШчЭМЫљЪОЁЃ
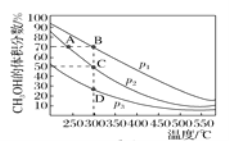
ЂйЭМжабЙЧПp1ЁЂp2ЁЂp3ЕФДѓаЁЙиЯЕЪЧ_______ЁЃ
ЂкCЕуЦНКтГЃЪ§KЃН___ЃЌAЁЂBЁЂDШ§ЕуЕФЦНКтГЃЪ§K(ЗжБ№гУKAЁЂKBЁЂKDБэЪО)ЕФДѓаЁЙиЯЕЪЧ_____ЁЃ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com