
【题目】下列物质有如下转化关系![]() 有的生成物未列出
有的生成物未列出![]() ,其中:D为碱,G为酸,金属甲在G 的浓溶液中会钝化;F的溶液中只含一种溶质.
,其中:D为碱,G为酸,金属甲在G 的浓溶液中会钝化;F的溶液中只含一种溶质.
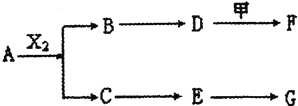
A、B、C、D、E均由Q、R、X、T四种短周期元素中的两种或三种组成,且Q、R、X、T原子序数依次增大;X的最外层电子数是电子层数的3倍;R和X相邻;Q和T同主族,Q为非金属元素,T为金属元素.则:
(1)X在周期表中的位置是 ______ ,R、X、T的原子半径从小到大的顺序为 ______ ![]() 用元素符号表示
用元素符号表示![]() ;
;
(2)A和G等物质的量反应产物的水溶液显 ______ 性,其原因用离子方程式表示为 ______ ;
(3)A和X2反应的化学方程式为 ______ ;
(4)pH均为12的D溶液和F溶液中,水电离出的c(OH-)之比为 ______ ;
(5)为保护环境,通过安装汽车尾气处理装置,使尾气中的E和CO反应转化为两种空气的成分,当反应转移1 mol电子时,生成的气体在标准状况下的总体积为 ______ L。
【答案】第二周期VIA族 O<N<Na 酸 H2O+NH4+H++NH3H2O 4NH3+5O2 ![]() 4NO+6H2O 1:1010,或10-10或10-10:1 14
4NO+6H2O 1:1010,或10-10或10-10:1 14
【解析】
X的最外层电子数是电子层数的3倍,应为O元素,R和X相邻,且原子序数小于R,则应为N元素,Q和T同主族,Q为非金属元素,T为金属元素,在元素周期表中只有H和Na符合,则Q为H元素,T为Na元素,题中信息“D为碱,金属甲在G的浓溶液中会钝化”,说明金属甲能与碱反应,则甲为Al,结合“A、B、C、D,E均由Q,R、X、T四种短周期元素中的两种或三种组成”可知G应为HNO3,则E为NO2,C为NO,A能与氧气反应生成NO,且含有N元素,应为NH3,则B为H2O,D为NaOH,F应为NaAlO2。
(1)X为氧元素,在周期表中的位置是:第二周期,ⅥA族,R为N,X为O,T为Na,原子半径从小到大的顺序为:O<N<Na;
(2)NH3和G(HNO3)等物质的量反应生成的产物为硝酸铵,为强酸弱碱盐,铵根离子水溶液水解呈酸性,水解方程式为H2O+NH4+H++NH3H2O;
(3)A(NH3)和X2(O2)反应的化学方程式为:4NH3+5O2 ![]() 4NO+6H2O;
4NO+6H2O;
(4)pH均为12的NaOH溶液和NaAlO2溶液中,水电离出的c(OH-)之比为10-12:10-2=1:1010,或10-10或10-10:1;
![]() 安装汽车尾气处理装置,使尾气中的E(NO2)和一氧化碳反应转化为两种空气的成分,发生的反应为:2 NO2+4CO=N2+4CO2,反应中N元素化合价由+4价降低到0价,C元素化合价由+2价升高到+4价,当反应转移1mol电子时,生成0.125mol N2和0.5mol CO2,体积为0.625mol×22.4L/mol=14L。
安装汽车尾气处理装置,使尾气中的E(NO2)和一氧化碳反应转化为两种空气的成分,发生的反应为:2 NO2+4CO=N2+4CO2,反应中N元素化合价由+4价降低到0价,C元素化合价由+2价升高到+4价,当反应转移1mol电子时,生成0.125mol N2和0.5mol CO2,体积为0.625mol×22.4L/mol=14L。


科目:高中化学 来源: 题型:
【题目】X、Y、Z三种短周期元素,原子半径的大小关系为r(Y)>r(X)>r(Z),原子序数之和为16。X、Y、Z三种元素的常见单质在适当条件下可发生如图所示变化,其中B和C均为10电子分子。下列说法不正确的是( )
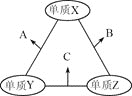
A.X元素位于第ⅥA族
B.A不能溶解于B中
C.A和C不可能发生氧化还原反应
D.B的沸点高于C的沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CoCO3可用作选矿剂、催化剂及家装涂料的颜料。以含钴废渣(主要成份CoO、Co2O3,还含有Al2O3、ZnO等杂质)为原料制备CoCO3的一种工艺流程如下:
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Co2+ | 7.6 | 9.4 |
Al3+ | 3.0 | 5.0 |
Zn2+ | 5.4 | 8.0 |
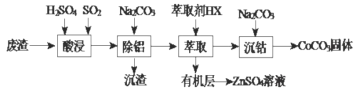
下列说法不正确的是( )
A.“酸溶”时发生氧化还原反应的离子方程式Co2O3+SO2+2H+=2Co2++H2O+SO42-
B.“除铝”过程中需要调节溶液 pH 的范围为5.0~5.4
C.在实验室里,“萃取”过程用到的玻璃仪器主要有分液漏斗、烧杯
D.在空气中煅烧CoCO3生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为0.672L(标准状况),则该钴氧化物的化学式为CoO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯乙烷跟化合物之间的转化如图所示:

(1)写出各反应的化学方程式
①________________________________________________________________________,
②________________________________________________________________________,
③________________________________________________________________________,
④________________________________________________________________________,
⑤________________________________________________________________________。
(2)根据上述方程式回答下列问题:
A.上述化学反应的反应类型有________,________,________。
B.用AgNO3溶液通过________反应可证明卤代烃中含卤元素。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式及有关应用的叙述中,正确的是
A.甲烷的燃烧热为890.3kJmol-1,则甲烷燃烧的热化学方程式可表示为: CH4(g)+![]() O2(g) ═ CO(g) + 2H2O(l) △H = -890.3kJmol-1
O2(g) ═ CO(g) + 2H2O(l) △H = -890.3kJmol-1
B.已知稀溶液中,H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3kJ·mol-1,则稀醋酸与稀氢氧化钠溶液反应生成1mol水时放出57.3kJ的热量
C.500℃下,将0.5mol I2(g)和0.5molH2(g)置于密闭的容器中充分反应生成HI(g),放热10kJ,其热化学方程式为:I2(g) + H2(g)![]() 2HI(g) △H = -20kJmol-1
2HI(g) △H = -20kJmol-1
D.已知25℃、101KPa条件下:4Al(s) + 3O2(g) ═ 2A12O3(s) △H = -2834.9kJmol-1, 4Al(s) + 2O3(g) ═ 2A12O3(s) △H = -3119.1kJmol-1,则O2比O3稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图两圆相交部分A、B、C、D分别表示两物质间的反应。下列各对应反应的离子方程式书写不正确的是( )
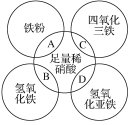
A.Fe+4H++NO3-=Fe3++NO↑+2H2O
B.Fe(OH)3+3H+=Fe3++3H2O
C.Fe3O4+8H+=Fe2++2Fe3++4H2O
D.3Fe(OH)2+10H++NO3-=3Fe3++NO↑+8H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室中过氧乙酸消毒液试剂瓶标签上的有关数据,回答下列问题:

(1)C2H4O3的物质的是浓度为___ mol·L-1。
(2)取用任意体积的该过氧乙酸溶液时,下列物理量中不随所取体积的多少而变化的是___。
A.溶液中C2H4O3的物质的量
B.C2H4O3的物质的量浓度
C.溶液的密度
D.溶液中C2H4O3分子的数目
(3)某学生欲用上述溶液和蒸馏水配制480mL0.100mol·L-1过氧乙酸稀溶液。
①该学生需要选用的容量瓶规格是___ mL。
②该学生需要用量筒量取___ mL上述过氧乙酸溶液进行配制。
③在配制过程中,下列实验操作会使所配制的过氧乙酸的物质的是浓度偏大的是___ (填字母)。
A.转移溶液后未洗涤烧杯和玻璃棒就直接定容
B.用量筒量取过氧乙酸溶液时俯视凹液面
C.在容量瓶中定容时俯视刻度线
D.定容后把容量瓶倒置摇匀,发现液面低于刻度线,又加水至刻度线
(4)室温下,过氧乙酸可以分解放出氧气并生成酷酸(C2H4O2),若取质量分数为15%的过氧乙酸溶液50.0mL,完全分解,理论上得到标准状况下的氧气体积为___ L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等物质的量的铁和铜的混合物24g与600mL稀硝酸恰好完全反应,生成NO6.72L(标准状况)。向反应后的溶液中加入1molL-1NaOH溶液使金属离子恰好沉淀。下列有关说法错误的是( )
A.混合物溶解后的溶液中c(Fe3+):c(Fe2+)=1:1
B.稀硝酸的物质的量浓度度是2molL-1
C.需要加入NaOH溶液1000mL
D.最后所得沉淀在空气中充分加热可得固体32g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应的离子方程式书写正确的是( )
A.氯化铝溶液与过量氨水反应:3NH3H2O+Al3+=Al(OH)3↓+3NH4+
B.向氢氧化钠溶液中通入过量的CO2气体:CO2+2OH-=CO32-+H2O
C.FeCl3溶液与Cu粉反应:Cu+Fe3+=Cu2++Fe2+
D.氢氧化钡溶液与稀硫酸反应:Ba2++SO42-+H++OH-=BaSO4↓+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com