
 H2SO4、Al2(SO4)3和MgSO4的混合溶液中,加入NaOH溶液时,其沉淀的质量W和加入的NaOH体积V之间的关系如图所示,则原混合溶液中Al3+、Mg2+和SO42-的物质的量之比为( )
H2SO4、Al2(SO4)3和MgSO4的混合溶液中,加入NaOH溶液时,其沉淀的质量W和加入的NaOH体积V之间的关系如图所示,则原混合溶液中Al3+、Mg2+和SO42-的物质的量之比为( )| A、1:1:1 |
| B、5:3:2 |
| C、2:1:5 |
| D、3:2:2 |
| 1 |
| 2 |
| 1 |
| 3 |
| 1 |
| 2 |
| 5 |
| 2 |


科目:高中化学 来源: 题型:
| A、0.7 L |
| B、1.4 L |
| C、1.6 L |
| D、2.8 L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向溶液中滴加盐酸酸化的BaCl2溶液 | 产生白色沉淀 | 溶液中不一定含有SO42- |
| B | 向溶液X中先滴加稀NaOH溶液,再将湿润红色石蕊试纸置于试管口附近 | 试纸不变蓝 | 原溶液中无NH4+ |
| C | 向PbO2中滴入浓盐酸 | 有黄绿色气体 | PbO2具有氧化性 |
| D | 向溶液X中加入稀盐酸,并将产生的无色气体通入澄清石灰水中 | 有白色沉淀生成 | 溶液X中一定含有CO32- |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2种和1种 |
| B、2种和3种 |
| C、3种和2种 |
| D、4种和1种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
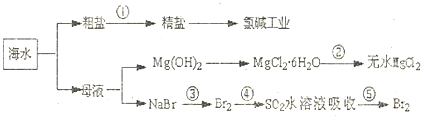
| A、流程①中除去粗盐中的SO42-,Ca2+,Mg2+,Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
| B、流程②中结晶出的MgCl2?6H2O可在空气中受热分解制无水MgCl2 |
| C、在流程③④⑤中溴元素均被氧化 |
| D、大量的氮、磷废水排入海洋,易引发赤潮 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、②④⑤ |
| C、②④⑤⑥ | D、②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该溶液中,K+、Fe2+、C6H5OH、Br-可以大量共存 |
| B、和KI溶液反应的离子方程式:Fe3++2I-═Fe2++I2 |
| C、1 L 0.1 mol?L-1该溶液和足量的Zn充分反应,生成11.2 g Fe |
| D、和Ba(OH)2溶液反应的离子方程式:Fe3++SO42-+Ba2++3OH-═Fe(OH)3↓+BaSO4↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com