
| A、该溶液中,K+、Fe2+、C6H5OH、Br-可以大量共存 |
| B、和KI溶液反应的离子方程式:Fe3++2I-═Fe2++I2 |
| C、1 L 0.1 mol?L-1该溶液和足量的Zn充分反应,生成11.2 g Fe |
| D、和Ba(OH)2溶液反应的离子方程式:Fe3++SO42-+Ba2++3OH-═Fe(OH)3↓+BaSO4↓ |


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
 H2SO4、Al2(SO4)3和MgSO4的混合溶液中,加入NaOH溶液时,其沉淀的质量W和加入的NaOH体积V之间的关系如图所示,则原混合溶液中Al3+、Mg2+和SO42-的物质的量之比为( )
H2SO4、Al2(SO4)3和MgSO4的混合溶液中,加入NaOH溶液时,其沉淀的质量W和加入的NaOH体积V之间的关系如图所示,则原混合溶液中Al3+、Mg2+和SO42-的物质的量之比为( )| A、1:1:1 |
| B、5:3:2 |
| C、2:1:5 |
| D、3:2:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、可逆反应在一定条件下有一定的限度,当反应进行到一定限度后,反应物不再转化为生成物 |
| B、决定化学反应速率的主要因素是参加反应的物质的性质 |
| C、化学反应的速率和限度均可通过改变化学反应条件而改变 |
| D、化学反应达到平衡状态时,只要条件不改变,各物质的浓度就不再改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某溶液中加入稀硫酸再加入铜粉,共热,铜粉溶解且有红棕色气体产生,说明原溶液中含有NO3- |
| B、浓硝酸在光照条件下变黄,说明浓硝酸不稳定,有有色产物生成且能溶于浓硝酸 |
| C、某溶液中加入NaOH溶液,加热能产生使湿润的红色石蕊试纸变蓝的气体,说明原溶液中含有NH4+ |
| D、在KI淀粉溶液中通入氯气,溶液变蓝,说明氯气能与淀粉发生显色反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
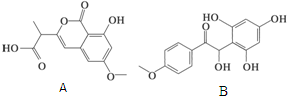
| A、二者都能与Br2发生反应,等物质的量A和B最多消耗的Br2的比例为2:3 |
| B、有机物A和B既可以与FeCl3溶液发生显色反应,又可以和NaHCO3溶液反应 |
| C、1 mol B最多能与6 mol氢气反应 |
| D、等物质的量A和B最多消耗的氢氧化钠质量比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、和酸反应放出等量的CO2所消耗的酸比Na2CO3多 |
| B、相同温度下溶解度比Na2CO3要大 |
| C、热稳定性比Na2CO3小 |
| D、NaHCO3只能和酸作用不能和碱作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、晶体熔点由低到高:CF4<CCl4<CBr4<CI4 |
| B、晶格能由大到小:NaF>NaCl>NaBr>NaI |
| C、硬度由大到小:金刚石>碳化硅>晶体硅 |
| D、熔点由高到低:Na>Mg>Al |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com