
【题目】NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)相同条件下,0.1mol/L NH4Al(SO4)2中c(NH4+) ______ ![]() 填“等于”、“大于”或“小于”0.1mol/LNH4HSO4中c(NH4+)。
填“等于”、“大于”或“小于”0.1mol/LNH4HSO4中c(NH4+)。
(2)如图是0.1mol/L电解质溶液的pH随温度变化的图象:
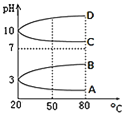
①其中符合0.1mol/L NH4Al(SO4)2的pH随温度变化的曲线是 ______ (填写字母);
②20℃时,0.1mol/L NH4Al(SO4)2中2c(SO42-)-c(NH4+)-3c(Al3+)=______mol/L
(3)室温时,向100mL0.1mol/LNH4HSO4溶液中滴加0.1mol/LNaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。试分析图中a、b、c、d四个点,水的电离程度最大的是 ______ ;在b点,溶液中各离子浓度由大到小的排列顺序是 ______
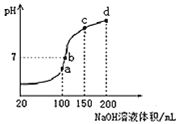
(4)已知Al(OH)3为难溶物(常温下,Ksp[Al(OH)3]=2.0×10-33)当溶液pH=5时,某溶液中的Al3+ ______ ![]() 填“能”或“不能”
填“能”或“不能”![]() 完全沉淀(溶液中的离子浓度小于1×10-5mol/L时,沉淀完全)
完全沉淀(溶液中的离子浓度小于1×10-5mol/L时,沉淀完全)
【答案】小于 A 10-3 a c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) 能
【解析】
(1)相同条件下,铝离子抑制铵根离子水解程度小于氢离子,铵根离子水解程度越大,溶液中铵根离子浓度越小;
(2)①NH4Al(SO4)2中铵根离子和铝离子水解导致溶液呈酸性,则pH<7,升高温度促进水解,溶液酸性增强;
②任何电解质溶液中都存在电荷守恒,根据电荷守恒计算;
(3)a、b、c、d四个点,根据反应量的关系,a点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4;b、c、d三点溶液均含有NH3H2O,(NH4)2SO4可以促进水的电离,而NH3H2O抑制水的电离.b点溶液呈中性;
(4)根据浓度积与溶度积常数相对大小判断,如果浓度积大于溶度积常数,则有沉淀生成,否则没有沉淀生成.
(1)相同条件下,铝离子抑制铵根离子水解程度小于氢离子,铵根离子水解程度越大,溶液中铵根离子浓度越小,所以NH4Al(SO4)2中铵根离子水解程度大于NH4HSO4,则NH4Al(SO4)2中c(NH4+)小于0.1mol/LNH4HSO4中c(NH4+);
(2)①NH4Al(SO4)2中铵根离子和铝离子水解导致溶液呈酸性,则pH<7,升高温度促进水解,溶液酸性增强,溶液的pH减小,故选A;
②根据电荷守恒得2c(SO42-)-c(NH4+)-3c(Al3+)=c(H+)-c(OH-)=10-3mol/L [c(OH-)太小,可忽略];
(3)a、b、c、d四个点,根据反应量的关系,a点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4;b、c、d三点溶液均含有NH3H2O,(NH4)2SO4可以促进水的电离,而NH3H2O抑制水的电离,b点溶液呈中性,即溶液含有(NH4)2SO4、Na2SO4、NH3H2O三种成分,a点时c(Na+)=c(SO42-),b点时c(Na+)>c(SO42-),根据N元素与S元素的关系,可以得出c(SO42-)>c(NH4+),故c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+);
(4)pH=5的溶液中c(OH-)=10-9mol/L,c(Al3+)=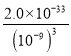 mol/L=2.0×10-6mol/L<1×10-5 mol/L,所以能完全沉淀。
mol/L=2.0×10-6mol/L<1×10-5 mol/L,所以能完全沉淀。


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案科目:高中化学 来源: 题型:
【题目】![]() 时,一定量的
时,一定量的![]() 与盐酸混合所得溶液中,部分含碳微粒的物质的量分数
与盐酸混合所得溶液中,部分含碳微粒的物质的量分数![]() 与pH的关系如图所示。下列说法正确的是
与pH的关系如图所示。下列说法正确的是
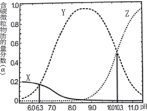
A.曲线X表示的微粒为![]()
B.![]() 时,
时,![]()
C.![]() 时,
时,![]()
D.![]() 时,
时,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“位置”、“结构”和“性质”是我们学习元素周期律的重要思路。
(1)我们可以根据原子结构示意图来推测元素在周期表中的位置,以下为X元素的原子结构示意图(未画全):
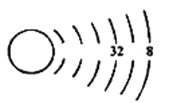
请写出X元素在周期表中的位置_____________________。
(2)我们也可以根据物质性质推测该元素在元素周期表中的位置,如Y元素最高价氧化物既可以溶于浓盐酸,也可以溶于NaOH溶液;其最高价氧化物对应的水化物既可以与酸反应,也可以与碱反应;1mol该元素最高价氧化物对应的水化物在与盐酸反应时,最多能消耗4molHCl。请写出Y元素在周期表中的位置_____________________。
(3)反过来,知道了元素的位置关系,我们可以推测元素性质或者元素对应的单质及化合物的性质。四种短周期元素在周期表中的位置如下图所示,其中只有M为金属元素。则Y和Z原子半径更大的是____(填元素符号或化学式,下同),Y和X最高价氧化物对应水化物的酸性更弱的是______。
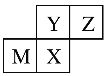
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物W用作调香剂、高分子材料合成的中间体等,制备W的一种合成路线如图。
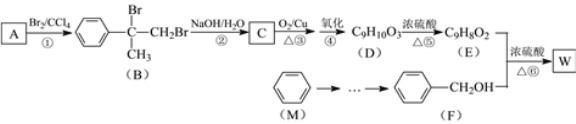
已知:![]() +CH3Cl
+CH3Cl![]()
![]() +HCl
+HCl
请回答下列问题:
(1)A的化学式是___,F的化学名称是___。
(2)②和⑤的反应类型分别____、____。
(3)E中含氧官能团是___(写名称),D聚合生成高分子化合物的结构简式为___。
(4)写出反应⑥的化学方程式:___。
(5)反应③的化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型储氢材料是开发利用氢能的重要研究方向.
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
①基态Cl原子中,电子占据的最高能层符号为_____,该能层具有的原子轨道数为_____.
②LiBH4由Li+和BH4﹣构成,BH4﹣的立体结构是_____,B原子的杂化轨道类型是_____.
Li、B、H元素的电负性由大到小排列顺序为_____.
(2)金属氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径Li+_____H﹣(填“>”、“=”或“<”).②某储氢材料是第三周期金属元素M的氢化物.M的部分电离能如表所示:
I1/kJmol﹣1 | I2/kJmol﹣1 | I3/kJmol﹣1 | I4/kJmol﹣1 | I5/kJmol﹣1 |
738 | 1451 | 7733 | 10540 | 13630 |
M是_____(填元素符号).
(3)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488pm(棱长),Na+半径为102pm,H﹣的半径为_____,NaH的理论密度是___________gcm﹣3(只列算式,不必计算出数值,阿伏加德罗常数为NA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4,溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。 回答下列问题:

(1)外电路的电流方向是由________极流向________极(填字母)。
(2)电池正极反应式为___________________________________。
(3)是否可用水代替电池中的混合有机溶剂?________(填“是”或“否”),原因是________________________________________________________________。
(4)MnO2可与KOH和KClO3在高温下反应,生成K2MnO4,反应的化学方程式为_______________________________________________。K2MnO4在酸性溶液中歧化,生成KMnO4和MnO2的物质的量之比为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃和101kPa时,乙烷、乙炔和丙烯组成的混合烃24mL,与过量氧气混合并完全燃烧,通过浓硫酸后,恢复到原来的温度和压强,气体总体积缩小了54mL,原混合烃中乙炔的体积分数为( )
A.75%B.50%C.25%D.20%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金刚烷胺(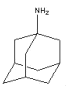 )是最早用于抑制流感病毒的抗病毒药,每片感康(复方氨酚烷胺片)含盐酸金刚烷胺100mg。金刚烷胺一般是由金刚烷合成的。金刚烷是一种重要的化工原料,由环戊二烯合成金刚烷的路线如下:
)是最早用于抑制流感病毒的抗病毒药,每片感康(复方氨酚烷胺片)含盐酸金刚烷胺100mg。金刚烷胺一般是由金刚烷合成的。金刚烷是一种重要的化工原料,由环戊二烯合成金刚烷的路线如下:
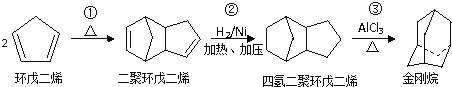
请回答下列问题:
(1)金刚烷的碳架结构相当于是金刚石晶格网络中的一个晶胞,故得金刚烷这个名字。它可看作是由四个等同的六元环组成的空间构型。金刚烷的二氯代物有___种。上述合成金刚烷的路线中,反应①的反应类型为___。
(2)金刚烷与四氢二聚环戊二烯的关系是___。(填字母)
a.均为环烃 b.均为烷烃 c.互为同系物 d.互为同分异构体
(3)下面是以环戊烷为原料制备环戊二烯的合成路线:
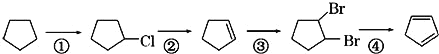
反应④的化学方程式为____。
(4)在有机分析中,常用臭氧氧化分解来确定有机物中碳碳双键的位置与数目。
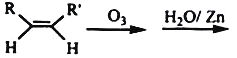 RCHO+R’CHO
RCHO+R’CHO
A是金刚烷的一种同分异构体,经臭氧氧化后的产物仅为一种,其结构为![]() ,试写出A可能的结构简式(任写一种)___。
,试写出A可能的结构简式(任写一种)___。
(5)B是二聚环戊二烯的同分异构体,B分子结构中有一个甲基,B能使溴的四氯化碳溶液褪色,B经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸(提示:苯环上的烷基(—CH3、—CH2R、—CHR2)或烯基侧链经高锰酸钾酸性溶液氧化得羧基),B的结构有多种,其中核磁共振氢谱为6组峰,且面积比为3﹕2﹕2﹕2﹕1﹕2的结构简式是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组欲测定铁的氧化物![]() 样品组成,查阅资料发现:甲酸
样品组成,查阅资料发现:甲酸![]() 是一种有刺激性气味的无色液体,易挥发,有较强的还原性,熔点
是一种有刺激性气味的无色液体,易挥发,有较强的还原性,熔点![]() ,沸点
,沸点![]() ,能与水、乙醇互溶,甲酸与浓硫酸共热可制备一氧化碳:HCOOH
,能与水、乙醇互溶,甲酸与浓硫酸共热可制备一氧化碳:HCOOH![]() H2O+CO↑,制备时先加热浓硫酸至
H2O+CO↑,制备时先加热浓硫酸至![]() ,再逐滴滴入甲酸。根据以上信息设计了实验装置,如图所示:
,再逐滴滴入甲酸。根据以上信息设计了实验装置,如图所示:
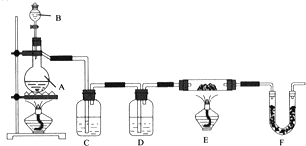
请回答下列问题:
![]() 仪器中装入的试剂:B ______ 、C ______ 、D ______。
仪器中装入的试剂:B ______ 、C ______ 、D ______。
![]() 该实验装置A仪器中须添加一种玻璃仪器,其名称为______;连接好装置后应首先______。
该实验装置A仪器中须添加一种玻璃仪器,其名称为______;连接好装置后应首先______。
![]() “加热反应管E”和“从B向A逐滴滴加液体”这两步操作应该先进行的是______
“加热反应管E”和“从B向A逐滴滴加液体”这两步操作应该先进行的是______![]() 在这两步之间还应进行的操作是______。
在这两步之间还应进行的操作是______。
![]() 反应过程中F管
反应过程中F管![]() 内盛碱石灰
内盛碱石灰![]() 逸出的气体是______,其处理方法是______。
逸出的气体是______,其处理方法是______。
![]() 测得下列数据
测得下列数据![]() 空E管的质量为
空E管的质量为![]() ;
;![]() 管和
管和![]() 样品的总质量为
样品的总质量为![]() ;
;![]() 反应后冷却至室温称量E管和铁粉的总质量为
反应后冷却至室温称量E管和铁粉的总质量为![]() 经确认样品全部变为铁粉
经确认样品全部变为铁粉![]() 计算可知该铁的氧化物化学式为______。
计算可知该铁的氧化物化学式为______。
![]() 设计实验证明:
设计实验证明:
![]() 甲酸的酸性比碳酸的强______。
甲酸的酸性比碳酸的强______。
![]() 的氧化性比
的氧化性比![]() 的弱______。
的弱______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com