
����Ŀ��ij��ѧʵ��С�����ⶨ����������![]() ��Ʒ��ɣ��������Ϸ��֣�����
��Ʒ��ɣ��������Ϸ��֣�����![]() ��һ���д̼�����ζ����ɫҺ�壬�ӷ����н�ǿ�Ļ�ԭ�ԣ��۵�
��һ���д̼�����ζ����ɫҺ�壬�ӷ����н�ǿ�Ļ�ԭ�ԣ��۵�![]() ���е�
���е�![]() ������ˮ���Ҵ����ܣ�������Ũ���Ṳ�ȿ��Ʊ�һ����̼��HCOOH
������ˮ���Ҵ����ܣ�������Ũ���Ṳ�ȿ��Ʊ�һ����̼��HCOOH![]() H2O+CO�����Ʊ�ʱ�ȼ���Ũ������
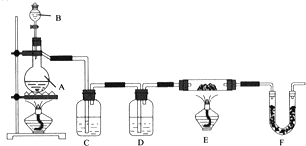
H2O+CO�����Ʊ�ʱ�ȼ���Ũ������![]() ������ε�����ᡣ����������Ϣ�����ʵ��װ�ã���ͼ��ʾ��
������ε�����ᡣ����������Ϣ�����ʵ��װ�ã���ͼ��ʾ��
��ش��������⣺
![]() ������װ����Լ���B ______ ��C ______ ��D ______��
������װ����Լ���B ______ ��C ______ ��D ______��
![]() ��ʵ��װ��A������������һ�ֲ���������������Ϊ______�����Ӻ�װ�ú�Ӧ����______��
��ʵ��װ��A������������һ�ֲ���������������Ϊ______�����Ӻ�װ�ú�Ӧ����______��
![]() �����ȷ�Ӧ��E���͡���B��A��εμ�Һ�塱����������Ӧ���Ƚ��е���______
�����ȷ�Ӧ��E���͡���B��A��εμ�Һ�塱����������Ӧ���Ƚ��е���______![]() ��������֮�仹Ӧ���еIJ�����______��
��������֮�仹Ӧ���еIJ�����______��
![]() ��Ӧ������F��
��Ӧ������F��![]() ��ʢ��ʯ��
��ʢ��ʯ��![]() �ݳ���������______���䴦��������______��
�ݳ���������______���䴦��������______��
![]() �����������
�����������![]() ��E�ܵ�����Ϊ
��E�ܵ�����Ϊ![]() ��
��![]() �ܺ�
�ܺ�![]() ��Ʒ��������Ϊ
��Ʒ��������Ϊ![]() ��
��![]() ��Ӧ����ȴ�����³���E�ܺ����۵�������Ϊ
��Ӧ����ȴ�����³���E�ܺ����۵�������Ϊ![]() ��ȷ����Ʒȫ����Ϊ����
��ȷ����Ʒȫ����Ϊ����![]() �����֪�����������ﻯѧʽΪ______��
�����֪�����������ﻯѧʽΪ______��
![]() ���ʵ��֤����
���ʵ��֤����
![]() ��������Ա�̼���ǿ______��
��������Ա�̼���ǿ______��
![]() �������Ա�
�������Ա�![]() ����______��
����______��
���𰸡����� ����������Һ Ũ���� �¶ȼ� ��������� ��B��A��εμ�Һ�� ����CO�Ĵ��� CO ��F�ܳ��ڴ���ȼ���������ռ� FeO ��ʢ������![]() ���Թ���μӼ�����Һ�����ݲ��� ��ʢ����������ͭ��Һ���Թ���������ۣ����к�ɫ������֣���Һ����ɫ��Ϊdz��ɫ
���Թ���μӼ�����Һ�����ݲ��� ��ʢ����������ͭ��Һ���Թ���������ۣ����к�ɫ������֣���Һ����ɫ��Ϊdz��ɫ
��������
װ��AΪ��ƿʢ��Ũ���ᣬ��Һ©����ʢ�ż��ᣬ�Ʊ�ʱ�ȼ���Ũ������80��-90�棬����ε�����ᣬ������ӦHCOOH![]() H2O+CO����ͨ��װ��C�е�����������Һ���ջӷ����ļ��ᣬͨ��װ��D�� ��Ũ�������������е�ˮ�������õ���������һ����̼��ͨ��װ��E�к���������������ȷ�Ӧ�������Ͷ�����̼��ͨ��װ��F�������ɵĶ�����̼��ʣ������һ����̼��ȼ������
H2O+CO����ͨ��װ��C�е�����������Һ���ջӷ����ļ��ᣬͨ��װ��D�� ��Ũ�������������е�ˮ�������õ���������һ����̼��ͨ��װ��E�к���������������ȷ�Ӧ�������Ͷ�����̼��ͨ��װ��F�������ɵĶ�����̼��ʣ������һ����̼��ȼ������
��1�������зֱ�ʢ�ŵ��Լ��ֱ�Ϊ�������������Һ��Ũ���
��2����ʵ��װ��A������������һ�ֲ�������ӦΪ�¶ȼƣ���֪��Ӧ�¶�80��-90�棬��ֹ����ӷ������巢��װ�úͳ���װ�á�������֤װ�õ���Ҫ����װ�������ԣ�
��3��ʵ�������Ӧ�ȵ�ȼ��ƿ���ƾ��ƣ������������װ�ú��ټ���װ��E���ƾ��ƣ���������֮����Ҫ����һ����̼�Ĵ��ȣ���ֹ����װ��E�е�һ����̼���п������ȱ�ը��
��4����Ӧ������F�ܣ���ʢ��ʯ�ң��ݳ���������һ����̼�������ŷŵ������У���Ҫ��ȼ������
��5������������ݢٿ�E�ܵ�����Ϊ16.6g����E�ܺ�FexOy��Ʒ��������Ϊ27.4g���۷�Ӧ����ȴ�����³���E�ܺ����۵�������Ϊ25.0g����ȷ����Ʒȫ����Ϊ���ۣ����õ���������������=27.4g-16.6g=10.8g��������������=25.0g-16.6g=8.4g������Ԫ���غ������Ԫ�غ���Ԫ�����ʵ����õ������ﻯѧʽ��
��6���ټ�������Ա�̼���ǿ��������Ƽ����̼��������Һ��Ӧ���ɶ�����̼��֤����ǿ����
��Fe2+�������Ա�Cu2+����������������Ӱ���������������ƣ�������������ͭ��Һ�з�Ӧ����ͭ����������֤����
װ��AΪ��ƿʢ��Ũ���ᣬ��Һ©����ʢ�ż��ᣬ�Ʊ�ʱ�ȼ���Ũ������![]() ������ε�����ᣬ������ӦHCOOH
������ε�����ᣬ������ӦHCOOH![]() H2O+CO����ͨ��װ��C�е�����������Һ���ջӷ����ļ��ᣬͨ��װ��D�е�Ũ�������������е�ˮ�������õ���������һ����̼��ͨ��װ��E�к���������������ȷ�Ӧ�������Ͷ�����̼��ͨ��װ��F�������ɵĶ�����̼��ʣ������һ����̼��ȼ������
H2O+CO����ͨ��װ��C�е�����������Һ���ջӷ����ļ��ᣬͨ��װ��D�е�Ũ�������������е�ˮ�������õ���������һ����̼��ͨ��װ��E�к���������������ȷ�Ӧ�������Ͷ�����̼��ͨ��װ��F�������ɵĶ�����̼��ʣ������һ����̼��ȼ������
![]() ���ݷ������̿�֪�������зֱ�ʢ�ŵ��Լ��ֱ�Ϊ��B��Ϊ���ᡢC��Ϊ����������Һ��D��ΪŨ���ᣬ�ʴ�Ϊ���������������Һ��Ũ���
���ݷ������̿�֪�������зֱ�ʢ�ŵ��Լ��ֱ�Ϊ��B��Ϊ���ᡢC��Ϊ����������Һ��D��ΪŨ���ᣬ�ʴ�Ϊ���������������Һ��Ũ���
![]() ��ɿ�֪��Ӧ�¶�
��ɿ�֪��Ӧ�¶�![]() ����ʵ��װ��A������������һ�ֲ�������ӦΪ�¶ȼƣ���ֹ����ӷ������巢��װ�úͳ���װ�á�������֤װ�õ���Ҫ����װ�������ԣ��ʴ�Ϊ���¶ȼƣ���������ԣ�
����ʵ��װ��A������������һ�ֲ�������ӦΪ�¶ȼƣ���ֹ����ӷ������巢��װ�úͳ���װ�á�������֤װ�õ���Ҫ����װ�������ԣ��ʴ�Ϊ���¶ȼƣ���������ԣ�
![]() ʵ�������Ӧ�ȵ�ȼ��ƿ���ƾ��ƣ������������װ�ú��ټ���װ��E���ƾ��ƣ���������֮����Ҫ����һ����̼�Ĵ��ȣ���ֹ����װ��E�е�һ����̼���п������ȱ�ը�������ȷ�Ӧ��E��������B��A��εμ�Һ��������������Ӧ���Ƚ��е��ǣ���B��A��εμ�Һ�壬��������֮�仹Ӧ���еIJ����Ǽ���CO�Ĵ��ȣ��ʴ�Ϊ����B��A��εμ�Һ�壻����CO�Ĵ��ȣ�
ʵ�������Ӧ�ȵ�ȼ��ƿ���ƾ��ƣ������������װ�ú��ټ���װ��E���ƾ��ƣ���������֮����Ҫ����һ����̼�Ĵ��ȣ���ֹ����װ��E�е�һ����̼���п������ȱ�ը�������ȷ�Ӧ��E��������B��A��εμ�Һ��������������Ӧ���Ƚ��е��ǣ���B��A��εμ�Һ�壬��������֮�仹Ӧ���еIJ����Ǽ���CO�Ĵ��ȣ��ʴ�Ϊ����B��A��εμ�Һ�壻����CO�Ĵ��ȣ�
![]() ��Ӧ������F��
��Ӧ������F��![]() ��ʢ��ʯ��
��ʢ��ʯ��![]() �ݳ���������һ����̼�������ŷŵ������У���Ҫ��ȼ���������ռ��������ʴ�Ϊ��CO����F�ܳ��ڴ���ȼ���������ռ���
�ݳ���������һ����̼�������ŷŵ������У���Ҫ��ȼ���������ռ��������ʴ�Ϊ��CO����F�ܳ��ڴ���ȼ���������ռ���
![]() �����������
�����������![]() ��E�ܵ�����Ϊ
��E�ܵ�����Ϊ![]() ��
��![]() �ܺ�
�ܺ�![]() ��Ʒ��������Ϊ
��Ʒ��������Ϊ![]() ��
��![]() ��Ӧ����ȴ�����³���E�ܺ����۵�������Ϊ
��Ӧ����ȴ�����³���E�ܺ����۵�������Ϊ![]() ��ȷ����Ʒȫ����Ϊ����
��ȷ����Ʒȫ����Ϊ����![]() ���õ���������������
���õ���������������![]() ��������������
��������������![]() ������Ԫ���غ������Ԫ�غ���Ԫ�����ʵ����õ������ﻯѧʽ
������Ԫ���غ������Ԫ�غ���Ԫ�����ʵ����õ������ﻯѧʽ![]() ��
��![]() ��
��![]() 1:1����ѧʽΪFeO���ʴ�Ϊ��FeO��
1:1����ѧʽΪFeO���ʴ�Ϊ��FeO��
![]() ��������Ա�̼���ǿ��������Ƽ����̼��������Һ��Ӧ���ɶ�����̼��֤����ǿ������ʢ������
��������Ա�̼���ǿ��������Ƽ����̼��������Һ��Ӧ���ɶ�����̼��֤����ǿ������ʢ������![]() ���Թ���μӼ�����Һ�����ݲ�����˵����������ǿ��̼�ᣬ�ʴ�Ϊ����ʢ������
���Թ���μӼ�����Һ�����ݲ�����˵����������ǿ��̼�ᣬ�ʴ�Ϊ����ʢ������![]() ���Թ���μӼ�����Һ�����ݲ�����
���Թ���μӼ�����Һ�����ݲ�����
![]() �������Ա�
�������Ա�![]() ���������������������Դ�������������ƣ�������������ͭ��Һ�з�Ӧ����ͭ����������֤�����������Ϊ����ʢ����������ͭ��Һ���Թ���������ۣ����к�ɫ������֣���Һ����ɫ��Ϊdz��ɫ��˵��ͭ���������Դ����������ӣ��ʴ�Ϊ����ʢ����������ͭ��Һ���Թ���������ۣ����к�ɫ������֣���Һ����ɫ��Ϊdz��ɫ��
���������������������Դ�������������ƣ�������������ͭ��Һ�з�Ӧ����ͭ����������֤�����������Ϊ����ʢ����������ͭ��Һ���Թ���������ۣ����к�ɫ������֣���Һ����ɫ��Ϊdz��ɫ��˵��ͭ���������Դ����������ӣ��ʴ�Ϊ����ʢ����������ͭ��Һ���Թ���������ۣ����к�ɫ������֣���Һ����ɫ��Ϊdz��ɫ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NH4Al(SO4)2��ʳƷ�ӹ�����Ϊ��ݵ�ʳƷ���Ӽ������ڱ���ʳƷ�У�NH4HSO4�ڷ����Լ���ҽҩ�����ӹ�ҵ����;�㷺����ش��������⣺
(1)��ͬ�����£�0.1mol/L NH4Al(SO4)2��c(NH4+) ______ ![]() ������������������������С����0.1mol/LNH4HSO4��c(NH4+)��
����������������������������0.1mol/LNH4HSO4��c(NH4+)��
(2)��ͼ��0.1mol/L�������Һ��pH���¶ȱ仯��ͼ��
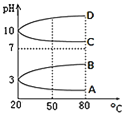
�����з���0.1mol/L NH4Al(SO4)2��pH���¶ȱ仯�������� ______ (��д��ĸ)��
��20��ʱ��0.1mol/L NH4Al(SO4)2��2c(SO42-)-c(NH4+)-3c(Al3+)=______mol/L
(3)����ʱ����100mL0.1mol/LNH4HSO4��Һ�еμ�0.1mol/LNaOH��Һ���õ�����ҺpH��NaOH��Һ����Ĺ�ϵ������ͼ��ʾ���Է���ͼ��a��b��c��d�ĸ��㣬ˮ�ĵ���̶������� ______ ����b�㣬��Һ�и�����Ũ���ɴ�С������˳���� ______
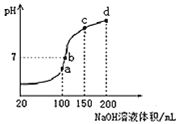
(4)��֪Al(OH)3Ϊ������(�����£�Ksp[Al(OH)3]=2.0��10-33)����ҺpH=5ʱ��ij��Һ�е�Al3+ ______ ![]() ������������������
������������������![]() ��ȫ����(��Һ�е�����Ũ��С��1��10-5mol/Lʱ��������ȫ)
��ȫ����(��Һ�е�����Ũ��С��1��10-5mol/Lʱ��������ȫ)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1��2����������������Ϳ����������Ӽ���������������ɫҺ�壬������ˮ�������ڴ����л��ܼ���ʵ�����Ʊ�1��2����������ķ�Ӧԭ�����£�
CH3CH2OH![]() CH2=CH2+H2O
CH2=CH2+H2O
CH2=CH2+Br2��BrCH2CH2Br
��֪�����Ҵ���Ũ�����������140����ˮ��������
2CH3CH2OH![]() CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
��ʵ���г����¶ȹ��߶�ʹ�Ҵ���Ũ���ᷴӦ��������SO2��CO2����12.0g����������Ҵ��Ʊ�1��2-�������飬ʵ��װ����ͼ��ʾ��
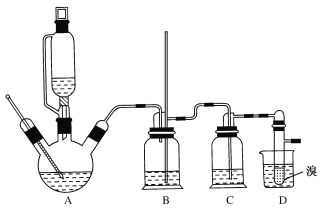
�й������б����£�
��� | �Ҵ� | 1��2-�������� | ���� |
״̬ | ��ɫҺ�� | ��ɫҺ�� | ��ɫҺ�� |
�ܶ�/g��cm-3 | 0.79 | 2.2 | 0.71 |
�е�/�� | 78.5 | 132 | 34.6 |
�۵�/�� | -130 | 9 | -116 |
�ش��������⣺
��1���ڴ��Ʊ�ʵ���У�A�а���������3�s1�����Ҵ���Ũ�����A�л�Ҫ���뼸�����Ƭ����������___��Ҫ������Ѹ�ٵذѷ�Ӧ�¶���ߵ�170�����ң�������ҪĿ����___��
��2��װ��B������������ȫƿ��ƿ��ʢˮ�����˿��Է�ֹ�������⣬�����ж�װ���Ƿ��������������B��������____��
��3����װ��C��Ӧ����NaOH��Һ����Ŀ����____��
��4��װ��D��С�Թ���ʢ��Һ�壬�жϸ��Ʊ���Ӧ�Ѿ��������������___��
��5����1��2����������ֲ�Ʒ���ڷ�Һ©���м�ˮ�����ã�����Ӧ��___��(����������������)����������������δ��Ӧ��Br2�������___ϴ�ӳ�ȥ�������������������������ѣ�����____��������������ƣ��ķ�����ȥ��
��6����Ӧ������Ӧ����ˮ��ȴװ��D������ҪĿ������ϩ���巴Ӧʱ���ȣ���ȴ�ɱ�����Ĵ����ӷ������ֲ��ܹ�����ȴ(���ñ�ˮ)����ԭ����___��
��7����ʵ�������õ�9.4g��Ʒ��1��2����������IJ���Ϊ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������һ�������������������ο�����������������������ױ���������ʵ�����Ʊ�������ij��÷���֮һ��
��һ����Ӧԭ��
C6H5CH3+2KMnO4![]() C6H5COOK+KOH+2MnO2��+H2O
C6H5COOK+KOH+2MnO2��+H2O
C6H5COOK+HCl��C6H5COOH+KCl
��֪����������Է�������122���۵�122.4�棻��������ˮ�е��ܽ�����±���
�¶�/�� | 17.5 | 25 | 75 | 80 | 100 |
�ܽ��/g | 3.00 | 3.99 | 5.90 | 8.39 | 11.7 |
������ʵ�����
�ٽ�һ�����ױ���ˮ��������ʯ����������ƿ�У�
��װ�������ܣ��������к������������������أ����������Ӧ4Сʱ��
�۽���Ӧ�������ȼ�ѹ���ˣ�������ˮϴ����������ϴ��Һ������Һ�У�
����Һ���������ữ����(װ����ͼ1)��ϴ�ӡ�����ñ�����ֲ�Ʒ��
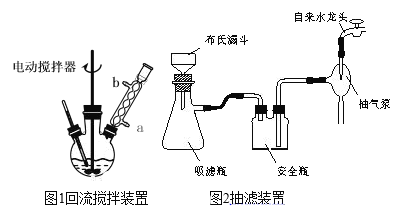
��1��ͼ1�綯��������������_____������������ˮӦ��_____������a������b�����ڽ��룻�жϼױ���������ȫ��ʵ��������____��
��2���ڢ۲����˲���ʱ��Ҫ���Ƚ��У�����Ϊ_____����Ӧ�������ȼ�ѹ���˺�����Һ�ʺ�ɫ����������NaHSO3��Һ��������Ӧ�����ӷ���ʽΪ_____��
���������Ȳⶨ
��3����ȡ1.22g��Ʒ�ܽ��ڼ״������100mL��Һ����ȡ25.00mL��Һ����KOH����Һ���еζ�������KOH�����ʵ���Ϊ2.30��10-3mol����Ʒ�б����������ٷ���Ϊ____��������λ��Ч���֣���
���ģ�ʵ�鷴˼
��4���õ��Ĵֲ�ƷҪ��һ���ᴿ�����ᣬ�ɲ���_____�ķ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�������Ҵ���Ũ������ȷ�Ӧ��ȡ��ϩ����ش��������⣺
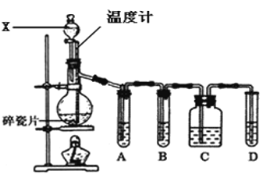
��1��д��ʵ��������ϩ�Ļ�ѧ��Ӧ����ʽ��___���÷�Ӧ��Ũ����������ǣ�___��___��
��2�������������ʵ����ȷ�������������������ϩ�Ͷ��������Իش��������⣺
��ͼ��A��B��C��D4��װ�ÿ�ʢ�ŵ��Լ���A___��B___��C___��D__���������й��Լ�����������ո��ڣ���
��1��Ʒ����Һ ��2��NaOH��Һ ��3��KMnO4��Һ
����˵����������������ڵ�������___��
��ʹ��װ��B��Ŀ����___��
��ʹ��װ��C��Ŀ����___��
����֤��������ϩ��������___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ָ����ѧ������ȷ������ ��
A. NaHCO3ˮ������ӷ���ʽ��HCO3-+H2O = CO32-+H3O+
B. Ba(OH)2�ĵ��뷽��ʽ��Ba(OH)2![]() Ba2++2OH-
Ba2++2OH-
C. NaHSO4��ˮ�еĵ��뷽��ʽ��NaHSO4= Na++H++SO42-
D. Na2Sˮ������ӷ���ʽ��S2-+2H2O = H2S+2OH-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. �����£�pH=4��CH3COOH��Һ�У���ˮ�����c(H��) = 10-10 mol/L
B. ��pH=2��HCl��Һ��pH=4��H2SO4��Һ�������ϣ�������ҺpH=3
C. 0.1 mol/L��ˮ��0.1 mol/L NH4Cl��Һ�������Ϻ�������ҺpH>7����c(NH4��) < c(NH3��H2O)
D. ��0.1 mol/L��pH=1��NaHA��Һ�м���NaOH��Һ��Ӧ�����ӷ���ʽΪ��HA��+ OH�� = H2O + A2-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������Һ��������������ռ���Һ��װ����ͼ��ʾ������������������Ϊ���Ե缫�����ͬ��ͬѹ�£�������������ҵ������ԼΪ1��2������˵����ȷ����(����)
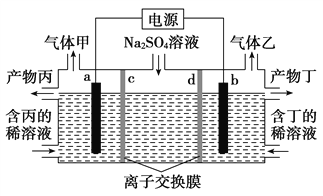
A. a�����Դ�ĸ�������
B. ���������
C. ���ӽ���ĤdΪ�����ӽ���Ĥ
D. a�缫��Ӧʽ��2H2O��2e��===H2����2OH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.100 0 mol��L-1NaOH��Һ�ֱ�ζ������Ϊ20.00 mL������ʹ�����Һ���ζ���������ͼ������˵����ȷ����
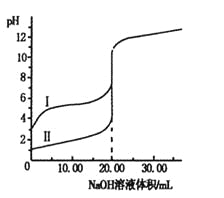
A.I����ֱ��ʾ����ʹ���ĵζ�����
B.����ʹ����Ũ�Ⱦ�Ϊ0.100 0 mol��L-1
C.pH��7ʱ��������������NaOH��Һ��������
D.V(NaOH)��20.00mLʱ��c(Clһ)��c(CH3COOһ)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com