
����Ŀ������˵����ȷ����
A. �����£�pH=4��CH3COOH��Һ�У���ˮ�����c(H��) = 10-10 mol/L
B. ��pH=2��HCl��Һ��pH=4��H2SO4��Һ�������ϣ�������ҺpH=3
C. 0.1 mol/L��ˮ��0.1 mol/L NH4Cl��Һ�������Ϻ�������ҺpH>7����c(NH4��) < c(NH3��H2O)
D. ��0.1 mol/L��pH=1��NaHA��Һ�м���NaOH��Һ��Ӧ�����ӷ���ʽΪ��HA��+ OH�� = H2O + A2-
���𰸡�A
��������
A. �����£�pH=4��CH3COOH��Һ�У�c(H��) = 10-4mol/L������ˮ�����c(H��) ˮ= c(OH-)ˮ= 10-10 mol/L����A��ȷ��B. ��pH=2��HCl��Һ��c(H��) = 10-2mol/L��pH=4��H2SO4��Һ��c(H��) = 10-4mol/L�����ߵ������ϣ�������Һ��c(H��) = ![]() ��(10-2mol/L +10-4mol/L)��
��(10-2mol/L +10-4mol/L)��![]() ��10-2mol/L��10-3mol/L��pH��3����B����C. 0.1 mol/L��ˮ��0.1 mol/L NH4Cl��Һ�������Ϻ�������ҺpH>7����c(H+)��c(OH-)�����ݵ���غ㣬��c(NH4��) ��c(Cl-)����˰�ˮ�ĵ���Ϊ������� c(NH4��) ��c(NH3��H2O)����C����D. 0.1 mol/LNaHA��Һ��pH=1��˵��HA����ȫ���룬����0.1 mol/L��pH=1��NaHA��Һ�м���NaOH��Һ��Ӧ�����ӷ���ʽΪ��H++ OH�� =H2O����D����ѡA��
��10-2mol/L��10-3mol/L��pH��3����B����C. 0.1 mol/L��ˮ��0.1 mol/L NH4Cl��Һ�������Ϻ�������ҺpH>7����c(H+)��c(OH-)�����ݵ���غ㣬��c(NH4��) ��c(Cl-)����˰�ˮ�ĵ���Ϊ������� c(NH4��) ��c(NH3��H2O)����C����D. 0.1 mol/LNaHA��Һ��pH=1��˵��HA����ȫ���룬����0.1 mol/L��pH=1��NaHA��Һ�м���NaOH��Һ��Ӧ�����ӷ���ʽΪ��H++ OH�� =H2O����D����ѡA��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���з�ӦCO(g)��H2O(g) ![]() CO2(g)��H2(g)����H��0����������������������
CO2(g)��H2(g)����H��0����������������������
A. ����������ı��˷�Ӧ��;������Ӧ�Ħ�HҲ��֮�ı�
B. �ı�ѹǿ��ƽ�ⲻ�����ƶ�����Ӧ�ų�����������
C. �����¶ȣ���Ӧ���ʼӿ죬��Ӧ�ų�����������
D. ����Ӧ��Ũ�ȣ���Ӧ�Ħ�HҲ��֮�ı�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�����һ��ԭ��ء��Իش���������(���ݹ��ʺ���)��

(1)�������ҺΪϡ����ʱ������________ (��������������������a�⣬���������b��)��
a��������������Mg�缫�Ϸ����ķ�ӦΪ______________��Al�缫�Ϸ����ķ�ӦΪ________________________________________________________________________��
(2)�������ҺΪNaOH��Һʱ������________ (��������������������a�⣬���������b��)��
a������������Al�缫�Ϸ����ķ�ӦΪ________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(���ӻ�����)������18�����ӣ�
���� | A�� | B2�� | C | D | E | F |
����ص� | �������� | �����˫�˷��� | ���ʣ�˫�˷��� | ��������˷��� | ������ĺ˷��� | |
��ش��������⣺
(1)A��Ԫ�ط�����____________��B2���Ľṹʾ��ͼ��________��
(2)C��D��ϣ�������Ӧ�Ļ�ѧ����ʽΪ_____________________________________��
(3)E�ĵ���ʽ��________��F��ˮ��Һ��������������F�Ļ�ѧʽ��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڳ��º��ݵ��ܱ������г���Ũ�Ⱦ�Ϊ1 mol/L��NH3��HCl������NH3(g) + HCl(g)![]() NH4Cl(?) ��H = -a kJ/mol������˵����ȷ����
NH4Cl(?) ��H = -a kJ/mol������˵����ȷ����
A. ������������
B. ��Ӧ��Ļ��Ϊa kJ/mol
C. �������£���������ƽ��Ħ������ʼ�ղ���
D. �κ��¶��£��÷�Ӧ�����Է�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��һ��Ҷ���ط��ӣ���Ѫ�쵰���ӣ��ң��ľֲ��ṹ��ͼ������˵������ȷ���ǣ� ��
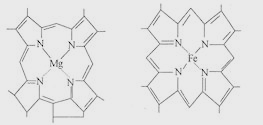
A.�ϳ�Ҷ���غ�Ѫ�쵰�ֱ���Ҫþ����
B.ֲ����ȱ����Ӱ��������
C.����ȱ����Ӱ��Ѫ�쵰����������
D.Mg��Fe�ֱ������ֲ��Ͷ���ϸ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йغ�̼����˵������Ҫ����գ�
(1)ͬ�¶ȣ�ͬŨ�ȵ�Na2CO3��Һ�ļ���_________ NaHCO3��Һ�ļ���(��������������С��������������)�������һ���ϼ���ʵ��֤��___________��
(2)��25 ��ʱ����10 mL 0.1 mol/L Na2CO3��Һ����μ���0.1 mol/L HCl��Һ20 mL����Һ�к�̼�������ʵ�������ҺpH�ı仯��ͼ��ʾ��
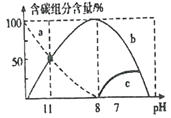
��HC1��Һ�μӵ�һ��ʱ����Һ��___________(������������������������������)��������____________________(����Ҫ�����ӷ���ʽ��ʾ)��
�ڹ���ͼ������˵����ȷ����_________________��
A��0.1 mol/L Na2CO3��Һ�У�c(Na��) + c(H��) = c(OH��) + 2c(CO32��) + c(HCO3��)
B��b���ߴ���CO32��
C��pH=11ʱ��c(HCO3��) > c(Cl��)
D��pH=11 ʱ��c(Na��) + c(H��) = 3c(CO32��) + c(OH��)
E����ͬһ��Һ�У�H2CO3��HCO3����CO32���ܴ�������
(3)����(H2C2O4)��Һ���л�ԭ�ԣ�������KMnO4��Һ���������Һ�У���������ݣ����Ϻ�ɫ��ȥ��д���÷�Ӧ�����ӷ���ʽ________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б�ʾʽ�������(����)
A. Na���Ĺ����ʾʽ��![]() B. Na���Ľṹʾ��ͼ��
B. Na���Ľṹʾ��ͼ��![]()
C. Na�ĵ����Ų�ʽ��1s22s22p63s1 D. Na����Χ�����Ų�ʽ��3s1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ۺͻ���̿�Ļ������NaCl��Һʪ���������ͼ��ʾװ���У��������ĵ绯ѧ��ʴʵ�顣�����йظ�ʵ���˵����ȷ����

A. ���������ĵ缫��ӦʽΪFe3e![]() Fe3+
Fe3+
B. ����ʴ�����л�ѧ��ȫ��ת��Ϊ����
C. ����̿�Ĵ��ڻ�������ĸ�ʴ
D. ��ˮ����NaCl��Һ�������ܷ���������ʴ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com