
【题目】A,B,C,D,E,F,G为7种由短周期元素构成的粒子,它们都有10个电子,其结构特点如下,其中:B的离子半径大于E的离子半径;D是由极性键构成的4原子分子;C与F可形成D和G分子。
微粒 | A | B | C | D | E | F | G |
原子核数 | 单核 | 单核 | 多核 | 多核 | 单核 | 多核 | 多核 |
电荷数 | 0 | 1+ | 1- | 0 | 2+ | 1+ | 0 |
(1)A粒子的结构示意图是_________。
(2)用电子式表示D的形成过程: ________________________
(3)比较B与E相应元素的最高价氧化物对应水化物的碱性强弱,为______>_______(用化学式表示)。
(4)D与G反应的化学方程式是_________________。
(5)C粒子是_________,F粒子是_________(用电子式表示)。
【答案】 ![]()
![]() NaOH Mg(OH)2 NH3 +H2O== NH3 .H2O OH-
NaOH Mg(OH)2 NH3 +H2O== NH3 .H2O OH- 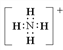
【解析】本题考查元素周期表中的“位构性”应用,以及化学用语的正确使用,(1)都是10电子微粒,A为单核,且电荷数为0,A为Ne,其原子结构示意图为:![]() ;(2)D是由极性键构成的4原子分子,电荷数为0,即D为NH3,NH3是共价化合物,
;(2)D是由极性键构成的4原子分子,电荷数为0,即D为NH3,NH3是共价化合物,![]() ;(3)B为单核的+1价阳离子,即B为Na+,对应元素是Na,其最高价氧化物对应水化物是NaOH,E是单核显+2价的阳离子,即E为Mg2+,对应元素是Mg,其最高价氧化物对应水化物是Mg(OH)2,金属性越强,其最高价氧化物对应水化物的碱性越强,金属性:Na>Mg,即碱性:NaOH>Mg(OH)2;(4)C为多核带有-1价阴离子,即C为OH-,F为多核的+1价阳离子,可能是H3O+,也可能是NH4+,C与F形成NH3和G,因此F为NH4+,NH4++OH-
;(3)B为单核的+1价阳离子,即B为Na+,对应元素是Na,其最高价氧化物对应水化物是NaOH,E是单核显+2价的阳离子,即E为Mg2+,对应元素是Mg,其最高价氧化物对应水化物是Mg(OH)2,金属性越强,其最高价氧化物对应水化物的碱性越强,金属性:Na>Mg,即碱性:NaOH>Mg(OH)2;(4)C为多核带有-1价阴离子,即C为OH-,F为多核的+1价阳离子,可能是H3O+,也可能是NH4+,C与F形成NH3和G,因此F为NH4+,NH4++OH-![]() NH3↑+H2O,G为H2O,因此D和G的反应是NH3+H2O=NH3·H2O;(5)根据问题(4)的分析,C为OH-,F为NH4+,其电子式为
NH3↑+H2O,G为H2O,因此D和G的反应是NH3+H2O=NH3·H2O;(5)根据问题(4)的分析,C为OH-,F为NH4+,其电子式为 。
。


科目:高中化学 来源: 题型:
【题目】从H、O、S、K四种元素中选择适当的元素,组成与表中第一行物质类别相同的物质,将其化学式天子表中相应空格内
示例 | HN03 | NaOH | Na2CO3 | CO2 |
化学式 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表的一部分,已知A、B、C、D均为短周期元素,A与D的原子序数之和是C的原子序数的1.5倍。
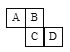
(1)A、B、C、D的简单气态氢化物中最不稳定的是__________(写化学式)。
(2)A、D两种元素的简单气态氢化物相互反应的化学方程式为___________________,现象为___________;产物的电子式为____________。
(3)写出下列物质的电子式:D的气态氢化物______________。A的单质_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中属于消去反应的是
A. 溴乙烷与NaOH醇溶液共热 B. 甲苯与浓硫酸和浓硝酸的反应
C. 溴乙烷与NaOH水溶液共热 D. 甲烷与氯气在光照的条件下反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素在元素周期表中的位置,反映了元素的原子结构和元素的性质,右图所示是元素周期表的一部分:

(1)元素N在元素周期表中的位置为第______周期________族。根据元素周期律,请预测H3AsO4、H3PO4的酸性强弱:H3AsO4_________ H3PO4 (填“>”“<”或“=”)。
(2)根据NaH的存在,有人提议可把氢元素放在ⅦA族,那么根据其最高正化合价与最低负化合价的绝对值相等,又可把氢元素放在元素周期表中的________族。
(3)元素甲是第3周期金属元素中原子半径最小的元素,该元素的离子与过量的氨水反应的离子方程式为_________________________。
(4)元素周期表中有10多种人体所需的微量元素,其中有一种被誉为“生命元素”的主族元素R,对延长人类寿命起着重要作用。已知R的原子有4个电子层,其最高价氧化物的分子式为RO3,则R的名称为______(填序号)。
A.硫 B.砷 C.硒 D.硅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我们的衣食住行中都蕴含着丰富的化学知识,下列说法中正确的是( )
A.衣料中的蚕丝和涤纶都属于合成有机高分子材料
B.加碘食盐和铁强化酱油都可以补充人体必需的微量元素
C.建筑高楼大厦时用到的钢是纯净物
D.用液化石油气代替汽油作汽车燃料,不会造成空气污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定质量的铝铁合金溶于足量的NaOH溶液中,完全反应后产生3.36 L(标准状况下)气体;用同样质量的铝铁合金完全溶于足量的盐酸中,在标准状况下产生5.6 L的气体。该合金中铝、铁的物质的量之比为( )
A. 1∶1 B. 2∶5 C. 3∶2 D. 3∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研单位利用电化学原理用SO2来制备硫酸,装置如下图,含有某种催化剂。电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触。
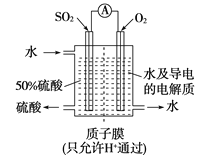
(1)通入SO2的电极为__________极,其电极反应式为_________________,此电极区pH_______(填“增大”“减小”或“不变”)。
(2)若通入SO2的速率为2.24 L/min(标准状况),为稳定持续生产,硫酸溶液的浓度应维持不变,则左侧水的流入速率是 (结果用 mL/min表示)
(3)以此电源电解足量的硝酸银溶液,若阴极产物的质量为21.6 g,则阳极产生气体标准状况下体积为__________L。
(4)常温时,BaSO4的Ksp=1.08×10-10。现将等体积的BaCl2溶液与3.5×10-3mol/L的Na2SO4溶液混合。若要生成BaSO4沉淀,BaCl2溶液的最小浓度为________。
(5)已知:Fe2O3(s)+3C(石墨)==2Fe(s)+3CO(g) ΔH =+489.0 kJ·mol-1
CO(g)+1/2O2(g)==CO2(g) ΔH=-283.0 kJ·mol-1
C(石墨)+O2(g)==CO2 (g) ΔH=-393.5 kJ·mol-1
则4Fe(s)+3O2(g)==2Fe2O3(s)的ΔH为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com