
����Ŀ��ͼ���dz��������巢��װ��;�����������������ռ�װ��,����Ҫ��ش���������:



![]()


��1������MnO2��Ũ���ᷴӦ��ȡ����,Ӧѡ��װ��________,�÷���ʽ��ʾ����ȡ�����ķ�Ӧԭ����___________________________��
��2������KMnO4��Ũ���ᷴӦ��ȡ����,Ӧѡ�õ�װ��________,
����ɲ���ƽ�������ӷ���ʽ:___MnO4-+____Cl-+____H+![]() ___Mn2++___Cl2��+_____��
___Mn2++___Cl2��+_____��
��3����ѡ�â�Ϊ�������ռ�װ��,Ӧ�����Թܿڷ���һ����,������Ӧ��________��Һ��ʪ,��������________��
��4����ѡ�â�Ϊ�����ռ�װ��,������Ӧ��________��ͨ��.�û�ѧ�������������ռ����˵ķ�����________��
���𰸡� �� MnO2+4HCl![]() MnCl2+Cl2��+2H2O �� 2 10 16 2 5 8H2O �������� ��ֹ�����ݳ���Ⱦ���� A ��ʪ��ĵ���KI��ֽ����B�ڴ�����ֽ����ɫ��֤�������Ѽ���
MnCl2+Cl2��+2H2O �� 2 10 16 2 5 8H2O �������� ��ֹ�����ݳ���Ⱦ���� A ��ʪ��ĵ���KI��ֽ����B�ڴ�����ֽ����ɫ��֤�������Ѽ���
����������1���������̺�Ũ����ķ�Ӧ�ǹ�Һ��ϼ����ͣ�����ѡ���װ�ã��ڼ��������£��������̺�Ũ���ᷴӦ�����Ȼ��̡�������ˮ������ʽΪMnO2+4HCl![]() MnCl2+Cl2��+2H2O����2��KMnO4��Ũ����ķ�Ӧ�ǹ�Һ��ϲ���Ҫ���ȵģ�����Ӧѡ���װ�ã���Ӧ��MnO4-����Ԫ�صĻ��ϼ���+7�ۣ�Mn2+�Ļ��ϼ���+2�ۣ�����һ��MnO4-����Mn2+��5�����ӣ�����һ��Cl2������Ҫ2��������ʧȥ2�����ӣ����Ե�ʧ���ӵ���С��������10���ٸ���Ԫ���غ�֪���������л���ˮ�����Ը����ӷ���ʽ�еļ������ֱ�Ϊ��2��10��16��2��5��8H2O����3�������ж����ݳ�����Ⱦ���������Բ����������ݳ���������ˮ�ܷ�Ӧ������ʹ����ᣬ����ʹ��������ᣬ���ܺͼӦ�����Կ�������������Һ������������4���������ܶȴ��ڿ������ܶȣ�����Ӧ���������ſ������ռ���������AΪ�����ڣ������������Դ��ڵ�������ԣ������������û����⻯���еĵ⣬�ҵ������۱���ɫ�����Կ���ʪ��ĵ���KI��ֽ�����Ƿ��ռ���������������ʪ��ĵ���KI��ֽ����B�ڴ�����ֽ����ɫ��֤�������Ѽ�����
MnCl2+Cl2��+2H2O����2��KMnO4��Ũ����ķ�Ӧ�ǹ�Һ��ϲ���Ҫ���ȵģ�����Ӧѡ���װ�ã���Ӧ��MnO4-����Ԫ�صĻ��ϼ���+7�ۣ�Mn2+�Ļ��ϼ���+2�ۣ�����һ��MnO4-����Mn2+��5�����ӣ�����һ��Cl2������Ҫ2��������ʧȥ2�����ӣ����Ե�ʧ���ӵ���С��������10���ٸ���Ԫ���غ�֪���������л���ˮ�����Ը����ӷ���ʽ�еļ������ֱ�Ϊ��2��10��16��2��5��8H2O����3�������ж����ݳ�����Ⱦ���������Բ����������ݳ���������ˮ�ܷ�Ӧ������ʹ����ᣬ����ʹ��������ᣬ���ܺͼӦ�����Կ�������������Һ������������4���������ܶȴ��ڿ������ܶȣ�����Ӧ���������ſ������ռ���������AΪ�����ڣ������������Դ��ڵ�������ԣ������������û����⻯���еĵ⣬�ҵ������۱���ɫ�����Կ���ʪ��ĵ���KI��ֽ�����Ƿ��ռ���������������ʪ��ĵ���KI��ֽ����B�ڴ�����ֽ����ɫ��֤�������Ѽ�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���˿���Դ����ίԱ�ḱ���Ρ��й���ѧԺԺʿ�ش�ӱ�ʾ����ǰ�����ɢ��ú��û������ú������й������������߶�����������Ҫԭ��ú�������ǽ����������������ú̿����Ҫ;��֮һ��
����֪:H2O(g)=H2O(I) ��H=-44kJ/mol
���� | H2(g) | C(s) | CO(g) |
ȼ����kJ/mol | -285.8 | -393.5 | -283.0 |
����д��ú��������Ӧ���ɺϳ���(CO��H2)���Ȼ�ѧ����ʽ___________��
���ں��¡����ݵķ�Ӧ���У��ܱ���������Ӧ�ﵽƽ��״̬����_______��
a.�������ƽ����Է����������ٸı�
b.����ѹǿ���ٸı�
c.������Ũ�����
d.��Ӧ��ϵ���¶ȱ��ֲ���
e.���������������Ƕ�����������ʵ�2��
f.��������ܶȲ���
g.��λʱ���ڣ�����ˮ������������������������Ϊ9��1
���ڴ��������ºϳ����ϳɼ�������лᷢ�����·�Ӧ��
I CO(g)+3H2(g) = CH4(g)+H2O(g) ��H1= -206 kJ/mol
II CO(g)+H2O(g) = CO2(g)+H2(g) ��H2= -41 kJ/mol
�� 2CO(g)+2H2(g)= CH4(g)+CO2(g) ��H 3= -247.4 kJ/mol
��ͼ1��̫ԭ������ѧú�����о�����������ѧ���ݷ����õ��¶ȶԷ�Ӧ��InK(��ѧƽ�ⳣ��K����Ȼ����)������ͼ,����������������Ƶ�ԭ����____________��
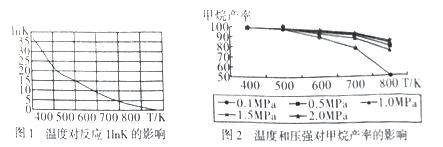
������鷴Ӧѡ���ԵĹؼ�������_______���������֪ʶ��ͼ2�����ϳɼ������˵ķ�Ӧ������
��550��630K��1MPa��ԭ����__________________��
��850��ʱ�����Ϊ5L��Ӧ���з�����Ӧ��CO��H2O(g)Ũ�ȱ仯��ͼ��ʾ������ʽ����������µ�ƽ�ⳣ��_____________ ��
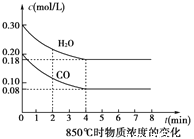
(3)CH4ȼ�ϵ�������ʺܸߣ�װ��������1L2mol/L��KOH��ҺΪ����ʣ���������ͨ���״���¼���22.4L��33.6 Lʱ�����缫��ӦΪ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�CO2�����öԴٽ���̼���Ĺ���������Ҫ���塣
��1����CO2�뽹̿��������CO��CO�����������ȡ�
����֪��Fe2O3(s)��3C(ʯī)=2Fe(s)��3CO(g) ��H1��akJ��mol��1
C(ʯī)��CO2(g)=2CO(g) ��H2��bkJ��mol��1
��CO��ԭFe2O3(s)���Ȼ�ѧ����ʽΪ______________��
��2����CO2ת��Ϊ�״����Ȼ�ѧ����ʽΪ�� CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ��H
CH3OH(g)+H2O(g) ��H
ȡһ�����CO2��H2�Ļ������(���ʵ���֮��Ϊ1��3)����������ܱ������У�����������Ӧ��
�����������˵����Ӧ�Ѵ�ƽ��״̬����________������ĸ����
A.�����������ܶȲ��� B.������������ѹǿ���ֲ���
C.���Ⱥ���ʱ��ƽ�ⳣ������ D.v��(CH3OH)=3v��(H2)
�ڷ�Ӧ�����в�ü״������������(CH3OH)�뷴Ӧ�¶�T�Ĺ�ϵ��ͼ��ʾ����÷�Ӧ�Ħ�H______0(�>������<������)��
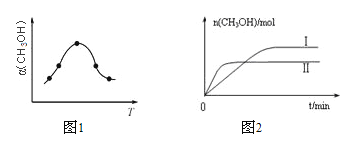
�������ֲ�ͬ�����·�����Ӧ�����CH3OH�����ʵ�����ʱ��仯��ͼ��ʾ������I�����Ӧ��ƽ�ⳣ����С��ϵΪK��_____K��(�>������<������)��
��3����CO2Ϊԭ�ϻ����Ժϳɶ������ʡ�
����ͼ��ģ�⡰�����Ƽ����ȡNaHCO3�IJ���װ�á�����������_____��ͨ��NH3���壬Ȼ������_______��ͨ��CO2���塣
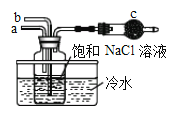
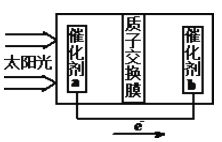
���˹���������ܹ�����̫������CO2��ˮ�Ʊ���ѧԭ�ϣ���ͼ��ͨ���˹���������Ʊ�HCOOH��ԭ��ʾ��ͼ����д������b���ĵ缫��Ӧʽ��________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����̼�������ס����Ԫ����ɵĵ����ʣ������ھ������������պ�����������ᣬ��Ӧ�����ȷ���ǣ� ��
A. ̼��̼�� B. �������� C. �������� D. ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����������������Ҫ��������
������һ��������Ũ������Ũ����Ļ����,���뷴Ӧ���У�
���������µĻ��������μ���һ�����ı�,�����,��Ͼ��ȣ�
����50~60���·�����Ӧ,ֱ����Ӧ������
�ܳ�ȥ������,�ֲ�Ʒ����������ˮ��5%��NaOH��Һϴ��,�����������ˮϴ�ӣ�
�ݽ�����ˮCaCl2�����Ĵ���������������,�õ�����������
��ش���������:
��1������һ������Ũ������Ũ��������ʱ,����ע��������___________��
��2���������,Ϊ��ʹ��Ӧ��50~60���½���,���õķ�����____________��
��3���������ϴ�Ӵ�������ʹ�õ�������_____________��
��4��������дֲ�Ʒ��5%��NaOH��Һϴ�ӵ�Ŀ����__________________��
��5��д�����������ķ���ʽ________��������������ɫ���ܶȱ�ˮ_____(�С����),����________��ζ����״Һ�塣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������·�����Ӧ��2A(g)+2B(g)![]() xC(g)+2D(g)����2L�ܱ������У���4molA��2molB��ϣ�2min��ﵽƽ��ʱ����1.6molC���ֲ�÷�Ӧ����VD=0.2mol/��Lmin��������˵����ȷ���ǣ�������
xC(g)+2D(g)����2L�ܱ������У���4molA��2molB��ϣ�2min��ﵽƽ��ʱ����1.6molC���ֲ�÷�Ӧ����VD=0.2mol/��Lmin��������˵����ȷ���ǣ�������
A. A��B��ת���ʾ���20% B. x=4
C. ƽ��ʱA�����ʵ���Ϊ2.8mol D. ƽ��ʱ����ѹǿ��ԭ����С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ����У������ɵ���ֱ�ӻ����Ƶã��ֿ��ɽ��������ᷴӦ�Ƶõ��ǣ�������
A.CuCl2
B.FeCl2
C.FeCl3
D.AlCl3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������漰�Ļ�ѧ���֪ʶ������˵����ȷ���ǣ� ��
A.ֲ���Ϳ�����Ϊ��ȡ���������ˮ�еĵ�
B.ʯ�͵ķ���ú����������ˮ��þ��������ѧ�仯
C.������ˮʱ����������Ϊ�����������Գ�ȥˮ�е�����
D.��ϩ�����顢SO2������ɫ���������ˮ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com